Резус-фактор
Резус-фактор – это белок, который может содержаться на поверхности эритроцитов человека. Он имеет большое значение при ведении беременности и при переливании крови.
Rh, Rh type, Rh typing, Rh-factor, rhesus factor.
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
- Исключить из рациона жирную пищу в течение 24 часов до исследования.
- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Резус-фактор – это белок, находящийся на поверхности эритроцитов у некоторых людей. Кровь тех, у кого он есть, называют резус-положительной, у кого нет – резус-отрицательной. Наличие или отсутствие этого белка является индивидуальной особенностью, а не патологией. Положительный резус-фактор встречается у 85 % людей, соответственно, отрицательный – у 15 %.
Особое значение резус-фактор имеет во время беременности. Если у матери положительный резус, то ее кровь будет в любом случае совместима с кровью ребенка, если отрицательный – возможны варианты: в том случае, когда у отца ребенка тоже отрицательный резус-фактор, кровь матери будет совместима с кровью плода, потому что и ребенок унаследует отрицательный резус, когда же у отца положительный резус-фактор, а у матери отрицательный, с вероятностью в 50 % может возникнуть несовместимость крови матери и ребенка – резус-конфликт, который грозит осложнениями.
Происходит это следующим образом: когда кровь плода попадает в кровоток матери, на его положительный резус в ее организме начинают вырабатываться антитела, так как белки на молекулах эритроцитов воспринимаются организмом матери как нечто чужеродное. Это не опасно для женщины, однако антитела через плаценту проникают в кровоток плода, что грозит ему негативными последствиями: антитела “приклеиваются” к эритроцитам плода и могут вызывать их слипание. Этот процесс называется гемолизом. Гемолиз во время беременности может привести к нарушениям развития плода и в некоторых случаях к выкидышу, а после рождения – к так называемой гемолитической желтухе новорождённых, при которой в крови младенца разрушается значительное количество эритроцитов. При этом кожа новорождённого желтеет, так как продукты распада эритроцитов окрашены именно в желтый цвет. Чаще всего поражается головной мозг, может развиться водянка. В тяжелых случаях младенцу требуется переливание крови.
Для чего используется исследование?
- Для определения возможного резуса-конфликта между матерью и плодом. Если определяется его высокая вероятность, женщине назначаются инъекции сыворотки, содержащей антирезус-иммуноглобулин, который связывается с эритроцитами плода и “скрывает” их от иммунной системы матери, что препятствует выработке антител к эритроцитам плода.
- Чтобы подобрать донора для безопасного переливания крови. Важно убедиться, что донорская кровь совместима с кровью реципиента. Если в донорской крови или ее компонентах есть антитела к белку, содержащемуся на эритроцитах реципиента, может развиться тяжелая трансфузионная реакция, вызванная разрушением эритроцитов в сосудистом русле. В настоящее время разрешено переливание только той крови, которая совпадает по группе и по резус-фактору у донора и у реципиента.
Когда назначается исследование?
- При беременности, чтобы подтвердить группу крови, резус-фактор и антирезусные антитела женщины. Эта информация имеет огромное значение при ведении беременности.
- При донорстве крови. Чаще всего переливание крови необходимо при:
- тяжелой анемии,
- кровотечении, возникшем у пациента во время или после операции,
- тяжелых травмах,
- значительных кровопотерях,
- онкологических заболеваниях и побочных эффектах химиотерапии,
- нарушении свертываемости крови, в частности гемофилии.
Что означают результаты?
Если у женщины резус-отрицательная кровь и положительный результат на антирезусные антитела, необходимо определение группы крови и резус-фактора отца ребенка. Если у отца отрицательный резус-фактор, дальнейшего обследования не требуется, если положительный – проводится дальнейшее наблюдение за динамикой уровня антирезусных антител в крови матери. При его повышении следует принять своевременное решение о терапии.
- Несовместимость матери и плода по резус-фактору в настоящее время не является препятствием для рождения здорового ребенка.
- Во время первой беременности резус-конфликта обычно не происходит, так как антитела вырабатываются медленно и в небольших количествах. При повторной беременности и последующих вероятность резус-конфликта возрастает.
Кто назначает исследование?
Акушер-гинеколог, врач-терапевт, врач общей практики, гематолог, трансфузиолог, хирург.
Как определить резус-фактор крови: методы анализа и интерпретация результатов
Наверное, каждый знает, что кровь человека имеет определенные характеристики. Первое, что приходит на ум, — это группа: I, II, III, IV. Вторая важная характеристика — резус-фактор. Но если о значении группы крови большинство имеет хотя бы базовое представление, то значение слова «резус» для многих остается непонятным.
Что же это за понятие и почему оно важно для каждого человека?
Что такое резус-фактор и почему о своем «статусе» нужно знать?
На самом деле, все довольно просто.
Наша кровь состоит из клеток, эритроцитов, на поверхности которых может быть специфический белок (антиген) — тот самый резус — либо его может не быть. В первом случае говорят о том, что кровь резус-положительная, во втором — резус-отрицательная. По статистике, 80–85% населения Земли имеют этот специфический белок. Люди, у которых антиген отсутствует, имеют одну важную особенность: при переливании (трансфузии) им «положительной» крови или при беременности, в случае вынашивания плода с противоположным резусом, организм может начать «атаку» на инородный белок. Это чревато серьезными осложнениями, вплоть до гибели пациента (при переливании) или ребенка (при вынашивании).
Поэтому резус-фактор нельзя не учитывать при планировании материнства или в экстремальных жизненных ситуациях, когда человеку необходимо стать донором или реципиентом крови.
Как узнать свой резус-фактор: положительный vs отрицательный
Поскольку резус — свойство крови, для того, чтобы определить его наличие или отсутствие, проводят анализ именно этого биоматериала.
Самый известный метод исследования — определение резус-фактора цоликлонами . В лабораторных условиях небольшое количество крови смешивают со специальной сывороткой. Если при этом начинается склеивание эритроцитов (агглютинация), резус считают положительным, в противоположном случае — отрицательным.
Есть и более совершенные методы, например гель-фильтрация . Кровь помещают в пробирку со специальным гелем с реагентами. При отрицательном резусе она проходит до самого дна, при положительном — начинается процесс склеивания и биоматериал остается в верхней части колбы. Данный метод более чувствительный и наглядный и в настоящее время применяется почти в 60% мировых клиник.
Ошибки при определении резус-фактора в современных условиях чрезвычайно редки, но все же встречаются. Они могут иметь технический характер, в частности, к ним приводит использование старых образцов крови, непрофессионализм персонала поликлиники (путаница с пробирками, неверная оценка результатов). Встречаются и ошибки по биологическим причинам: при некоторых заболеваниях печени, почек в крови могут присутствовать посторонние белки или бактерии, способные исказить результат.
Когда проводят определение резус-фактора крови
Несмотря на то, что наличие специфического белка на поверхности эритроцитов является очень важным показателем, многие люди живут, не зная свой статус. Проверить резус-фактор можно и без направления врача, однако в ряде случаев анализ обязателен:
- при подготовке к материнству и беременности;
- при гемолитической болезни новорожденных;
- при подготовке к хирургической операции, поскольку потенциально может понадобиться переливание крови или трансплантация;
- если человек выступает донором или реципиентом крови, костного мозга или органов.
Подготовка к исследованию и забор биоматериала
Процедура взятия образца биоматериала ничем не отличается от обычного (например, общего) анализа крови: медсестра собирает в пробирку немного венозной крови (в некоторых клиниках — капиллярной), запечатывает и маркирует пузырек. Процедура практически безболезненна для пациента и отнимает всего несколько минут.
Если анализ будет проходить в частной лаборатории или клинике, то с правилами подготовки к нему обычно можно ознакомиться на сайте соответствующего медцентра. Обычно соблюдения строгого режима перед исследованием не требуется, однако желательно, чтобы с последнего приема пищи прошло не менее четырех часов. В случае приема лекарств лучше уточнить у медиков, не повлияют ли они на результат теста: некоторые лекарственные средства, например, препараты метилдопа, способны искажать показатели.
Как расшифровать результаты
Анализ на резус-фактор — один из самых быстрых в исполнении. По результатам исследования пациент получает бланк, в котором стоит отметка Rh+ либо Rh-. Первый вариант означает наличие специфического белка, то есть положительный резус, второй — отрицательный.
Внимательного отношения требует лишь отрицательный резус. Во-первых, следует сообщать о нем в случае хирургических вмешательств, переливаний крови. Врачи обычно назначают контрольный анализ резуса непосредственно перед операцией или трансфузией, и если его результаты не совпали с данными предыдущих исследований, то это повод провести тест повторно.
Во-вторых, особенное значение отрицательный резус-фактор имеет для женщин, планирующих материнство. Если отец ребенка резус-положителен, плод может также иметь специфический белок в крови. В этом случае возможен резус-конфликт: организм матери может начать «атаку» на ребенка, что вызывает ряд тяжелых последствий, вплоть до гибели малыша.
Какие еще анализы могут потребоваться при определении резус-принадлежности и почему?
Отсутствие в крови специфического белка резуса в настоящий момент не является препятствием для вынашивания здорового ребенка. При первой беременности вероятность конфликта невелика даже при разных резусах матери и малыша. Однако по правилам, чтобы обезопасить плод, при отрицательном резусе будущей маме (если отец ребенка при этом резус-положителен) придется сдать ряд дополнительных анализов.
В первую очередь, это анализ на резус-антитела. Исследование необходимо для того, чтобы выявить, произошел ли резус-конфликт, начал ли организм матери «атаковать» плод. Анализ сдается несколько раз в течение беременности: при постановке на учет, а начиная с 18-20-ой недель — ежемесячно. Если организм начал вырабатывать антитела, женщине вводят специальные препараты, предотвращающие резус-конфликт. В сложных случаях может понадобиться госпитализация будущей мамы.
Существуют способы, позволяющие узнать резус-фактор плода на ранних стадиях беременности. Подобные исследования проводят, например, по крови матери, с использованием методов молекулярно-генетических исследований. Если белок отсутствует, то нет необходимости в профилактике — конфликта в этом случае не произойдет. Однако даже в этом случае специалисты не рекомендуют женщинам отказываться от дополнительного наблюдения и анализов на антитела: при определении резуса плода вероятность ошибки выше, чем у стандартных исследований.
Где можно сдать кровь на резус-фактор и группу крови?
Узнать о наличии или отсутствии в крови специфического белка довольно просто: в настоящий момент такое исследование проводят практически в любом медицинском центре. Это и государственные больницы, и частные клиники и лаборатории, а также пункты сдачи крови. На последних мы не будем останавливаться подробно, так как все-таки это не специализированные учреждения для сдачи анализов и не каждый может похвастаться отсутствием противопоказаний для донорства.
В городских и муниципальных больницах исследование на резус-фактор проводят бесплатно (при наличии полиса ОМС), однако только по направлению терапевта. Недостатком также можно считать очереди и необходимость забирать результаты лично. Многие жалуются на длительные сроки ожидания результатов, использование устаревших методов исследования и низкую квалификацию персонала в отдельных клиниках.
Частные медцентры и лаборатории проводят анализ гораздо быстрее (как правило, от нескольких часов до 1–2 суток), а результаты можно узнать онлайн, по телефону или получить по электронной почте. Обычно в таких центрах не приходится тратить время на ожидание своей очереди и получать направление. Оборудование в частных клиниках часто совершеннее и современнее, чем в государственных. Из недостатков — услуга платная: цена анализа крови на резус-фактор обычно составляет несколько сотен рублей.
Резус-фактор, как и группу крови, должен знать каждый: в экстремальных ситуациях это знание может спасти жизнь человеку или его близким. В обязательном порядке свой резус необходимо узнать женщинам, планирующим рождение малыша. Чтобы быть уверенным в достоверности анализа, лучше выбирать надежные клиники и лаборатории, работающие в соответствии с требованиями мировых стандартов.
Резус конфликт при беременности
Резус конфликт это состояние, которое развивается у беременной женщины с резус-отрицательной кровью в ответ на контакт с клетками крови, несущими резус антиген и приводящее к развитию антирезус антител.
Что такое антиген
Антиген это вещество, которое вызывает в организме иммунный ответ. Антигенами являются части вирусов, бактерий, растений и части клеток. Антиген вызывает в организме иммунные реакции, которые сопровождаются выработкой антител.
Что такое антитело
Антитело это белок, который вырабатывается иммунной системой организма в ответ на присутствие антигена. Антитела бывают разных типов. Есть антитела, которые вырабатываются быстро и исчезают, когда прекращается контакт с антигеном, например иммуноглобулины класса М. Есть антитела, которые вырабатываются медленно и могут находиться в организме спустя годы, после контакта с антигеном. К таким антителам относятся, например, иммуноглобулины класса G.

Взаимодействие антиген – антитело
Антиген имеет уникальную структуру. Например антигены вируса гепатита В отличаются от антигенов вируса гепатита С. Каждый антиген уникален. Антитело, которое вырабатывается иммуной системой является строго специфичным по отношению к тому антигену, который вызвал его образование. Например антитела к вирусу гепатита В отличаются от антител к вирусу гепатита С. Взаимодействие между антигеном и антителом возможно только в тех случаях, когда происходит встреча антител одного типа с антигенами того же типа. Такое взаимодействие напоминает ключ и замок. Замок –это антиген. Ключ – это антитело. Если ключ подходит к замку, взаимодействие происходит. Как правило взаимодействие антигена и антитела приводит к развитию иммунных реакций, которые приводят к элиминации (разрушению) носителя антигена.
Что такое резус-конфликт
Резус-конфликт развивается при взаимодействии антител к резус-фактору женщины с клетками крови, содержащими резус антиген. Взаимодействие приводит к разрушению клеток крови и развитию гемолиза с последующей анемией.
Что такое резус-фактор
Резус фактор это соединение на поверхности эритроцита (красного кровяного тельца). Название произошло от названия вида обезьян, у которых впервые обнаружили этот антиген. Резус –фактор является антигеном, то есть способен вызывать выработку антирезус антител. Существуют люди с кровью, клетки которой несут резус-антиген. Такую кровь называют «резус плюс». Люди, у которых резус-антиген отсутствует имеют кровь «резус-минус». Если в организм человека с «резус –минус» кровью попадет резус –положительная кровь, начнут вырабатываться антирезус антитела, которые приведут к разрушению клеток резус-положительной крови.
Как возникает резус-конфликт у беременных
Существует два механизма развития резус-конфликта у беременных. Первый, наиболее часто встречающийся, возникает при контакте резус-отрицательной крови матери с резус-положительной кровью плода при спонтанном или индуцированном аборте, при предшествующих родах и контакте с резус-положительной кровью ребенка, при акушерских диагностических манипуляциях (амниоцентез). Второй, менее частый, механизм обусловлен получением резус-положительной крови во время переливания крови.
Вследствие такого контакта в организме резус-отрицательной матери появляются антитела к резус-фактору, которые разрушают клетки резус-положительной крови. Достаточно одного контакта с резус-положительной кровью, чтобы в организме матери выработались антитела к резус фактору и остались на продолжительное время. Антирезус антитела способны проникать через плаценту и при последующей беременности, если плод имеет резус-положительную кровь, антитела матери могут разрушать его эритроциты. Разрушение эритроцитов плода ведет к гемолизу, вызывая аллоиммунно индуцированную гемолитическую анемию.
Какие процессы ведут к резус-конфликту при беременности
Считается, что около 30 % резус-отрицательных женщин не вырабатывают антирезус-антител и, следовательно, у них не развивается резус-конфликт. С другой стороны, есть женщины, у которых антирезус-антитела вырабатываются в значительных количествах при контакте всего лишь с 1 мл резус-положительной крови. Для того, чтобы количество антирезус-антител у матери уравновесилось с резус-антителами в крови плода, необходимо около одного месяца. Чаще всего контакт с резус –положительной кровью плода происходит во время родов и проходит для новорожденного незаметно, так как за краткое время не успевают выработаться антитела и не могут нанести вреда. При последующей беременности резус-положительным плодом на его организм уже будут воздействовать антирезус-антитела матери и у таких детей может развиться незначительная гемолитическая анемия. С каждой последующей беременностью количество антирезус-антител у матери нарастает и это влечет тяжелую патологию у резус-положительных детей, вплоть до внутриутробной смерти. Осложняется резус-конфликт также, если у матери и ребенка несовместимость и по группе АВО (общепринятое деление на группы крови).
Риск развития резус-конфликта зависит от трех причин
- Интенсивности кровотечения и количества контактирующей крови
- Выраженности иммунного ответа матери
- Наличия конфликта по системе АВО
Оценка риска развития резус-конфликта у беременных
Для прогнозирования развития резус-конфликта необходимо получить такую информацию:
- Проводилось ли когда-либо переливание крови
- Группа крови и резус фактор матери
- Резус фактор отца (у 55% мужчин с резус-полжительным фактором имеется гетерозиготность по резус-антигену и они могут давать резус –негативное потомство в 50 % случаев)
- Предшествующее применение антирезус иммуноглобулина G
- Количество предшествующих беременностей, включая аборты
- Механизм повреждений при травмах во время предшествующей беременности
- Наличие вагинальных или амниотических кровотечений
- Предшествующие инвазивные акушерские вмешательства, включая амниоцентез, кордоцентез, биопсию ворсин хориона и эктопическую (внематочную)беременность
Диагностика резус-конфликта при беременности
Всем беременным в обязательном порядке определяют группу крови и резус фактор. В том случае, если у беременной выявляют резус-отрицательную кровь, поводят определение уровня антител к резус –фактору.
Если женщина не была предварительно сенсибилизирована и не имеет антител к резус–фактору, то на этом исследования прекращают.
Если у женщины была предшествующая история, свидительствующая о возможности контакта с резус-положительной кровью, определяют резус-фактор мужа. Если у мужа резус-фактор отрицательный, дальнейшие наблюдения прекращают.
В том случае, если у женщины была история взаимодействия с резус-положительной кровью и имеются антитела к резус –фактору, становится вероятным развитие резус-конфликта и гемолитической анемии у плода. Таким беременным проводят анализ крови на содержание антител к резус-фактору. Определяют количество антител путем титрования. Титрование – это показатель концентрации антител. При значениях титров антирезус-антител от 8-до 32 исследования проводят раз в месяц до срока беременности 24 недели. Затем измерения антирезус-антител проводят каждые 2 недели. Если зафиксировано превышение титра антирезус-антител, возникает подозрение на начинающийся резус-конфликт. В этом случае, дополнительно к стандартным узи при беременности применяют допплеровское исследование средней мозговой артерии плода и измеряют в ней скорость кровотока.
Какие изменения при узи узи плода возникают при резус-конфликте у беременных
Резус-конфликт у беременных приводит к возникновению гемолиза (разрушению эритроцитов) плода. В связи с этим развивается гемолитическая анемия плода, повышается уровень билирубина, возникает повреждение головного мозга плода, сердечная недостаточность, отек легких плода и другие угрожающие состояния.
Узи диагностика при резус-конфликте беременных
При помощи узи при беременности можно выявить такие нарушения как, отек легких, сердечную недостаточность, гепато и спленомегалию, подкожные отеки, асцит и выпот в плевральных полостях. Очень точным методом определения нарушения сердечной деятельности при гемолитической болезни плода является допплерометрия. Измерение скорости в средней мозговой артерии плода выявляет повышение скорости кровотока в более, чем 1.5 раза по сравнению с нормой. До 20 недели признаки гемолитической болезни плода при резус-конфликте на узи не видны. Начиная с 20 недели узи проводят каждые 2-3 недели, а иногда и чаще.
Профилактика резус-конфликта при беременности
Профилактика резус конфликта проводится резус-отрицательным матерям, у которых отсутствуют антитела к резус-фактору. Для этой цели применяют антирезус иммуноглобулин G (RhoGAM). Механизм его действия таков: при введении в организм беременной антирезусный иммуноглобулин связывает резус-антигены на поверхности эритроцитов плода, которые попадают в материнский кровоток и тем самым тормозит иммунный ответ матери на резус-антиген плода. Как следствие, материнские антитела к резус-фактору не вырабатываются и резус-конфликт не развивается ни в текущей ни в последующих беременностях. В США профилактику резус-конфликта проводят на 28-32 неделе беременности. В некоторых случаях и после 40 недели (если беременность пролонгирована). Затем иммуноглобулин вводят повторно в течение 72 часов после родов. Также применяют антирезус иммуноглобулин каждый раз после амниоцентеза,биопсии ворсин хориона или при эпизоде вагинального кровотечения. В Украине принята однократная профилактика иммуноглобулином после родов.
Лечение при резус-конфликте у беременных
Для лечения развившейся гемолитической болезни новорожденных применяют внутриутробную гемотрансфузию (заменное переливание донорской крови), а при угрожающих жизни плода состояниях вызывают преждевременные роды в 32-34 недели.
в акушерстве и гинекологи мы работаем по таким направлениям как:
Лечим такие проблемы:
- Диагностическая гистероскопия (офисная)
- Хирургическая гистерорезектоскопия
- Диагностическая лапароскопия
- Лапароскопическая пластика маточных труб
- Лапароскопическая миомэктомия
- Лапароскопическое лечение внематочной беременност
- Лапароскопическое лечение эндометриоза
- Лапароскопическое лечение пролапса органов малого таза
- Лапароскопическое удаление кисты яичника
- Лапароскопическое лечение поликистоза яичников (дриллинг)
- Пластика малых половых губ
- Пластика влагалища после родов
- Хирургическое лечение недержания мочи
- Хирургическое лечение бартолинита (киста, абсцесс бартолиниевой железы)
БИОЛОГИЧЕСКИЙ ОТДЕЛ ЦЕНТРА ПЕДАГОГИЧЕСКОГО МАСТЕРСТВА
- Морфология растений
- Зоология беспозвоночных
- Микробиология
- Биохимия
- Анатомия растений
- Зоология позвоночных
- Цитология и гистология
- Молекулярная биология
- Альгология и микология
- Физиология человека и животных
- Биология развития
- Генетика
- Физиология растений
- Анатомия человека
- Экология
- Биосистематика
Группы крови. Резус-фактор
Автор статьи Зыбина А.М.
Группа крови — это описание индивидуальных антигенных характеристик эритроцитов. В качестве антигенов могут выступать как мембранные белки, так и углеводы, покрывающие их. Для человека известно несколько систем антигенов и все они должны быть учтены при переливании крови. В настоящее время известно около 30 систем групп крови, однако, наиболее клинически важными являются системы AB0 и резус-фактор.
Система АВ0
Эту систему групп крови открыл Карл Ландштейнер в 1900 году, за что в 1930 году ему была присуждена Нобелевская премия. Эритроцит покрыт плазмалеммой толщиной около 7 нм, в которую встроены антигены систем АВО и резус-фактор. В плазме крови каждого человека имеются антитела против антигенов эритроцитов, которые не содержатся в его собственной крови. К. Ландштейнер описал четыре группы крови (рис. 1). При смешивании крови, взятой у разных людей, при несовместимости групп крови, происходит агглютинация (склеивание) эритроцитов в результате реакции антиген – антитело.
Рис. 1. Четыре группы крови по системе АВ0.
В мембрану эритроцитов встроен целый ряд специфических полисахаридно-аминокислотных комплексов, обладающих антигенными свойствами. Гликозилирование обеспечивают специальные ферменты – гликозилтрансферазы, гены которых расположены в 9 хромосоме и имеют три разных аллеля: А, В и 0. Белок гена 0 переносит короткую олигосахаридную цепочку, в случае наличия гена А к этой цепочке дополнительно присоединен N-ацетил-D-галактозамин, при наличии гена В – D-галактоза (рис. 2). Работа глигозилтрансфераз А и В обеспечивает образование соответствующих агглютиногенов.
Рис. 2. Структура олигосахаридов H-антигена, отвечающего за группы крови системы АВ0.
В плазме крови образуются специфические агглютинины анти-А (α) и анти-В (β). По сути – это антитела, которые вырабатывает иммунная система. Они постоянно содержатся в крови человека и предполагается, что они вырабатываются как иммунный ответ на микрофлору кишечника. Чтобы не происходило агглютинации, одновременно в крови не должны находиться пары А и анти-А, В и анти-В. Поэтому иммунная система учится распознавать свои эритроциты и не реагировать на их агглютиногены.
Таким образом, возможны следующие комбинации:
- I (0) – анти-А+анти-В;
- II (А) – А+анти-В;
- III (В) – В+анти-А;
- IV (АВ) – А+В.
При переливании крови, чтобы не произошло склеивания красных кровяных телец, нужно, чтобы эритроциты донора не содержали агглютиногенов, к которым в плазме крови реципиента есть агглютинины. Схема переливания крови представлена на рис. 3. Эритроциты I группы крови не содержит агглютиногенов, ее можно переливать любому реципиенту, людей с такой группой крови называют универсальными донорами. Эритроциты IV группы крови содержат оба агглютиногена, но в плазме нет агглютининов, следовательно, людям с такой группой крови можно переливать любую другую, и таких людей называют универсальными реципиентами.
Рис. 3. Схема переливания крови.
Исключением из этой схемы является Бомбейский феномен. Он был открыт при переливании крови людям во время вспышки малярии в Индии в 1952 году. Оказалось, что у некоторых людей не образуется олигосахаридный остов, на который глигозилтрансферазы А и В переносят дополнительные сахара. Таким образом, даже при наличии генов А и В, гликозилтрансферазы не имеют субстрата, с которым могут работать. У таких людей, помимо наличия агглютининов анти-А и анти-В, агглютинация возникает даже при переливании I группы крови. Носители такой крови являются универсальными донорами.
Анализ группы крови провести достаточно просто. Для этого, каплю исследуемой крови смешивают с сыворотками I-III групп крови. В зависимости от того, где произошла агглютинация, можно выяснить группу крови (рис. 4). В случае Бомбейского феномена, агглютинация произойдет во всех трех лунках. В настоящее время вместо сывороток используют цоликлоны – моноклональные антитела к агглютиногенам.
Стоит отметить, что реакция агглютинации происходит между эритроцитами и плазмой крови. При смешивании плазмы крови разных групп агглютинации не произойдет.
Рис. 4. Анализ групп крови. 1 – I (0) группа, 2 – II (А) группа крови, 3 – III (В) группа крови, 4 – IV (АВ) группа крови.
Резус-фактор
Резус-фактор – это группа антигенов, среди которых самым реакционноспособным является антиген D. Именно поэтому, говоря о положительном или отрицательном резусе, подразумевают именно его. Резус фактор может находиться на мембране эритроцитов, в таком случае он считается положительным (85% людей), либо отсутствовать – в таком случае он считается отрицательным (15% людей). Резус-фактор имеет важное диагностическое значение не только для переливания крови, но и для нормального протекания беременности.
В отличие от системы АВ0, антитела к антигену D не всегда имеются у людей с отрицательным резусом. Чтобы они появились, необходим первичный контакт с эритроцитами, содержащими этот антиген. Это может произойти при некорректном переливании крови, а также во время родов (если ребенок резус-положительный). После контакта антитела вырабатываются достаточно долго, несколько месяцев. Однако, если организм был иммунизирован, то антитела сохраняются в течение всей жизни.
В настоящее время, случаи некорректного переливания крови редки, поэтому резус имеет большее значение для нормального протекания беременности у резус-отрицательных женщин.
Если резус-отрицательная мать беременна резус-положительным ребенком, то первая беременность протекает нормально, так как антител нет, а эритроциты не проникают через гематоплацентарный барьер. Во время родов этот барьер нарушается, и эритроциты ребенка могут попасть в организм матери, что приведет к выработке антител (рис. 5). При повторной беременности резус-положительным ребенком готовые антитела будут проникать через плаценту, что приведет к возникновению гемолитической болезни новорожденных, которая характеризуется гемолизом эритроцитов, что, в свою очередь, приводит к желтухе и нехватке кислорода у плода (рис. 6).
В настоящее время есть множество способов избежать атаки плода антителами, в частности, плазмоферрез – очищение плазмы крови матери от антител. Однако самым эффективным способом является предотвращение резус-конфликта при повторной беременности. Для этого в течение 72 часов после родов женщине вводят антирезусный иммуноглобулин. Таким образом, эритроциты ребенка, попавшие в кровоток матери, быстро уничтожаются, а иммунитет не успевает обучиться их распознавать.
Рис. 5. Причины резус-конфликта.
Рис. 6. Причины и симптомы гемолитической болезни новорожденных.
Как определяют значение резус-фактора? Какие современные методики применяются в лабораториях? Что такое резус-конфликт?
Генетические особенности резус-фактора и возможности диагностики
В составе системы группы крови Резус (Rhesus, Rh) выделяют 5 антигенов с наибольшим значением для клинической практики: D (резус-фактор), C, с, E и е. Белки, формирующие эти антигены, кодируются 2 генами: RHD (антиген D) и RHCE (антигены C, с, E и е). Эти гены и получающиеся с них белки очень похожи. Такое сходство осложняет генотипирование по этим генам. Дело в том, что для оценки риска развития резус-конфликта нужно знать вероятность появления Rh+ эмбриона у каждой пары, планирующей беременность. Для расчета этой вероятности необходимо установить генотип отца и матери по гену RHD.
В первую очередь в группу риска попадают женщины с отрицательным резус-фактором. Если партнер тоже имеет резус-отрицательный статус, то беременность точно будет протекать без развития резус-конфликта и дополнительные обследования такой паре не нужны. В первую очередь в группу риска попадают женщины с отрицательным резус-фактором. Если партнер тоже имеет резус-отрицательный статус, то беременность точно будет протекать без развития резус-конфликта и дополнительные обследования такой паре не нужны.
Если отец является гомозиготой, то есть обе гомологичные хромосомы несут полноценный ген RHD, то вероятность получения Rh+ эмбриона в такой паре равна 100%, так как для положительного резус-фактора нужна хотя бы одна хромосома с этим геном, которая обязательно придет от гомозиготного Rh+ отца. В этом случае врач-генетик ничего не сможет предложить в качестве способа предотвращения резус-конфликта и паре следует обратиться к врачу, ведущему беременность. Врач составит индивидуальный план профилактики резус-конфликта.
Если же у мужчины на одной из хромосом отсутствует ген RHD, то существует 50% вероятность того, что среди эмбрионов будут резус-отрицательные, с которыми беременность будет протекать без осложнений со стороны резус-фактора.
Однако большое сходство последовательностей генов RHD и RhCE усложняет не только диагностику по этим генам и группе крови Rhesus, но и оценку рисков по развитию резус-конфликта. У других млекопитающих есть только один ген, который больше похож на человеческий RhCE. Предположительно у человека ген RHD появился в качестве дубликата RhCE и со временем немного изменился, найдя свою функцию в организме. Таким образом, одной из главных особенностей генетической диагностики резус-фактора является анализ нескольких локусов этого гена. Дело в том, что из-за схожести генов анализ одного локуса с большой для диагностического теста вероятностью может дать ложноположительный ответ, то есть вместо гетерозиготы по делеции RHD гена мы увидим гомозиготу с двумя копиями RHD из-за того, что в анализ сделает ложный вклад ген RhCE. Для точной диагностики в нашей лаборатории используется современная методика MLPA, основанная на анализе сразу большого количества точек в этих генах, что позволяет не только точно диагностировать отсутствие/наличие гена RHD, но и выявить его другие особенности, о которых расскажем дальше в следующей статье на нашем сайте. С помощью этого метода можно с высокой точностью генотипировать будущих родителей и проводить инвазивную пренатальную диагностику при естественной беременности для того, чтобы вовремя приступить к профилактическим мерам по устранению развития резус-конфликта.
При преимплантационной диагностике эмбрионов (ПГД) для еще большей уверенности мы проводим анализ двумя различными способами. В первую очередь, с помощью разработанной в нашей лаборатории тест-системы для прямого анализа мутации: мы генотипируем именно наличие/отсутствие делеции гена RHD. Однако при ПГД используется очень маленькое количество биоматериала, что может привести к ложным результатам, поэтому результаты прямого анализа мутации в нашей лаборатории всегда дополняются проверкой групп сцепления. Дело в том, что в геноме человека есть такие последовательности, короткие повторы нуклеотидов, длина которых очень отличается у разных людей. Поэтому если узнать длину нескольких таких повторов у одного человека, его с высокой вероятностью можно будет отличить от всех других людей на Земле по набору длин этих участков. Причем по длинам этих участков мы можем различать не только людей, но и гомологичные хромосомы одного человека. Поэтому мы подбираем такие вариабельные участки, которые наиболее близко расположены к гену, чтобы избежать эффектов рекомбинации, узнаем длины этих участков у родителей и получаем четыре набора длин, описывающих каждую из четырёх родительских хромосом – две маминых и две папиных. Это такая характеристика каждой хромосомы. При этом мы уточняем, на какой из отцовских хромосом находится опасный для беременности резус-отрицательной женщины ген RhD. Косвенная диагностика заключается в том, чтобы посмотреть, какие хромосомы получил эмбрион от родителей и вычислить, получил ли он ту отцовскую хромосому, на которой находится ненужный нам ген, или нет. Соответственно, если женщина резус-отрицательна, а ее партнер гетерозиготный резус-положительный носитель гена RHD, то для профилактики резус-конфликта мы отбираем такие эмбрионы, у которых нет гена RHD ни на одной из хромосом. Двойная проверка результата двумя независимыми тест-системами, основанными на разных принципах, позволяет получить высокоточный достоверный результат даже на малых количествах биоматериала, с которыми приходиться работать в рамках ПГД.
О редких вариантах гена RHD и точности биохимического и генетического анализа статуса по резус-фактору, а также о том, как обезопасить себя и свою семью в таких случаях, мы расскажем в следующей статье на нашем сайте.
Определение группы крови и резус принадлежности
Крайне важное значение для клинической практики имеет определение антигенов эритроцитов – идентификация группы крови и резус-фактора. Группа крови человека определяется наличием на поверхности эритроцита антигенов и является индивидуальным признаком. Эритроцитарные поверхностные антигены эритроцитов определяет фенотип эритроцитов или группу крови человека.
В настоящее время известно более 200 антигенов эритроцитов, поэтому группа крови может отличаться в зависимости от количества используемых антисывороток для идентификации антигенов на поверхности эритроцитов. Эритроцитарные антигены, идентифицированные в популяции в 1% случаев, считаются редкими.
Основной системой идентификации групп крови является система АВО, в которой группа крови характеризуется наличием на поверхности эритроцитов антигенов А, В, АВ или их отсутствием (О), т.е. четыре группы крови. В некоторых руководствах встречается дополнительная маркировка групп крови: О (I); А(II); В (III) и АВ (IV).
Выявление в 1901 г. эритроцитарных антигенов положило начало изучению допустимости смешивания эритроцитов разных групп, т.е. совместимости гемотрансфузий. В крови (сыворотке) каждого индивидуума циркулируют антитела (называемые так же агглютинины), активные в отношении чужеродных антигенов. Взаимодействие антиген-антитело приводит к агглютинации (слипанию) и разрушению эритроцитов. В крови индивидуумов с группой крови А циркулируют антитела против антигенов В. Индивидуумы с группой крови В имеют антитела, против антигенов А. При группе крови О в сыворотке определяются антитела анти-А, анти-В, тогда как при группе крови АВ ни антитела А, ни антитела В в сыворотке не определяются.
Таким образом, индивидуумы с группой крови АВ являются универсальными реципиентами иногрупной крови.
Индивидуумы с группой крови О, эритроциты которых не имеют на поверхности ни А, ни В антигенов, являются универсальными донорами.
Антитела к эритроцитарным антигенам А или В являются генетически детерминированными, в соответствии с группой крови эритроцитов, тогда как антитела к другим поверхностным антигенам эритроцитов являются приобретенными. Пациенты, получающие трансфузии, со временем накапливают антитела, что может осложнять подбор требуемой группы крови. Для таких пациентов важно выполнять типирование группы крови с оценкой возможно большего спектра антител сыворотки.
Группа крови оценка совместимости
Для оценки совместимости групп крови и возможности трансфузий необходимо исследование реакции антител сыворотки донора и эритроцитов реципиента, а также эритроцитов донора и антител сыворотки реципиента.
При совместимости групп крови смешивание эритроцитов и сыворотки не приводит к изменению состава и окраски реакционной капли.
При несовместимости групп смешивание эритроцитов донора и сыворотки пациента вызывает реакцию агглютинации – образование в капле неоднородностей в виде слипшихся эритроцитов, точечно насыщающих поле реакции.
Резус-фактором (Rh) называют антиген D, который может располагаться на поверхности эритроцитов. Наличие или отсутствие этого антигена на поверхности эритроцитов индивидуума определяет такую характеристику группы крови, как резус положительная или резус отрицательная (Rh+ или Rh–). Примерно 85% популяции людей имеют резус-положительную группу крови (Rh+).
В отличие от антител к антигенам АВ, антитела к антигену D не присутствуют в крови. При контакте крови резус-положительной группы с резус-отрицательной, происходит сенсибилизация и синтез анти-резусных антител. Такая реакция развивается, например, при беременности Rh– матери Rh+ плодом. Выход фетальных клеток во время родов в кровоток матери активизирует синтез антирезусных антител. В случае пересечения антирезусными антителами плацентарного барьера и попадания в кровь плода, развивается гемолитическая желтуха новорожденного, обусловленная разрушением эритроцитов.
Определение резус фактора необходимо для каждого индивидуума в дополнение к определению группы крови. Отмечено, что выраженность структуры эритроцитарного антигена различна у здоровых людей и тем более у иммуноскомпроментированных больных, беременных женщин.
В настоящее время определение групп крови, резус фактора, продукции антиэритроцитарных антител выполняется в автоматическом режиме стандартизированными методами, позволяющими одномоментно проводить как типирование групп крови, определение продукции антител, так и совместимости возможных трансфузий. Визуальное отображение полученной карты для каждого пациента может быть востребовано в течение всей жизни пациента, она хранится в базе данных лаборатории.
Показания к исследованию: Любое стационарное лечение, беременность.
Условия взятия и хранения образца
Для исследования используется венозную кровь, взятую с ЭДТА или без консервантов. Взятие крови производится натощак, или не менее чем через 8 ч после последнего приема пищи. Образец крови может храниться при температуре от 4–8 °С не более 24 ч.
Результаты исследования
Группа крови системы АВО:
- 0 (I) – первая группа;
- A (II) – вторая группа;
- B (III) – третья группа;
- AB (IV) – четвертая группа крови.
При выявлении подтипов (слабых вариантов) групповых антигенов результат выдается с соответствующим комментарием, например, «выявлен ослабленный вариант А2, необходим индивидуальный подбор компонентов крови».
Резус принадлежность
- Rh (+) положительная;
- Rh (–) отрицательная.
При выявлении слабых и вариантных подтипов антигена D выдается комментарий: «выявлен слабый резус-антиген, рекомендуется при необходимости выполнять трансфузию резус-отрицательных компонентов крови».
Как определяют значение резус-фактора? Какие современные методики применяются в лабораториях? Что такое резус-конфликт?

Аутоиммунные свойства крови являются одним из важнейших для практической медицины разделов нормальной физиологии. Своевременная трансфузия компонентов крови ежедневно спасает жизни многих людей. К сожалению, не всегда удается избежать грозных осложнений, вызванных переливанием крови. Тем более важным в образовании врачей представляется глубокое проникновение в суть аутоиммунных процессов. Наибольшее число проблем, связанных с переливанием крови, обусловлено высоким полиморфизмом самой иммуногенной из 30 систем групп крови –системы группы крови резус. Представление об иммуногенетической характеристике резус-антигенов необходимо для понимания механизмов несовместимости переливаемой крови и позволит снизить число трансфузионных осложнений.
1. Номенклатура антигенов системы RH
Система группы крови RH (резус) была открыта в 1940 г. Карлом Ландштейнером и Александром Винером [21]. Система RH представлена несколькими десятками антигенов, многие из которых возникли вследствие генных мутаций. В наши дни в научной литературе в основном применяются две номенклатуры антигенов системы резус: Фишера-Рeйса (Fisher-Race) и Винера (Weiner). По Фишеру-Рeйсу [31] наиболее клинически значимые антигены системы Rh обозначаются литерами D, С, Е, си е, по Винеру– Rh0,rh΄,rh΄΄,hr΄и hr΄΄ соответственно [37]. По убыванию иммуногенности резус-антигены располагаются в следующей последовательности:D, c, E, C и e. Антиген D встречается у 85% европейцев, С – у 70%, с– у 85%, Е– у 30%ие– у 97%.
2. Гены. Структура антигенов
Клинически значимые резус-антигены кодируются двумя тесно связанными генами – RHD и RHСЕ. Эти гены располагаются в локусе RH 1-й хромосомы. Ген RHСЕ имеет аллели RHce, RHCe и RHcE [7]. Ген RHD парного аллеля не имеет. Отсутствие рецессивного аллеля гена RHD, связанное чаще всего с делециейэтого гена [32], принято обозначать прописной литерой d. Аллели локуса RH всегда наследуются вместе в различных комбинациях: DCE, DCe, DcE, Dce, dCE, dCe, dcE и dce [16]. Лица, у которых ген RHDприсутствуетна обеих гомологичных хромосомах или на одной из них, являются D-положительными.Люди, у которых ген RHD отсутствуетна обеих гомологичных хромосомах, считаются D-отрицательными. Среди европейцев D-отрицательных людей 15-17%, в Южной Африке – 5%, в Японии, Китае, Монголии и Корее – 3% [13; 33]. Напротив, у басков лишь 34%D-положительных лиц. Отметим, что у европецев основной причиной D-отрицательности является делеция гена RHD, в то время как у африканцев и азиатов часто выявляется неактивный (молчащий) ген RHD [25] или гибридный ген RHD-СЕ-D [16], не экспрессирующий антиген D [11]. 20%D-отрицательных японцев имеют резус-фенотип DEL, характеризующийся очень низким уровнем экспрессии антигена D.
Прорыв в понимании молекулярных основ системы резус произошел в 90-х годах прошлого века, когда были клонированы гены локуса RH – ген RHD и ген RHСЕ [22]. Выяснилось, что эти гены кодируют две белковые молекулы, встраивающиеся в мембрану эритроцитов, –белокRhD и белокRhCE[4]. Частью аминокислотной структуры одного из этих белков – белка RhD– является антиген D. Белок RhCE, в отличие от белка RhD, формирует два резус-антигена –антиген С(или с) и антиген Е (или е), наследуемых в блоке в разных комбинациях: СЕ, Се, сЕ или се. Наличие двух различных антигенных детерминант в одной молекуле белка подтверждается выработкой двух типов антител в ходе иммунного ответа, инициированного белком RhCE, – анти-С (или анти-с) и анти-Е (или анти-е) [5].
Белки RhD и RhCE на 92% идентичны по структуре (аминокислотному составу и конформации) в связи с высокой гомологичностью кодирующих их генов RHD и RHСЕ, обусловленной, вероятно, генной дупликацией [30]. Оба белка состоят из 416 аминокислот и отличаются лишь 35 аминокислотами. В мембране одного эритроцита содержится от 10 до 30 тысяч молекул ключевых резус-антигенов. Резус-протеины RhD и RhCE– это молекулы, 12 раз пересекающие мембрану эритроцитов в направлении от внутренней поверхности к наружной и затем вновь ко внутренней с С- и N-концами, ориентированными к цитоплазме [9] (рис. 1).
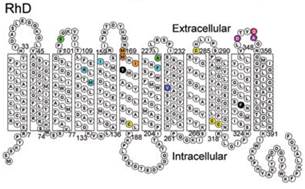
Рис. 1. Структурная организация протеина RhD
(из ConroyM. etal., BritishJournalofHaematology. 2005)
Некоторые участки этих белковых молекул, выступающие шестью петлями над наружной поверхностью мембраны эритроцитов, обладают свойствами эпитопов – детерминантных областей антигена [12]. Применение моноклональных антител, способных взаимодействовать с эпитопами лишь одного типа, позволило выявить в молекуле протеина RhDэпитопы 36 различных типов. Есть основания полагать, что в мембране эритроцитовD-положительных людей два ключевых резус-протеина RhD и RhCE образуют резус-комплекс с двумя молекулами резус-ассоциированного гликопротеина – RhAG. У D-отрицательных лиц резус-комплекс, возможно, содержит две RhCE субъединицы (обычно се) и две RhAG субъединицы [39].
Гликопротеин RhAG на 40% идентичен белкам RhD и RhCE, что указывает на его принадлежность к семейству резус-протеинов, и он, также как белки RhD и RhCE, 12 раз пересекает мембрану эритроцитов. Семейство резус-протеинов составляют ключевые резус-белки эритроцитов – носители антигенов D, С (или с), Е (или е) – и резус-ассоциированный гликопротеин RhAG [27]. С резус-семейством ассоциированы десятки дополнительных (accessory) гликопротеинов [17]. Очевидно, что столь значительное разнообразие антигенных белков системы резус, связанное с выпадением отдельных нуклеотидов, точечными нуклеотидными заменами в цепи ДНК, транслокацией, изменением экспрессии антигенов и пр., делает эту систему самой полиморфной из всех известных на сегодняшний день систем групп крови. Генетические исследования последних лет выявили случаи обменов между генами RHD и RHСЕ. Мутантные гены кодировали гибридные резус-протеины, у которых имелись RhD-специфические области в молекуле Rhсе-протеина и наоборот [8]. Эритроциты, содержащие гибридные резус-протеины Rhсе, могли взаимодействовать с некоторыми моноклональными антителами анти-D.
Показано, что для экспрессии белков RhD и RhCE в мембрану эритроцитов необходим гликопротеин RhAG [29]. В отсутствие протеина RhAG нарушается процесс сборки и переноса из цитоплазмы в мембрану эритроцитов ключевых белков резус-комплекса – белков RhD и RhCE. Это подтверждается одним из фенотипов системы RH – фенотипом резус-ноль (Rhnull). Rhnull может быть следствием мутации одного из генов большого комплекса резус-генов – гена RHAG, блокирующей образование резус-ассоциированного гликопротеина RhAG. Оказалось, что в мембране эритроцитов лиц фенотипа Rhnull отсутствуют не только молекулы протеинаRhAG, но и резус-протеиныRhD и RhСЕ [20]. При этом лица Rhnull могут передавать по наследству антигены семейства Резус своим детям (по аналогии с Бомбейским фенотипом). Имеются сведения о наличии у лиц фенотипа Rhnull естественных антител ко всем ключевым антигенам системы резус.
Важно отметить, что у носителей фенотипа Rhnull были выявлены морфологические и физиологические изменения эритроцитов [18]. В красных клетках крови повышалось осмотическое давление, они приобретали форму сфероцитов, уменьшалась продолжительность их жизни, наступал гемолиз [38]. Эти наблюдения, а также множество специальных исследований убеждают в том, что семейство резус-белков является существенной составляющей цитоскелета эритроцитов и участвует в транспорте воды и аммониячерез его мембрану [6; 19; 24].
Ключевые антигены системы RH начинают синтезироваться примерно с 6-й недели внутриутробного развития плода. Экспрессия белков с резус-антигенами в мембрану пронормобластов отмечается уже на 38-42-й день эмбриогенеза. Неэритроидные гомологи резус-белков обнаружены в печени, почках, головном мозге и коже. Эти белки осуществляют трансмембранный перенос аммония в клетках, составляющих эти органы [26].
3. Некоторые варианты антигена D, образовавшиеся в результате мутаций гена RHD
А. D weak – слабый антиген D
У лиц фенотипа Dweak (от англ. weak – слабый), а они составляют 1,5% среди резус-положительных, вследствие точечной мутации гена RHD снижена экспрессия антигена D на мембране эритроцитов [40]. В связи с этим антиген Dweak не может быть идентифицирован рутинным методом – прямой агглютинацией с использованием сывороток анти-D. Во избежание ошибочного отнесения лиц фенотипа Dweak к числу D-отрицательных, кровь всех D-отрицательных доноров должна быть исследована специальными методами на наличие антигена Dweak[35].
Доноры с антигеном Dweak определяются как резус-положительные(D-положительные), т.к. их эритроциты могут стимулировать образование антител анти-D у D-отрицательных реципиентов. При переливании эритроцитов фенотипа DweakD-положительным реципиентам антитела анти-D не продуцируются. Синтез анти-D в противоположной ситуации – у реципиентов Dweakпри переливании им D-положительных эритроцитов – ранее считался маловероятным. Однако в последние годы появляются сведения о случаях иммунизации Dweakреципиентов D-положительными эритроцитами [14]. В связи с этим реципиентов с антигеном Dweak в трансфузионных процедурах рекомендуют вести как резус-отрицательных (D-отрицательных).
При определении резус-принадлежности лаборатории выдают лицам фенотипа Dweak комментарий: «Выявлен слабый резус-антиген (Dweak), рекомендуется при необходимости переливать резус-отрицательную кровь». Впрочем, вопрос об иммунных свойствах фенотипа Dweak продолжает активно обсуждаться в научных кругах [15].
Б. D partial – частичный антиген D
Частичный(парциальный, вариантный) антиген D–Dpartial– отличается от антигена Dотсутствиемодного или нескольких из известных 36-ти эпитопов[3]. При этом количество RhD-протеинов в мембране эритроцитов остается таким же, как у лиц с нормальным антигеном D. У реципиентов Dpartialвозможно образование антител против недостающих эпитопов антигена D при переливании им D-положительной крови или во время беременности [36]. В связи с этим реципиенты фенотипа Dpartialсчитаются D-отрицательными, а доноры – D-положительными. Некоторые Dpartialявляются результатом точечных мутаций в гене RHD, другие возникают вследствие гибридизации генов RHD и RHСЕ.
В. Фенотип DEL
Фенотип DEL широко распространен у азиатских этносов. В Китае и Японии он составляет до 17% от числа резус-отрицательных лиц, выявленных серологически. У европейцев встечается очень редко. Характеризуется исключительно низкой экспрессией антигена D. Несмотря на это обстоятельство, эритроциты фенотипа DEL могут вызывать иммунную реакцию у D-отрицательных реципиентов [41]. До сих пор нет серологических реагентов, которые определяли бы этот фенотип. Идентификация доноров DEL производится лишь генетическим скринингом [34]. Поскольку DEL принадлежит к числу слабых D-фенотипов, на представителей этого фенотипа распространяются те же рекомендации по поводу гемотрансфузии, что и на лиц Dweak: доноры считаются резус-положительными (D-положительными), а реципиенты – резус-отрицательными (D-отрицательными).
4. Антирезус антитела
Антитела антирезус являются иммунными антителами [23]. В отличие от естественных антител системы АВ0, антитела к антигенам системы резус вырабатываются в процессе иммунных реакций (изосенсибилизации).
Антитела к антигенам системы резус, образующиеся при первичном иммунном ответе, в основном принадлежат к иммуноглобулинам М, серологически определяются через несколько недель после встречи с антигеном (чаще всего), достигают максимальной концентрации через 1-2 месяца. Антитела, синтезированные при вторичном иммунном ответе, в значительной степени принадлежат к иммуноглобулинам G, появляются в крови через несколько дней после внедрения антигена и сразу в высокой концентрации.
IgM и IgG, связавшись с соответствующими антигенами эритроцитов, активируют комплемент по классическому пути и фагоцитирующие клетки крови.
5. Определение резус-совместимости при переливании крови
Резус-антигены могут быть выявлены рядом методов:
– реакцией агглютинации с моноклональными антителами анти-D, анти-С, анти-с, анти-E, анти-е;
– реакцией агглютинации с универсальным реагентом антирезусD;
– другими высокоэффективными и надежными методиками [1].
Длядоноров в наши дни чаще всего применяется следующий алгоритм определения резус-принадлежности. Универсальным реагентом антирезусD, содержащим антитела анти-D, в эритроцитах донора выявляется антиген D: агглютинация эритроцитов антителами анти-D указывает на наличие антигена D на поверхности эритроцитов, отсутствие агглютинации – на отсутствие антигена D. Если антиген D не обнаружен, эритроциты донора обследуются моноклональными антителами анти-С и анти-E на наличие антигенов C и E [1].
Доноры, в эритроцитах которых обнаружен хотя бы один из ключевых резус-антигенов, обозначаемых заглавными буквами (D, и/или C, и/или E), cчитаются резус-положительными. Лица, у которых отсутствуют антигены D, C и E (фенотип dce), являются резус-отрицательными донорами. У реципиентов определяется антиген D универсальным реагентом антирезусD.
В том случае, если все ключевые резус-антигены выявляются моноклональными антителами, важно иметь в виду, что МАО синтезируются invitro одним штаммом плазматических клеток [2]. Эти антитела комплементарны лишь к одному типу эпитопа антигена. Если, к примеру, в исследуемых D-положительных эритроцитах данная детерминанта отсутствует (как у Dpartial), кровь будет считаться D-отрицательной со всеми вытекающими отсюда последствиями. Во избежание подобных ошибок эритроциты, идентифицированные МКА как D-отрицательные, должны дополнительно типироватьсяполиклональными анти-D антителами, содержащимися в универсальном реагенте антирезусD. Это связано с тем, что один антиген может содержать несколько разных или/и одинаковых эпитопов, при этом всеэпитопы одного антигена способны связываться с антителами, синтезированными в организме (invivo) всеми штаммами плазмоцитов в ответ на внедрение данного антигена–поликлональными антителами.
Универсальный реагент антирезусD является сывороткой крови D-отрицательных лиц группы крови АВ (IV), сенсибилизированных к антигену D предыдущими беременностями и/или трансфузиями крови, а также искусственно иммунизированных доноров-добровольцев. В этой сыворотке содержатся антитела анти-D. Универсальной сыворотку делает отсутствие в ней естественных антител анти-А и анти-В, которые могут агглютинацией по системе АВ0 замаскировать специфическое взаимодействие антител анти-Dс антигеном D.
В особых случаях (пока еще) для определения резус-совместимости пар «донор – реципиент» на cтанциях переливания крови производится фенотипирование крови по резус-антигенам. Фенотипирование– это серологическое типирование эритроцитов по всем главным антигенам системы резус –D, C, c, Eи e. При необходимости также определяются некоторые слабые резус-антигены и парциальные антигены D. В трансфузиологическом сообществе России обсуждается вопрос о необходимости введения в нашей стране обязательного фенотипирования доноров по 9 трансфузионно значимым антигенам – А, В, D, с, Е, С, е, Кеllи Cw, – шесть из которых представляют самую иммуногенную из 30-ти систем групп крови – систему резус [10]. Только индивидуальный подбор пар «донор-реципиент», основанный на совместимости их резус-фенотипов, может обеспечить безопасность переливания крови.
6. Природа резус-несовместимости при гемотрансфузии
Резус-несовместимость может быть вызвана двумя причинами – иммунизацией реципиента отсутствующим в его эритроцитах резус-антигеном (антигенами) донора или введением эритроцитов аллоиммунизированному реципиенту [28]. Рассмотрим на нескольких примерах механизм иммунизации реципиентов в процессе трансфузии резус-несовместимых эритроцитов.
1. Предположим, по причине недостаточной оснащенности серологической лаборатории у донора не выявленсодержащийся в его эритроцитахслабый антиген D–Dweak. Констатация отсутствия антигена D позволяет ответственному лицу станции переливания крови сделать заключение о D-отрицательности исследуемой крови (в процессе фенотипирования в эритроцитах донора идентифицированы также антигены с и е).Таким образом, фенотип донора ошибочноопределен как dce. Эритроциты фенотипированного донора используются для трансфузии резус-отрицательному (D-отрицательному) реципиенту с «аналогичным» фенотипом. D-положительные эритроциты донора (Dweak), поступая в кровоток D-отрицательного реципиента, распознаются В-лимфоцитами как чужеродные. Активированные В-лимфоциты трансформируются в плазматические клетки, которые начинают синтезировать и секретировать в кровь антитела, комплементарные антигену Dweak эритроцитов донора – анти-Dweak. В крови реципиента анти-Dweakсвязываютсяс антигенами Dweakмембраны эритроцитов донора. Образование комплекса«антиген-антитело» на поверхности эритроцитов резус-несовместимого донора активирует комплемент по классическому пути, в результате чего мембраноатакующий комплекс разрушает мембрану эритроцитов донора.
2. Другой случай. Допустим, производится трансфузия D-положительных эритроцитов донора D-положительному реципиенту с не идентифицированным фенотипом Dpartial. В состав антигена D донора входят все детерминантные группы антигена –множество различных эпитопов, Dpartial реципиента лишен некоторых из них. Детерминанты D-антигена донора, отсутствующие в структуре Dpartial реципиента, запускают иммунную реакцию, направленную на разрушение и элиминацию эритроцитов донора.
Заметим, что далеко не каждая резус-несовместимая, по идее, ситуация разрешается образованием антирезус антител. Около 30%D-отрицательных людей не подвергаются аллоиммунизации даже при переливании им больших объемов D-положительной крови. Это связано с индивидуальными особенностями иммунных реакций, возможностью возникновения толерантности к определенным антигенам.
Рецензенты:
Лебедева А.Ю., д.м.н., профессор кафедры госпитальной терапии №1 ГБОУ ВПО «Российский национальный исследовательский университет им. Н.И. Пирогова» МЗ РФ, г.Москва;
Автандилов А.Г., д.м.н., профессор, заведующий кафедрой терапии и подростковой медицины Российской медицинской академии последипломного образования (ГБОУ ДПО «РМАПО»), г. Москва.
[1]Реакцией конглютинации с 10%-ным желатином, непрямым антиглобулиновым тестом, гелевым тестом.


