В чем заключается механика автоматизма сердца: центры регуляции ритма
Имеется ряд функций сердечной мышцы, которые формируют ее работу. Среди этих функций выделяют автоматизм.
- Что такое автоматизм сердца?
- Центры автоматического регулирования сердца
- Сердечные гликозиды: химическая регуляция
Что такое автоматизм сердца?
Автоматизмом называют способность миокарда к ритмичным сокращениям, которые не вызваны иными возбуждениями. Он нужен для того, чтобы работа сердца была постоянной, не прерывалась.
Важно! В сердечной мышце имеется особые клетки, которые служат источником автоматизма в работе. Находятся в разных отделах.
При нормальном и здоровом функционировании центр автоматизма находится в правом предсердии. При автоматическом функционировании создаются слабые импульсы, которые проводятся по организму, доходя до конечностей. Эти возбуждения регистрируются при помощи электрокардиограммы. По данным электрокардиограммы можно оценить состояние пациента, функционирование миокарда.
Воздействие на функционирование кровяного «насоса» оказывает и центральная нервная система путем подачи возбуждений. Рецепторы, которые снимают показания давления в сердце, располагаются внутри камер и стенках больших кровеносных сосудов. Под влиянием возбудителей на «датчики» осуществляется рефлекторная обратная реакция на работу сердца.
Различают два вида рефлексии:
- уменьшающие частоту сердечных сокращений,
- увеличивающие частоту сердечных сокращений.
Влияющие на сердце сигналы идут от нервных центров в продолговатом и спинном мозге. Есть два вида нервов, каждый из которых отвечает за передачу определенного типа сигнала. Замедляющие работу миокарда сигналы идут по парасимпатическим нервам, ускоряющие – по симпатическим нервам.
К примеру: ускорение сердцебиения возникает при изменении положения тела в быстром темпе. При смене горизонтального положения накапливается кровь в нижних конечностях, что снижает кровенаполнение верхних конечностей, страдает головной мозг. Для восстановления нормального кровотока центральная нервная система отправляет сигнал об ускорении сердцебиения в ответ на сигнал, полученный от рецепторов.
Изменение деятельности сердца самостоятельно может осуществляться и под влиянием боли. При болевых раздражителях центральная нервная система может либо ускорить, либо замедлить работу сердечной мышцы.
Эмоциональный фон способен воздействовать на функционирование сердца. Под воздействием положительных эмоций возможности регулирования кровотока раскрываются. У спортсменов это можно пронаблюдать по рекордным показателям и победам. Если человек испытывает отрицательные эмоции, то миокард приобретает нарушения в функционировании.
Возможна гуморальная регуляция. Сердечная мышца регулируется под воздействием химических веществ, которые постоянно подаются в кровь.
Например: для замедления ЧСС используют ацетилхолин. Организм реагирует на вещество чувствительно, потому малейшая доза способна замедлить работу сердца.
Для ускорения ЧСС используют адреналин, дающий динамику повышения ритма в небольших дозах.
Центры автоматического регулирования сердца
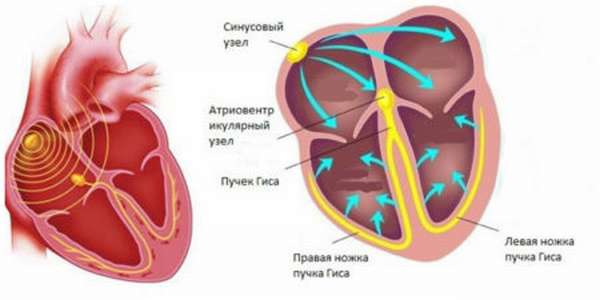
В сердце есть несколько центров, которые регулируют сократительный процесс в автоматическом режиме:
- Источник 1-го порядка. К нему относят синоатриальный узел, называемый водителем ритма и способный к выработке сигналов на сокращение частотой 65-85 в минуту.
- Источник 2-го порядка. Атриовентрикулярный узел и пучок Гиса образуют центр автоматизма, который стимулирует работу сердечной мышцы импульсами частотой 45-66 в минуту.
- Источник 3-го порядка. Клетки из нижней части пучка Гиса стимулируют сердечную деятельность импульсами частотой 25-45 в минуту.
При здоровой сердечной системе сионатриальный узел единственный водитель ритма, который подавляет автоматическую деятельность других водителей ритма.
Сердечные гликозиды: химическая регуляция
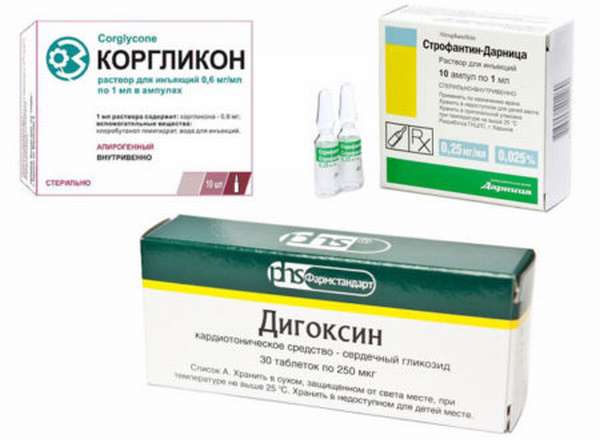
Сердечные гликозиды вещества, полученные из растений, которые оказывают избирательную стимуляцию. Среди растений подобным эффектом обладают следующие гликозиды:
- наперстянка,
- ландыш,
- весенний горицвет,
- строфант.
Название приобрели потому, что имеют в составе сахара.
Ценятся регуляторы, которые ускоряют ритм. Используют при сердечной недостаточности у пациента. Воздействуют на здоровое сердце незначительно.
Сердечные гликозиды оказывают благоприятное влияние на биохимические процессы: при увеличении ритм, потребление кислорода и глюкозы снижается. Стимуляция осуществляется из-за увеличения свободных ионов кальция. Данный фермент отвечает за создание импульсов.
Имеются гликозиды, которые оказывают обратную реакцию уменьшают ритм. При сердечной недостаточности возникает тахикардия, потому применение снижающих ритм гликозидов полезно.
Сердечные гликозиды способны ускорить или замедлить ЧСС. Ускорение выражается настолько, что даже при наличии брадикардии кровь нагнетается по кровеносным сосудам в увеличенном объеме. Гликозиды оказывают благоприятное влияние на перекачку крови. Под их воздействием перекачивается больше крови, обогащая кислородом органы.
Внимание! От гликозидов может образоваться частичный или полный блок для прохождения импульсов на сокращение через АВ-узел.
Увеличенный автоматизм сердца при помощи стимулирующих веществ может вызвать нарушение в виде внеочередных сокращений – экстрасистолы. При образовании частых экстрасистол функционирование сердца может серьезно нарушиться. Но есть и другая серьезная угроза, связанная с передозировкой стимулирующих веществ – фибрилляция предсердий.
В чем заключается механика автоматизма сердца: центры регуляции ритма
• В норме возбуждение генерируется в синусовом узле. Под действием этих импульсов сердце сокращается с частотой 60-80 в минуту.
• Возбуждение из синусового узла достигает сначала атриовентрикулярного (АВ) узла, затем, спустя непродолжительное время, распространяется по ПГ, его правой и левой ножкам, называемым также правой и левой ножками пучка Тавары, и далее по волокнам Пуркинье, вызывая сокращение миокарда желудочков сердца (систолу желудочков).
• Если генерация возбуждения в синусовом узле нарушается, электрический импульс может генерироваться в АВ-узле или на уровне желудочков. В этом случае сердце сокращается реже, с частотой примерно 40-20 в мин.
Миокард представлен двумя типами мышечной ткани. Один тип – рабочий миокард, другой – специализированный.
Рабочий миокард обеспечивает собственно сокращения сердца, его насосную функцию.
Функции специализированного миокарда:
• обеспечение ритмической автоматической генерации возбуждения (автоматизм);
• проведение этого возбуждения.
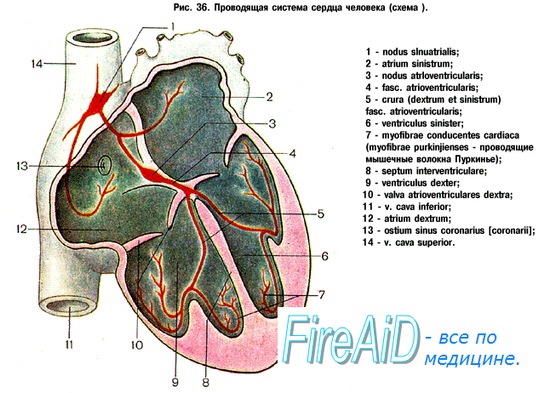
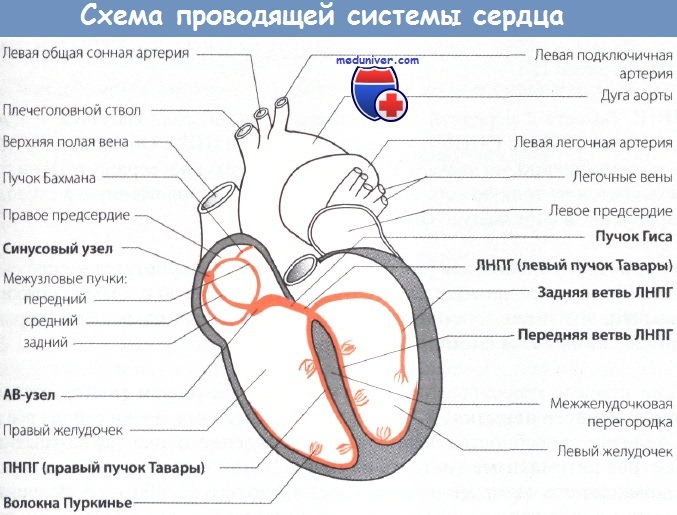
Специализированный миокард состоит из центра автоматизма, генерирующего возбуждение, и проводящей системы. В норме центром автоматизма является синусовый узел. Проводящая система охватывает предсердные проводящие пучки, АВ-узел, ПГ, правую и левую его ножки (или левый и правый пучки Тавары) и волокна Пуркинье.
1. Синусовый узел (узел Кис-Флака)
Синусовый узел располагается в стенке правого предсердия (ПП) между устьем верхней полой вены и ушком ПП, функционирует автономно и является центром автоматизма первого порядка. Возбуждение в норме генерируется в этом узле, и сердце здорового взрослого человека сокращается с частотой примерно 60-80 в минуту.
Возбуждение из синусового узла распространяется, с одной стороны, в левое предсердие (ЛП), с другой – по трем предсердным проводящим пучкам – в АВ-узел.
2. Атриовентрикулярный узел (узел Ашоффа-Тавары)
АВ-узлу присущи две важные функции. Одна из них состоит в задержке поступающего в него импульса возбуждения и дальнейшем проведении. Вторая функция заключается в генерировании возбуждения в случае, если функция автоматизма синусового узла оказывается по тем или иным причинам утраченной.
В этом случае АВ-узел выполняет роль центра автоматизма второго порядка, но сердце под влиянием генерируемых им импульсов сокращается с меньшей частотой, равной примерно 40-60 в минуту.
3. Пучок Гиса
Возбуждение из АВ-узла проводится в ПГ и далее в каудальном направлении. ПГ в норме является единственной мышечной структурой, которая связывает предсердия с желудочками.
Правая и левая ножки пучка Гиса. В стенке желудочков сердца проходят два проводящих пути – ЛНПГ и ПНПГ, или правый и левый пучки Тавары. Вскоре после начала ПГ от него отходит ЛН, которая в свою очередь разветвляется на переднюю и заднюю ветви, а затем ПН.
ЛНПГ (вместе с передней и задней его ветвями) располагается в левом желудочке (ЛЖ), а ПНПГ – в правом желудочке (ПЖ). Обе ножки ПГ следуют разобщенно, но вначале в направлении верхушки сердца, и затем разветвляются на тонкую сеть волокон Пуркинье, расположенную в субэндокардиальном слое желудочковой стенки.
В норме возбуждение, как уже говорилось ранее, генерируется в синусовом узле. Отсюда оно проводится в АВ-узел, ПГ, его левую и правую ножки и, наконец, достигает волокон Пуркинье. Это вызывает сокращение сердца, которое называется систолой.
Если процесс генерирования возбуждения в синусовом (центр автоматизма первого порядка) и АВ-узле нарушается, желудочки сердца все же сохраняют способность генерировать возбуждение за счет так называемых центров автоматизма третьего порядка. В этом случае желудочки сердца сокращаются с частотой, примерно равной только 20-40 в минуту.
Возникает опасность развития острой сердечной недостаточности, связанной с возможностью развития угрожающих жизни аритмий – желудочковой тахикардии, фибрилляции желудочков и асистолии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
В чем заключается механика автоматизма сердца: центры регуляции ритма
Различают функции автоматизма, возбудимости, проводимости, сократимости и тоничности. Среди них, пожалуй, трудно выделить главную. Все они играют колоссальную роль в работе сердца, тесно между собой взаимосвязаны и при нарушении одной из них изменяются другие функции.
Под функцией автоматизма понимают способность сердца безо всяких внешних воздействий выполнять ритмические, следующие одно за другим сокращения. Как отмечено выше, автоматическая функция сердца осуществляется проводниковой системой сердца. Обычно ритмом сердца управляет синусовый узел — автоматический центр первого порядка. При поражении синусового узла функция автоматизма исполняется атриовентрикулярным узлом — центром второго порядка. Если связь между предсердием и желудочками не нарушена, этот узел управляет ритмом всего сердца. Наконец, если поражены синусовый и атриовентрикулярный узлы, то функция автоматизма смещается к ножкам пучка Гиса, то есть к центрам третьего порядка.
Загадка функции автоматизма сердца до сих пор не раскрыта. По мнению некоторых исследователей, автоматизм сердца связан с синтезом ацетилхолина, потому что в венозном синусе ацетилхолина содержится значительно больше, чем в мышце предсердий или желудочков. Позже высказано предположение о существовании специфического гормона автоматизма. Е. И. Чазов и В. М. Боголюбов полагают, что объяснение функции автоматизма следует искать в особенностях изменения мембранного потенциала волокон проводящей системы сердца. Независимо от места нахождения они медленно деполяризуются в фазе диастолы, то есть потенциал покоя никогда не находится на постоянном уровне. Медленная деполяризация волокон приводящей системы сердца обусловлена более высоким содержанием в них натрия и более низким количеством калия, чем в волокнах предсердий и желудочков, не обладающих автоматической активностью.
Очевидно также, что автоматизм сердца вряд ли заключается в действии этих факторов, ибо взаимосвязи биоритмов в организме очень многогранны и сложны.

Сердцу, как и всякой живой структуре, присуща функция возбудимости, которая характеризуется возникновением потенциала действия и сокращения сердца. Возбудимостью обладают как клетки проводниковой системы, так и клетки сократительного миокарда.
Мышечная клетка сердца в невозбужденном состоянии имеет начальную разность потенциалов по обе стороны мембраны, которая определяется градиентами электролитов (потенциал покоя). Ее потенциал покоя колеблется в пределах 80—90 мВ.
При возбуждении мышечной клетки сердца образуется потенциал действия. Быстрый начальный подъем этого потенциала, обозначенный цифрой 0, соответствует деполяризации, когда электрический потенциал стремится к нулю. После наибольшего подъема потенциала развивается период реполяризации, когда восстанавливается потенциал покоя, в котором выделено три фазы реполяризации: 1 — быстрая, 2 — медленная (плато) и 3 — конечная фаза быстрой реполяризации. В начале и конце периода реполяризации внутренняя поверхность клетки становится положительно заряженной по отношению к наружной. Это изменение полярности, обычно величиной 15—20 мВ, называется реверсией, или превышением потенциала.
За период реполяризации следует диастолический период, в течение которого регистрируется трансмембранный потенциал покоя. Клеточная мембрана в покое почти непроницаема для ионов натрия вне клетки. Ионный механизм трансмембранного потенциала покоя обусловлен концентрационным градиентом калиевых ионов, то есть разницей концентраций ионов, обусловливающей отрицательное значение потенциала покоя.
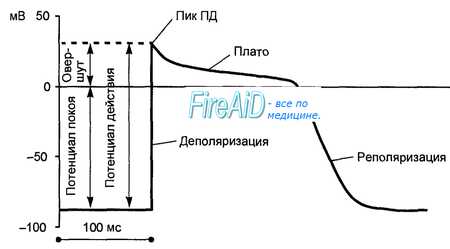 Потенциал действия клетки рабочего миокарда.
Потенциал действия клетки рабочего миокарда.
Быстрое развитие деполяризации и продолжительная реполяризация. Замедленная реполяризация (плато) переходит в быструю реполяризацию.
Молекулярные часы нашего сердца
- 3150
- 2,3
- 3
- 1
В каждой клетке сердца есть встроенные молекулярные часы, и чрезвычайно важно, чтобы ритм работы этих часов был синхронизирован с ритмом главных часов в головном мозге
Автор
 Полина Мирошникова
Полина Мирошникова
Редакторы
 Антон Чугунов
Антон Чугунов Андрей Панов
Андрей Панов
- «Био/мол/текст»-2014
- Медицина
- Процессы
Статья на конкурс «био/мол/текст»: Врачи уже давно заметили, что возникновение опасных для жизни обострений сердечно-сосудистых заболеваний, таких как инфаркт миокарда, инсульт, серьезные приступы аритмии, часто связано с определенным временем суток — намного чаще такие осложнения проявляются ранним утром. Заинтересовавшись этой особенностью, доктора провели многочисленные исследования и выяснили, что это явление тесно сопряжено с работой внутренних часов организма, и что при изучении сердечно-сосудистых заболеваний нужно обязательно уделять внимание особенностям регуляции суточных ритмов организма.

Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».

Главный спонсор конкурса — дальновидная компания «Генотек».
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Что такое циркадианный ритм
Мы живем в соответствии с ритмами природы: вслед за ночью неизбежно наступает день, тьму обязательно сменяет свет. И, чтобы приспособиться к этому регулярному, заданному внешней средой чередованию условий, наш организм выработал очень сложный и пока еще окончательно не разгаданный механизм внутренних часов — наш «встроенный хронометр», который физиологи называют суточным или циркадианным (циркадным) ритмом. Если дословно переводить с латинского, то «цирка» означает около, а диа — «день». То есть циркадианный ритм — это ритм с периодом около суток. Зачем же понадобилась эта приставка «около»? Дело в том, что время завершения полного цикла нашего «встроенного хронометра» все еще вызывает споры у ученых, так как внутренняя размеренность организма не вписывается точно в те 24 часа, которые составляют наши астрономические сутки.
В 1962 году физиолог-исследователь Ашофф в качестве эксперимента отправил своих сыновей в звуко- и светонепроницаемый бункер, где они жили, ориентируясь только на свои внутренние ритмы, а не на смену светлого дня и темной ночи. Это исследование показало, что внутренние хронометры регулярной изменчивости физиологических функций человека на самом деле настроены на ритм в 25 часов [1]. Но есть и другое мнение. Например, результаты эксперимента под руководством знаменитого спелеолога Мишеля Сифра продемонстрировали, что у участников, заточенных в пещеру на несколько месяцев, наблюдается постепенный переход с 24-часовых ритмов на 48-часовые: 36 часов человеку нужно было для бодрствования и 12 — для сна [2].
Но, так или иначе, не остается сомнений, что в нашем организме работают внутренние биологические часы, и работают они, как выявили генетические исследования последних лет, в каждой клеточке нашего тела. Генетическую природу биологических ритмов начали раскрывать с 1971 года, когда впервые в мире у мухи дрозофилы был найден часовой ген Per — его назвали сокращением от слова «период» (period) [3]. Было замечено, что мутация в этом гене вызывала у мушек отклонения в периодичности суточного ритма. Эти исследования положили начало целому ряду открытий, в результате которых сформировалось современное представление о молекулярном устройстве биологических часов.
Иерархия внутренних биологических часов
Итак, как же устроены наши внутренние часы? Последние исследования указывают на то, что внутренние задатчики ритма в нашем организме организованы по законам иерархии: здесь есть самые главные часы и подчиненные часики. Главным центром циркадианных часов является супрахиазматическое ядро в головном мозге — это плотное скопление из примерно 20 тысяч нейронов, и расположено оно как раз рядом с центром, регулирующем продукцию гормонов в организме. Что касается подчиненных часиков, то, как показал анализ экспрессии генов в клетках внутренних органов, гены, отвечающие за суточные ритмы, экспрессируются в каждой клетке организма, включая даже соединительную ткань. Это навело ученых на мысль, что каждый орган имеет свои внутренние часы. Собственную часовую систему внутренних органов назвали периферическими часами, а управляющее ими супрахиазматическое ядро — центральными часами (рис. 1). Свой собственный хронометр есть у печени, у кровеносных сосудов, у сердца, у почек. Но для эффективной работы организма чрезвычайно важно, чтобы все часовые механизмы были настроены на слаженную работу в одном ритме — синхронизированы.
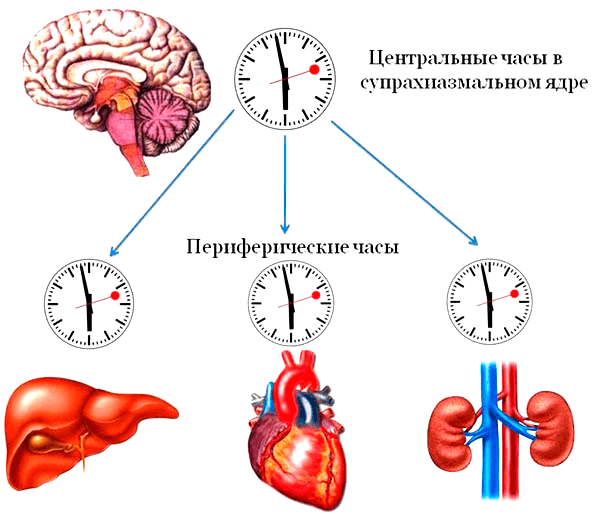
Рисунок 1. Иерархия внутренних биологических часов: главным центром циркадианных часов является супрахиазматическое ядро в головном мозге, задающее ритм работы всем клеткам организма посредством вегетативной нервной системы, специализированных гормонов и различных факторов. Подчиненные часы в клетках внутренних органов называются периферическими.
Фазы внутренних хронометров могут сдвигаться под воздействием определенных стимулов, которые способны навязывать свой ритм. Такие стимулы называются цайтгеберами (от нем. Zeit — «время» и geben — «давать») или задатчиками ритма. Каждые часы способны реагировать на свои специфические задатчики ритма. Например, свет задает ритм центральным часам в супрахиазматическом ядре, тогда как непосредственно на периферические часы он не влияет. Цайтгеберами могут быть не только внешние воздействия, но и особенности поведения: режим физической активности, цикл смены сна и бодрствования и даже режим питания. Например, четко было показано, что внутренние часы печени больше настроены на ритмичность приема пищи, чем на ритмы смены светлого и темного периодов суток [4].
Главный физиологический синхронизатор всех периферических часов — супрахиазматическое ядро. Благодаря своим связям со светочувствительными клетками сетчатки глаза, нейроны супрахиазматического ядра способны получать информацию о световом периоде снаружи и подстроить к внешним условиям внутренние ритмы организма. Синхронизация периферических часовых систем осуществляется посредством вегетативной нервной системы специальными гормонами и, возможно, другими, пока еще мало изученными путями. Ученые с каждым годом открывают и подробно описывают все больше новых факторов, влияющих на регуляцию внутренних ритмов [5].
Потеря синхронизации и прогрессирование болезни
Как показывают эксперименты, синхронизация всех внутренних ритмов — крайне важное условие для сохранения здоровья и продолжительности жизни. Когда ученые изучают взаимосвязь между сбоем биологических часов и сердечными заболеваниями, то у них возникает очевидный вопрос, что же первично: поломки во внутренних часах вызывают болезни сердца, или сама сердечная патология является причиной нарушения работы наших встроенных хронометров? В попытке ответить на этот вопрос выдвинуто как минимум две противоположные гипотезы.
В пользу гипотезы о том, что потеря синхронизации внутренних ритмов в возникновении болезни первична, был проведен целый ряд интереснейших экспериментов. Исследователь Тами Мартино анализировал продолжительность жизни золотистых хомячков с особой мутацией в гене tau, которая уменьшает период суточного ритма в периферических часах до 22 часов (рис. 2). Иными словами, внутренние часы у этой линии щекастых грызунов очень спешат. Оказалось, что и общая продолжительность жизни хомячков с мутацией уменьшается на 20%, а умирают они в раннем возрасте от серьезных заболеваний миокарда — фиброза и кардиомиопатий [6].

Рисунок 2. Золотистый хомячок с мутацией в гене tau: внутренние часы хомячка спешат на два часа в сутки. Отсутствие синхронизации внутреннего и внешнего ритмов привело к тому, что у грызуна возникли серьезные проблемы со здоровьем — гипертрофия миокарда.
Однако, когда таким хомячкам создали искусственные условия так, чтобы период чередования света и темноты составлял 22 часа, то сердечная патология сменилась на нормальное функционирование сердца. Более того, удаление супрахиазматического ядра — главных часов организма — также имело профилактический эффект: гипертрофия миокарда у золотистых хомячков после операции не развивалась. В чем же причина такого чудесного исцеления?
Полученные результаты свидетельствуют о том, что не столько повреждение периферических часов, сколько утрата синхронизации между центральными и периферическими задатчиками ритма приводит к возникновению сердечно-сосудистой патологии. У мутантных хомячков произошла нестыковка 22-часового периода периферических часов и 24-часового периода центральных часов. Когда центральному хронометру через изменения внешних условий (свет/темнота) навязали ритм в 22 часа, то он синхронизировался с периферическими часиками, и сердечная патология не развилась. А когда супрахиазмальное ядро удалили, то периферическим часам снова ничто не мешало свободно реализовывать свой собственный ритм, и сердечко хомяка опять же было спасено.
С другой стороны, и сама болезнь способна нарушить слаженность внутренних биоритмов. Например, во время острого инфаркта миокарда в поврежденных клетках происходит сдвиг фаз циркадианных часов по отношению к здоровым тканям. Эта потеря синхронизации очень опасна и может вызвать угрожающие жизни приступы аритмии.
Восстановление слаженности ритмов клеток сердца с естественными циклами остальных органов и тканей и с циклическими сменами условий окружающей среды может стать многообещающей стратегией в борьбе с сердечно-сосудистыми заболеваниями. Но для реализации этого направления необходимы очень глубокие знания о закономерностях функционирования биоритмов. Интересно, что даже у здоровых людей циркадианный ритм клеток внутренней оболочки вен варьирует в зависимости от их анатомического положения. Необходимы дальнейшие исследования, чтобы как можно точнее идентифицировать все цайтгеберы в организме, и использовать полученные знания для починки наших встроенных хронометров в случае сбоя.
Суточная вариабельность сердечно-сосудистых показателей
Еще один очень важный момент заключается в том, что в течение суток чувствительность сердца к стрессу, эмоциональным и физическим нагрузкам различна. Также меняются во времени и сами показатели сердечно-сосудистой функции: артериальное давление, скорость кровотока, частота сердечных сокращений и другие. Непрерывная запись электрокардиограммы в течение 24 часов у людей в состоянии покоя показывает, что частота сердечных сокращений у человека постоянно варьирует: она достигает минимума на пятом-шестом часу сна и в это время составляет 48–50 ударов в минуту. Максимума она достигает вечером, примерно в 18 часов, а затем снова постепенно начинает снижаться.
Все эти явления возможны благодаря сложным молекулярным механизмам собственных периферических часов в сердечно-сосудистой системе. Около 10% генов, экспрессирующихся в клетках сердца, имеют суточный ритм экспрессии. В настоящее время проводится активный поиск факторов, влияющих на работу сердца и обладающих суточной ритмичностью. Молекулярные часы уже обнаружены в мышечных клетках сердца, в клетках внутренней выстилки сосудов (в эндотелии) и в мышечных клетках сосудов.
Молекулярные часы в мышечных клетках сердца
Недавно ученые опубликовали в журнале Nature сообщение о том, что белок Klf 15 (kruppel-like factor), контролирующий в организме процессы формирования тканей, обмена жиров и воспаления, способен влиять и на суточные ритмы сердца. Концентрация этого белка варьирует в зависимости от стадии цикла «сон—бодрствование». Исследователями были выведены линии мышей с двумя вариантами мутаций в гене, кодирующем Klf 15, которые приводили к тому, что уровень фактора в плазме крови был либо чрезмерно повышен, либо белок отсутствовал вовсе. И в том, и в другом случае мышки страдали от угрожающих жизни сердечных аритмий [7].
При более глубоком изучении оказалось, что Klf 15 — это только первая ступень в сложном молекулярном каскаде, потому что он контролирует другой белок — KСhIP 2 (Kv channel-interacting protein) — фактор, взаимодействующий с калиевыми каналами в мышечных клетках сердца. Изменения концентрации KChIP 2 приводят к электрической нестабильности тканей сердца и, как следствие, к нарушениям сердечного ритма; при этом ген этого фактора имеет суточный ритм экспрессии.
Суточный ритм экспрессии имеют и сами гены калиевых каналов мышечных клеток сердца Kv1.5 и Kv4.2. Интересно, что экспрессия Kv1.5 увеличивается в темное время суток, тогда как матричную РНК белка Kv4.2 в большей концентрации обнаруживают в светлый период. Нарушения ритма в любом звене этой сложной системы могут быть связаны с суточным временем возникновения приступов аритмии.
Синхронизация молекулярных часов мышечных клеток сердца с обменом липидов
Мы уже говорили о том, как важна синхронизация ритмов сердца с циклами других физиологических систем организма. Не менее важно отметить, что некоторые внутренние циклы способны навязывать свой ритм сердечным часам. Одним из таких циклов-задатчиков является суточный ритм циркуляции жирных кислот и уровня липидов, жестко связанный с циркадианным. Жирные кислоты — преимущественное «сердечное топливо»: они на 70% утилизируются сердцем. При избытке жирных кислот сократительная функция сердца подавляется, и сердце отвечает на эти изменения внутренней среды активацией как оксидативного (митохондриального), так и неоксидативного метаболизма. Таким образом сердце уменьшает клеточную токсичность, вызванную нагрузкой жирными кислотами. И этот процесс также связан с суточными ритмами экспрессии генов.
Американская исследовательница Молли Брэй исследовала гены циркадианных часов с помощью метода микрочипов ДНК. Ей удалось выявить 548 генов, регулирующих часы в кардиомиоцитах предсердия, и 176 генов, связанных с циркадианным ритмом мышечных клеток желудочка сердца. Среди них были гены, вовлеченные в липогенез, и белки, связывающие липиды; все они демонстрировали суточную экспрессию [8].
Периферические часы в клетках эндотелия
Несколько групп ученых продемонстрировали роль часовых генов в функции эндотелия — ткани, выстилающей внутреннюю поверхность кровеносных сосудов и сердца. Они выяснили, что у мышей с мутацией в часовом гене Per 2 не расслабляются сосуды в ответ на воздействие главного релаксирующего нейромедитора — ацетилхолина. Кроме этого очень неприятного нарушения функции, в крови мышек выявляется очень высокая концентрация веществ, стимулирующих сжатие сосудов, что чревато возникновением артериальной гипертонии [9].
Но на этом проблемы со здоровьем у несчастных мышек не заканчивались. Исследователь Чао Ванг показал, что если в клетках эндотелия есть мутация гена Per 2, то кровеносные сосуды быстро стареют, плохо восстанавливаются после повреждений, а у самих грызунов сильно уменьшается продолжительность жизни [10].
Периферические часы в мышечных клетках сосудов
Клетки гладкой мускулатуры кровеносных сосудов — миоциты — также имеют собственные периферические часы. Такишиге Куньеда исследовал циркадианную систему в миоцитах стареющих сосудов. Он обнаружил, что в этих клетках потеря циркадной ритмичности связана с укорочением теломер. Введение теломераз предотвращало проблемы с экспрессией часовых генов. Эти исследования показывают, что регуляция теломеразами может стать одним из способов терапии нарушений циркадных ритмов, связанных с возрастом [11].
Заключение
Таким образом, изучение биоритмов, особенно с позиции их синхронизации с циклами внутренней и внешней среды, поможет пролить свет не только на причины сердечно-сосудистой патологии, но и на причины старения и низкой продолжительности жизни.
Жизнь современного человека наполнена событиями, которые не подчиняются естественным циклам природы: мы можем работать в ночную смену или регулярно не спать по ночам, засиживаясь за телевизором, компьютером или чтением книг, у нас есть возможность за один день пересечь сразу несколько часовых поясов. Только все ли из нас задумывались, какие серьезные физиологические перестройки происходят в это время в нашем организме? В статье мы рассмотрели несколько примеров работы внутренних молекулярных часов, связанных с функционированием сердца, и увидели, что внутренние и внешние ритмы взаимосвязаны очень тесно, и нарушение временнóй слаженности в одной системе может повлечь за собой сбои в другой. Исследования в этой области продолжаются и, возможно, когда-нибудь ученые откроют волшебное средство, приняв которое, мы мгновенно синхронизируем работу всех внутренних органов, замедлим старение и будем чувствовать себя бодрыми и веселыми независимо от времени суток. Но пока это средство остается в мечтах, мы должны понимать, что сами можем организовать свою жизнь так, чтобы в наших молекулярных часах было как можно меньше сбоев. Соблюдение регулярности в режимах приема пищи, сна и бодрствования, физической активности, полноценный ночной сон, осторожное отношение к перелетам с пересечением часовых поясов — все это может стать той самой волшебной пилюлей, которая починит молекулярные часы в нашем сердце.
ЭКГ-диагностика нарушений функции автоматизма синусового узла, замещающих комплексов и ритмов
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
Несмотря на все разнообразие использующихся методов функциональной диагностики, в практике врача-кардиолога свою прочную позицию занимает электрокардиография как «золотой стандарт» диагностики нарушений сердечного ритма и проводимости.
Электрокардиография позволяет диагностировать и выявлять блокады и аритмии сердца, гипертрофию различных отделов сердца, определять признаки ишемического повреждения миокарда, а также косвенно судить об электролитных нарушениях, воздействии различных лекарственных препаратов, экстракардиальных заболеваниях. Некоторые электрокардиографические признаки в совокупности с характерными клиническими проявлениями объединены в клинико-электрокардиографические синдромы, которых в настоящее время насчитывается более 40 видов.
Данный обзор посвящен наиболее сложному разделу ЭКГ-диагностики – аритмиям сердца. Многообразие нарушений сердечного ритма, в т. ч. обусловленных дисфункцией синусового узла, значительно затрудняет их диагностику. Тем не менее актуальность адекватной оценки нарушений функции автоматизма синусового узла не вызывает сомнений.
В обзоре представлены современные взгляды на ЭКГ-диагностику нарушений функции автоматизма синусового узла. Дана характеристика основных причин нарушений сердечного ритма, представлены иллюстрированные электрокардиограммами критерии диагностики нарушений функции автоматизма синусового узла. В статье приведена современная классификация нарушений сердечного ритма и проводимости, а также даны алгоритмы дифференциального диагноза между различными аритмиями сердца.
Ключевые слова: автоматизм сердца, синусовый узел, синусовый ритм, выскакивающие сокращения, блуждающий ритм, замещающие ритмы, медленный предсердный ритм, узловой ритм, идиовентрикулярный ритм, синдром слабости синусового узла, блокады сердца, остановка синусового узла, асистолия предсердий.
Для цитирования: Задионченко В.С., Ялымов А.А., Шехян Г.Г., Щикота А.М. ЭКГ-диагностика нарушений функции автоматизма синусового узла, замещающих комплексов и ритмов // РМЖ. Кардиология. 2016. № 9. С. –539.
Для цитирования: Задионченко В.С., Ялымов А.А., Шехян Г.Г., Щикота А.М. ЭКГ-диагностика нарушений функции автоматизма синусового узла, замещающих комплексов и ритмов. РМЖ. 2016;9:530-539.
ECG diagnosis of sinus node automaticity dysfunctions, substituting complexes and rhythms
V.S. Zadionchenko, A.A. Yalymov, G.G. Shekhyan, A.M. Shchikota
A.I. Evdokimov Moscow State Medical and Dental University, Moscow, Russia
Despite a variety of functional tests used by cardiologists, electrocardiography (ECG) remains the gold standard for the diagnosis of heart rhythm and conduction disorders. Currently, electrocardiography can be done almost everywhere, however, ECG interpretation by an expert is performed rarely. ECG helps to diagnose cardiac hypertrophy, heart block and arrhythmias, myocardial ischemic injury as well as to identify extracardiac pathologies, electrolyte imbalances, and the effects of various drugs. Electrocardiographic signs and typical clinical symptoms can be grouped into more than 40 clinical electrocardiographic syndromes. Long QT syndrome, post-tachycardia syndrome, Frederick syndrome, and Wolff-Parkinson-White syndrome are the best known conditions. The paper discusses the most difficult part of ECG diagnostics, i.e., heart arrhythmias. A variety of heart rhythm problems (including arrhythmias caused by sinus dysfunction) make their diagnosis difficult. Nevertheless, adequate interpretation of sinus node automaticity dysfunction is an important issue. The paper summarizes recent opinion on electrocardiographic diagnostics of this pathology. Major causes of heart rhythm problems are described. Diagnostic criteria sinus node automaticity dysfunction are illustrated by ECGs. Finally, current grading system of heart rhythm and conduction disorders as well as algorithms for the differential diagnosis of arrhythmias are reviewed.
Key words: heart automaticity, sinus node, sinus rhythm, escape beat, wandering pacemaker, substituting rhythms, slow atrial rhythm, junctional rhythm, idioventricular rhythm, sick sinus syndrome, heart block, sinus arrest, atrial asystole.
For citation: Zadionchenko V.S., YalymovA.A., Shekhyan G.G., Shchikota A.M. ECG diagnosis of sinus node automaticity dysfunctions, substituting complexes and rhythms // RMJ. Cardiology. 2016. № 9. P. –539.
Статья посвящена ЭКГ-диагностике нарушений функции автоматизма синусового узла, замещающих комплексов и ритмов
Синусовый узел (синоаурикулярный узел, узел Киса – Флака) (СУ) является нормальным водителем ритма сердца. Пейсмейкерные клетки СУ (водителя ритма первого порядка) обладают наибольшим автоматизмом, они генерируют 60–90 импульсов в минуту.
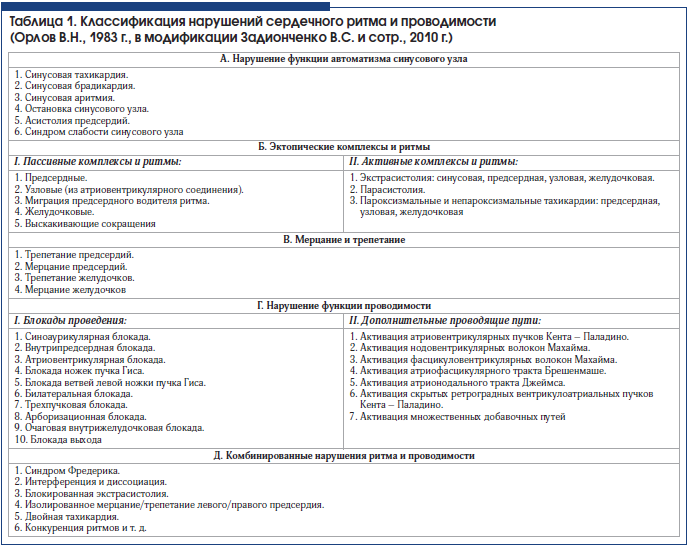
Нарушения функции автоматизма СУ можно подразделить на виды, имеющие и не имеющие гемодинамическую значимость, что, в свою очередь, делает крайне актуальной своевременную и правильную их диагностику, что позволяет назначить адекватную терапию, избежать (в т. ч. и ятрогенных) ошибок в процессе лечения, проводить профилактику развития внезапной смерти и других осложнений. В таблице 1 представлена классификация нарушений ритма и проводимости [1–5].
По этиологии нарушения ритма сердца можно разделить на следующие основные виды:
1. Дисрегуляторные или функциональные: связанные с нарушениями нейроэндокринной регуляции, вегетативной дисфункцией, психогенными воздействиями, переутомлением, рефлекторными влияниями (гастрит, язвенная болезнь, аэрофагия, синдром Ремхельда, желчнокаменная болезнь, нефроптоз, мочекаменная болезнь, колит, запор, метеоризм, панкреатит, межпозвоночная грыжа, эмболия в систему легочной артерии, опухоли средостения, бронхолегочные процессы, плевральные спайки, грудные операции, заболевания половых органов, травмы черепа, опухоли мозга, рассеянный склероз).
2. Миогенные или органические: связанные с болезнями миокарда (кардиомиопатия, миокардит, постмиокардитический кардиосклероз, дистрофия миокарда), с повреждениями кардиомиоцитов, возникающими на фоне ишемической болезни сердца (инфаркт миокарда, ишемическая кардиомиопатия), гипертонической болезни, пороков сердца.
3. Токсические: возникающие под воздействием лекарственных препаратов (сердечные гликозиды, анестетики, транквилизаторы, антидепрессанты, нейролептики, эуфиллин и его аналоги, адреномиметики (адреналин, нор-адреналин, мезатон, добутамин, дофамин, сальбутамол), ацетилхолин, ваголитики (атропин), глюкокортикостероиды, АКТГ, антиаритмические препараты, цитостатики, противовирусные препараты, противогрибковые препараты, антибиотики, диуретики, эфир, алкоголь, кофеин, никотин, соли тяжелых металлов, бензолы, угарный газ, отравление грибами, инфекции, эндогенная интоксикация при онкопатологии, уремия, желтуха и т. д.
4. Электролитные: гипокалиемия, гиперкалиемия, гипокальциемия, гиперкальциемия, гипомагнезиемия.
5. Дисгормональные: тиреотоксикоз, гипотиреоз, феохромоцитома, пубертатный возраст, климакс, беременность, гипопитуитаризм, дисфункция яичников, предменструальный синдром, тетания.
6. Врожденные: врожденные нарушения атриовентрикулярного (АВ) проведения, синдром удлиненного QT, синдромы предвозбуждения желудочков (WPW, CLC и др.).
7. Механические: катетеризация сердца, ангиография, операции на сердце, травмы сердца.
8. Идиопатические.
ЭКГ-диагностика аритмий, обусловленных нарушением функции автоматизма синусового узла, осуществляется с помощью электрокардиографического исследования, которое позволяет выделить следующие основные их типы [1, 2, 4–16].
1. Синусовая тахикардия – это правильный ритм с неизмененными зубцами ЭКГ (зубец Р, интервал PQ, комплекс QRS и зубец T не отличаются от нормы) из синусового узла с частотой > 90 в 1 мин. Синусовая тахикардия в состоянии покоя редко превышает 150–160 сокращений в 1 мин (рис. 1) [1, 16].

Дифференциальный диагноз:
– суправентрикулярная непароксизмальная тахикардия;
– суправентрикулярная пароксизмальная тахикардия;
– трепетание предсердий 2:1;
– мерцание предсердий с тахисистолией желудочков;
– желудочковая пароксизмальная тахикардия.
Этиология:
– физиологическая тахикардия: физическая нагрузка, эмоции, страх, ортостатическая, врожденные особенности;
– неврогенная тахикардия: невроз, нейроциркуляторная астения;
– ССЗ: воспалительные и дегенеративные заболевания миокарда, пороки клапанов, коллапс, сердечная недостаточность, легочное сердце, инфаркт миокарда, артериальная гипертензия;
– медикаментозная и токсическая тахикардия: ваголитики (атропин), симпатикотоники (адреналин, норадреналин, мезатон, добутамин, дофамин), эуфиллин, кортикостероиды, АКТГ, кофеин, кофе, чай, алкоголь, никотин;
– инфекционные заболевания: ОРВИ, сепсис, пневмония, туберкулез и т. д.;
– прочее: кровопотеря, анемия.
2. Синусовая брадикардия – замедление синусового ритма с ЧСС 2,5 с, возникающие вследствие остановки СУ, СА-блокады либо редких замещающих ритмов (рис. 6);
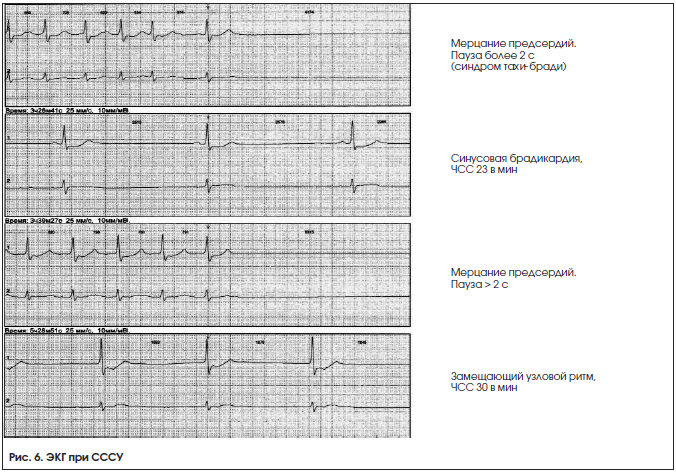
– синдром тахи-бради, чередование периодов тахикардии и брадикардии (рис. 6);
– редко приступы желудочковой тахикардии и/или мерцания желудочков;
– медленное и нестойкое восстановление функции СУ после экстрасистол, пароксизмов тахикардии и фибрилляции, а также в момент прекращения стимуляции при электрофизиологическом исследовании сердца (посттахикардиальная пауза, не превышающая в норме 1,5 с, при СССУ может достигать 4–5 с);
– неадекватное урежение ритма при использовании даже небольших доз бета-блокаторов. Сохранение брадикардии при введении атропина и проведении пробы с физической нагрузкой.
Классификация
Единой классификации СССУ не существует. В зависимости от характера поражения выделяют истинный (органический), регуляторный (вагусный), лекарственный (токсический) и идиопатический СССУ (рис. 6).
По клиническим проявлениям выделяют:
– латентный СССУ: изменений на ЭКГ нет, а патология СУ выявляется дополнительными функциональными методами исследования (ЭФИ);
– компенсированный СССУ: клинические изменения отсутствуют, есть изменения на ЭКГ;
– декомпенсированный СССУ: есть клинические и ЭКГ-проявления заболевания.
По ЭКГ-признакам выделяют:
– брадиаритмический вариант СССУ.
– синдром тахикардии-брадикардии.
Этиология:
– ССЗ: ИБС, миокардит, кардиомиопатии, оперативное повреждение СУ, ревматизм, врожденные пороки;
– рефлекторная: чувствительный каротидный синус, вагусные пробы, рефлекторные влияния при язвенной болезни, желчнокаменной болезни, грыже пищеводного отверстия диафрагмы;
– медикаментозная и токсическая: сердечные гликозиды (дигоксин, строфантин), опиаты, ацетилхолин, хинидин, бета-блокаторы, антагонисты кальция. Гиперкалиемия, интоксикация, гипоксемия;
– идиопатические формы.
Пассивные эктопические комплексы и ритмы
Пониженная активность СУ или полная блокада синусовых импульсов вследствие функционального или органического повреждения СУ вызывает включение в действие автоматических центров II порядка (клетки водителей ритма предсердий, АВ соединение), III порядка (система Гиса) и IV порядка (волокна Пуркинье, мускулатура желудочков).
Автоматические центры II порядка вызывают неизмененные желудочковые комплексы (наджелудочковый тип), тогда как центры III и IV порядка генерируют расширенные и деформированные желудочковые комплексы (желудочкового, идиовентрикулярного типа). Замещающий характер имеют следующие нарушения ритма: предсердные, узловые, миграция водителя ритма по предсердиям, желудочковые (идиовентрикулярный ритм), выскакивающие сокращения [1, 5, 16].
7. Предсердный ритм (медленный предсердный ритм) – очень медленный эктопический ритм с очагами генерирования импульсов в предсердиях (табл. 2).
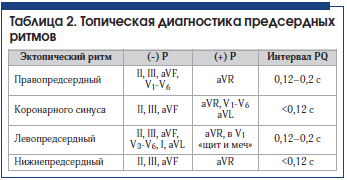
Правопредсердный эктопический ритм – ритм эктопического очага, расположенного в правом предсердии. На ЭКГ регистрируется отрицательный зубец Р в V1-V6, II, III, aVF отведениях. Интервал PQ – обычной продолжительности, комплекс QRST не изменен.
Ритм коронарного синуса (ритм венечной пазухи) – импульсы для возбуждения сердца исходят из клеток, расположенных в нижней части правого предсердия и коронарной синусной вены. Импульс распространяется по предсердиям ретроградно снизу вверх. Это приводит к регистрации отрицательных зубцов P во II, III, aVF отведениях. Зубец РaVR положительный. В отведениях V1-V6 зубец Р положительный либо 2-фазный. Интервал PQ укорочен и обычно 100 (101–120) в 1 мин. Ритм правильный, комплекс QRS не изменен (рис. 7).
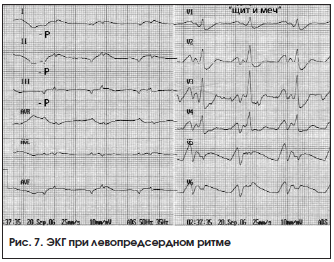
Регулярный ритм с отрицательным зубцом P I, II, III, aVF, V3-V6 перед комплексом QRS. Зубец Р в отведении V1 с начальной округлой куполообразной частью, за которой следует заостренный пик – «щит и меч». Нормальный интервал P-R=0,12-0,2 с.
Нижнепредсердный эктопический ритм – ритм эктопического очага, расположенного в нижних отделах правого либо левого предсердий. Это приводит к регистрации отрицательных зубцов P во II, III, aVF отведениях и положительного зубца Р в aVR. Интервал PQ – укорочен (рис. 8).
Дифференциальный диагноз:
– синусовая аритмия;
– узловой ритм;
– миграция водителя ритма по предсердиям;
– трепетание предсердий;
– политопная предсердная экстрасистолия;
– предсердные ритмы (правопредсердный, левопредсердный, нижнепредсердный, ритм коронарного синуса).
8. Узловой ритм (АВ-ритм, замещающий АВ узловой ритм) – сердечный ритм под действием импульсов из АВ-соединения с частотой 40–60 в 1 мин. Различают 2 основных типа АВ-ритма [1]:
– узловой ритм с одновременным возбуждением предсердий и желудочков (узловой ритм без зубца P, узловой ритм с АВ-диссоциацией без зубца P): на ЭКГ регистрируется неизмененный либо незначительно деформированный комплекс QRST, зубец Р отсутствует (рис. 9);
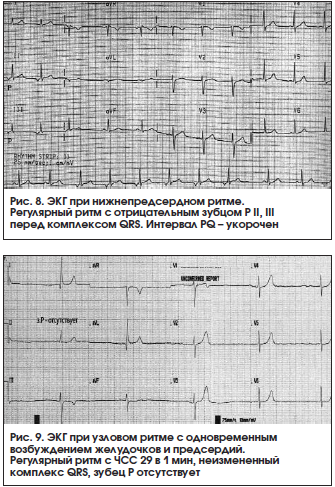
– узловой ритм с разновременным возбуждением желудочков, а затем предсердий (узловой ритм с ретроградным зубцом Р, изолированная форма АВ-ритма): на ЭКГ регистрируется неизмененный комплекс QRST, за которым следует отрицательный зубец P (рис. 10).
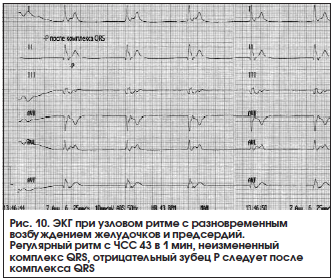
Дифференциальный диагноз:
– синусовая брадикардия;
– предсердный ритм;
– миграция водителя ритма по предсердиям;
– политопная предсердная экстрасистолия;
– идиовентрикулярный ритм.
9. Миграция водителя ритма по предсердиям (блуждающий ритм, скользящий ритм, мигрирующий ритм, миграция водителя сердечного ритма, wandering pacemaker). Различают несколько вариантов блуждающего (странствующего) ритма [1, 5,15]:
Блуждающий ритм в СУ. Зубец Р имеет синусовое происхождение (положительный во II, III, аVF), но его форма изменяется при различных сердечных сокращениях. Интервал P-R остается относительно постоянным. Всегда налицо выраженная синусовая аритмия.
Блуждающий ритм в предсердиях. Зубец Р положительный во II, III, аVF, форма и размер его изменяются при различных сердечных сокращениях. Наряду с этим изменяется продолжительность интервала P-R.
Блуждающий ритм между синусовым и атриовентрикулярными узлами. Это наиболее частый вариант блуждающего ритма. При нем сердце сокращается под влиянием импульсов, периодически меняющих свое место: постепенно перемещаются от СУ, предсердной мускулатуры до АВ-соединения и снова возвращаются в СУ. ЭКГ критерии миграции водителя ритма по предсердиям – это ≥ 3 различных зубцов Р на серии сердечных циклов, изменение продолжительности интервала P-R. Комплекс QRS не изменяется (рис. 11, 12).
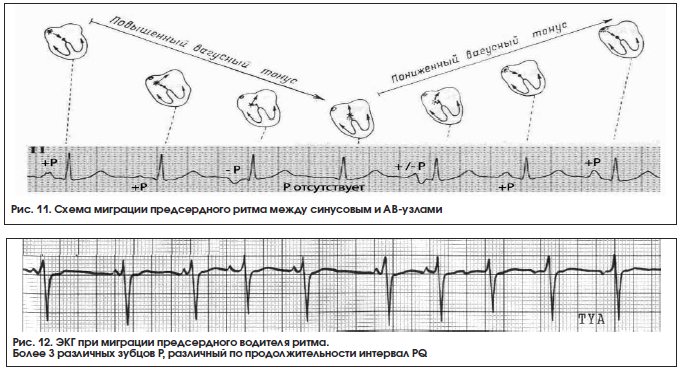
Этиология:
– рефлекторная: здоровые люди с ваготонией, чувствительный каротидный синус, вагусные пробы, интубация, глубокое дыхание;
– медикаментозные и токсические воздействия: сердечные гликозиды (дигоксин, строфантин), хинидин. Инфекционные заболевания, интоксикация;
– ССЗ: ИБС, ревматизм, пороки сердца, операции на сердце.
Дифференциальный диагноз:
– СА-блокада II ст., отказ СУ;
– АВ-блокада II ст.;
– мерцание предсердий;
– синусовая аритмия;
– политопная предсердная экстрасистолия.
10. Идиовентрикулярный (желудочковый) ритм (собственный желудочковый ритм, желудочковый автоматизм, внутрижелудочковый ритм) – импульсы сокращения желудочков возникают в самих желудочках. ЭКГ-критерии: уширенный и деформированный комплекс QRS (>0,12 с), ритм с ЧСС Литература
Нарушения ритма сердца (аритмии)

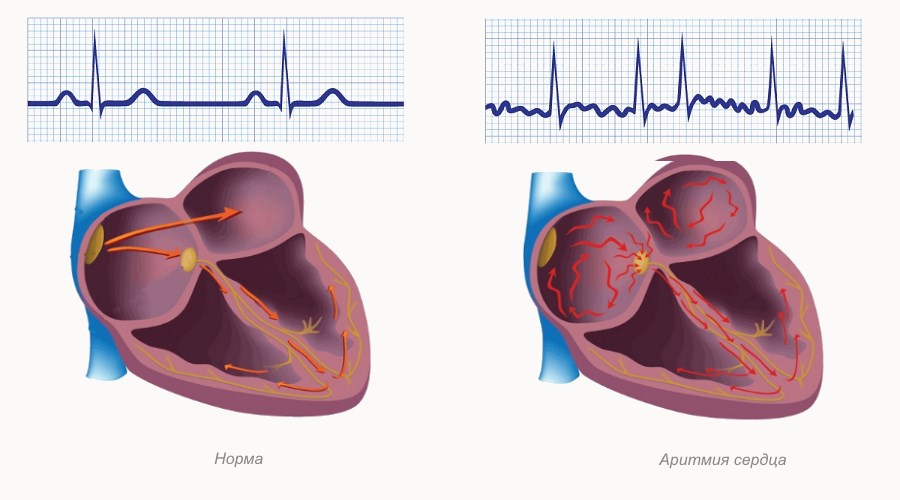
Сердце – необычайно сложно работающий орган. Его задача – собрать кровь, притекающую к сердцу по венам и выбросить эту кровь в артерии так, чтобы все клетки организма получили свою долю питательных веществ и кислорода. Реагируя на увеличение потребности какого либо органа или всего организма в питании, оно увеличивает выброс крови в артерии.
Сердце состоит из четырех камер – двух предсердий и двух желудочков. В здоровом сердце вначале сокращаются предсердия, выбрасывая кровь, поступившую в них из вен. Кровь попадает в желудочки сердца. Сокращение желудочков (систола) выбрасывает кровь в артерии.
В правое предсердие кровь собирается из вен всего организма, затем она попадает в правый желудочек, оттуда выбрасывается в артерии легких. В легких кровь обогащается кислородом, отдает углекислый газ и собирается в легочные вены. Оттуда кровь попадает в левой предсердие, затем в левый желудочек, из него – в артерии организма.
Согласованность работы сердца обеспечивается специальной проводящей системой сердца. Это специализированные клетки, которые вырабатывают и проводят электрические импульсы, руководящие согласованным сокращением мышцы сердца.
Импульс, запускающий сокращение сердца, вырабатывается в правом предсердии, в так называемом синусовом узле (водителе ритма). Именно этот узел ответственен за то, что сердце сокращается с частотой 60-90 ударов в минуту. Затем сигнал распространяется на остальные предсердия, вызывая их сокращение, потом на желудочки.
Нарушения в этой системе и приводят к нарушениям ритма сердца (аритмиям).
Какие бывают аритмии
Сокращения сердца следуют друг за другом через равные промежутки времени.. Если такая последовательность нарушена, говорят, что у больного аритмия. В зависимости от того, в каком месте возникают нарушения, все аритмии делят на предсердные (или суправентрикулярные) и желудочковые.
Аритмия – не самостоятельное заболевание, а признак (симптом) какой-либо болезни. Поэтому, возникновение аритмии требует обязательного обследования у специалиста кардиолога.
Наличие аритмии пациент может обнаружить у себя сам. Для этого, надо научиться находить и считать пульс.
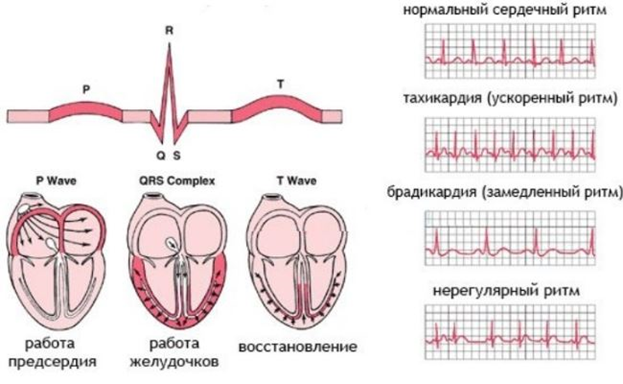
Работа сердца (ритмы)
Если частота пульса превышает 90 ударов в минуту, говорят о тахикардии. Частота сердечных сокращений может увеличиваться при физической или эмоциональной нагрузке (это нормальная реакция здорового сердца).
Повышение температуры тела вызывает тахикардию. Считается, что увеличение температуры тела на 1 градус приводит к увеличению частоты сердечных сокращений на 10 ударов.
Тахикардия может быть признаком очень многих болезней, но может быть и вариантом нормы.
Некоторые виды тахикардии требуют специального антиаритмического лечения.
Если частота пульса меньше 60 ударов в минуту, говорят о брадикардии.
Брадикардия может быть у абсолютно здоровых людей. Она, как правило, отмечается у спортсменов.
Умеренная брадикардия создает благоприятные условия для кровоснабжения мышцы сердца. Это связано с тем, что кровь к ней может поступить только тогда, когда она находится в состоянии расслабления (т.е. между сокращениями). Чем чаще ритм, тем больше крови необходимо для восполнения энергетических затрат сердечной мышцы, а период расслабления, при этом все короче. Поэтому, некоторые лекарства (например атенолол или анаприлин), способные урежать ритм (удлинять период расслабления) улучшают кровоснабжение сердечной мышцы.
Если брадикардия появилась внезапно, если урежение ритма сопровождается головокружением, или потерей сознания – немедленно обратитесь к врачу.
Посоветоваться с врачом надо и если частота пульса менее 50 в минуту, а других неблагоприятных признаков нет.
При некоторых формах брадикардии приходится вживлять специальный прибор – кардиостимулятор. Этот прибор берет на себя управление ритмом сердца в том случае, когда собственный водитель ритма (синусовый узел) не справляется со своей задачей.
Экстрасистолия
Если в правильный ритм сердечных сокращений вплетается преждевременное сокращение, говорят об экстрасистолии.
По тому, месту, из которого исходит электрический импульс, приведший к преждевременному сокращению, все экстрасистолы делят на предсердные и желудочковые.
Даже у абсолютно здорового человека несколько раз в сутки могут наблюдаться экстрасистолы. Однако, их появление – повод для обращения к врачу-кардиологу. Как и все аритмии, экстрасистолия – не самостоятельное заболевание, а лишь признак какой-либо болезни. Именно на поиск причины аритмии и будет направлено обследование.
Мерцательная аритмия – самая частая аритмия
Что такое мерцательная аритмия
Мерцательная аритмия – разновидность нарушений ритма, при которой из согласованной работы сердца выключаются предсердия. Электрический импульс с большой частотой бегает по предсердиям, вызывая хаотическое сокращение мышечных волокон (фиблилляцию). Поэтому, мерцательную аритмию еще иногда называют фибрилляцией предсердий. Некоторые импульсы прорываются к желудочкам, сокращение которых происходит из -за этого в неправильном, нерегулярном ритме. Отсутствие правильного ритма и есть основной признак мерцательной аритмии.
Иногда не удается выявить причину мерцательной аритмии, тогда говорят об идеопатической ее форме. Чаще всего мерцательная аритмия – признак порока сердца, ишемической болезни сердца, артериальной гипертонии и т.д. Не только сердечно-сосудистые заболевания могут приводить к мерцательной аритмии. Среди частых причин – болезни щитовидной железы, легких, острые и хронические отравления (например, алкоголем) и многие другие заболевания.
Важно, что для успеха в лечении мерцательной аритмии необходимо не только правильное назначение специальных антиаритмических препаратов, но и коррекция ее причины.
Проявления (симптомы) мерцательной аритмии
Самым частым проявлением мерцательной аритмии является ощущение сердцебиения. Оно связано с тем, что средний ритм желудочков при мерцательной аритмии обычно учащается и может доходить до 130-150 ударов в минуту. Часто ощущаются перебои в работе сердца, иногда резкое чувство нехватки воздуха, болевые ощущения в области сердца, головокружение. Примерно 1 из 10 больных вообще не ощущает появление мерцательной аритмии.
Виды мерцательной аритмии
Длительно существующую мерцательную аритмию называют постоянной. Если она возникает приступообразно говорят о пароксизмальной форме.
Мерцательная аритмия с высокой частотой сердечных сокращений называется тахисистолической, с нормальной частотой – нормосистолической и с низкой частотой – брадисистолической формой.
Надо ли лечить мерцательную аритмию
По разным оценкам от 1,5 до 5% человечества страдает этим видом аритмии. Это самый частый вид аритмии, требующей лечения. Появление мерцательной аритмии (если ее не лечить) существенно (в 5-7 раз) увеличивает риск инсульта, тромбоэмболии легочной артерии. Возрастает и вероятность развития сердечной недостаточности. Дополнительные факторы, такие как возраст, наличие тяжелых сопутствующих заболеваний еще более увеличивает риск инсульта и сердечной недостаточности у больных с мерцательной аритмией.
Поэтому, мерцательную аритмию надо лечить обязательно.
Восстановление правильного ритма сердца
Целью лечения у больного, страдающего мерцательной аритмией является, при возможности, восстановление синусового (правильного) ритма сердца и последующее его поддержание.
Имеется несколько способов, позволяющих восстановить правильный ритм. Первый – самый простой – может попробовать на себе сам больной. Метод основан на возможности стимуляции вагуса – нерва, замедляющего ритм сердца. Необходимо сделать глубокий вдох. Затем крепко зажать нос и рот, и попробовать выдохнуть с усилием. Этим способом можно прекращать и другие приступы сердцебиения. К сожалению, этот метод помогает далеко не всем больным.
Наиболее распространенным является восстановление ритма сердца с помощью лекарственных препаратов. Эти лекарства называются антиаритмическими. Как правило, лекарства вводят внутривенно. Однако, в некоторых случаях, больной сам может принять подобранное ранее лекарство, которое у него прекращает приступ мерцательной аритмии. К сожалению, не существует специальных признаков, позволяющих определить, какое из лекарств окажется более эффективным. На практике приходится перебирать несколько лекарств, прежде чем подобрать препарат, более всего подходящий больному.
В некоторых случаях, когда приступ мерцательной аритмии не поддается лечению лекарствами, если он существует уже длительное время, имеется непосредственная угроза для жизни больного, для восстановления ритма применяют так называемую электрическую кардиоверсию. Больной на короткое время (1-2 мин) погружается в сон, затем специальным синхронизированным (т.е. наносимым в определенную фазу сердечного цикла) разрядом электрического тока ритм сердца восстанавливается. Метод имеет несколько недостатков – необходимость погружать больного в сон, необходимость специального оборудования для проведения процедуры. Кроме того, эта процедура должна проводиться в больнице, в которой работает высококвалифицированный персонал. Но есть и значительные преимущества. Так, ритм восстанавливается почти во всех случаях (в отличие от лекарств, восстанавливающих ритм лишь в 60- 80%). Этот способ наиболее безопасен, так как любое лекарство имеет побочные эффекты. Если они появились, то нужно время, чтобы лекарство ушло из крови. Учитывая эти преимущества были созданы специальные вшиваемые под кожу аппараты – кардиовертеры, которые улавливают мерцательную аритмию и прекращают ее. Однако широко пока эти аппараты не применяются.
После восстановления ритма необходимо его поддерживать. Требуется проведение лечения заболевания, которое привело к мерцательной аритмии, устранение факторов, провоцирующих приступ. Если приступы редкие, то иногда от специальной антиаритмической терапии воздерживаются. Однако чаще всего приходится принимать лекарство, предотвращающее развитие приступа.
Иногда, при часто возникающих, тяжело переносимых больным приступах приходится применять хирургическое лечение.
Поддержание нормальной частоты сердцебиения при невозможности восстановления ритма
В некоторых случаях приходится отказаться от восстановления нормального ритма. Обычно в этом случае у больного имеется так называемая постоянная форма мерцательной аритмии. Основными лечебным мероприятием является поддержание нормальной частоты сердечных сокращений и профилактика осложнений.
Профилактика осложнений мерцательной аритмии
Поскольку основными осложнениями мерцательной аритмии являются инсульт и сердечная недостаточность, то их профилактика так же должна проводиться у больного с мерцательной аритмией. Способ такой профилактики выбирает Ваш врач.
Рекомендации больному с мерцательной аритмией
Постарайтесь выяснить и сказать Вашему врачу, что предшествует очередному приступу мерцательной аритмии. Это может быть необычна физическая нагрузка, повышение артериального давления, прием каких-либо лекарств, прием алкоголя, обострение заболевания легких, и т.д.
Научитесь считать пульс (или попросите Вашего врача научить Вас) и распознавать – есть ли у Вас мерцательная аритмия или ритм сердца правильный.
Если приступ не прошел самостоятельно в течение 2-3 часов, не прошел от приема обычных лекарств, вызывает неприятные ощущения, боли, одышку – обращайтесь к врачу. Чем раньше от момента начала приступ начать его лечить – тем проще восстанавливается правильный ритм.
Обязательно имейте при себе последнюю (или несколько последних) электрокардиограмму. Они могут понадобиться для сравнения в экстренном случае.
Не надейтесь на свою память, имейте при себе листок с названием и дозировкой принимаемых Вами препаратов. Это может оказаться очень важным, если Вам будут вводить новое лекарство, поскольку многие вещества взаимодействуют друг с другом.
Если Вы принимаете фенилин или синкумар – лекарства, снижающие уровень протромбина и предотвращающие инсульт и тромбоэмболию – не забывайте консультироваться с врачом, если:
- появились признаки кровоточивости (носовые кровотечения, появление крови на деснах при прикусывании, стали появляться синяки)
- если Вы стали принимать новые лекарства или изменили дозировки принимаемых ранее лекарств
- если поменялась диета (например, начался новый сезон)
- если Вы простудились, если у Вас расстройство желудка, или любое новое заболевание. Если Вам планируется какая либо операция, или удаление зуба – предупредите Вашего врача, что вы принимаете эти лекарства.
Обследование больного с аритмиями
Для того, чтобы правильно лечить аритмию, необходимо пройти специальное обследование. Оно состоит из двух частей. Первая – выявление самой аритмии, условий ее возникновения и прекращения. Вторая – поиск заболевания, приведшего к аритмии.
Для выявления аритмии ее надо зарегистрировать. Для этого записывают электрокардиограмму. Далеко не всегда на обычной ЭКГ выявляется искомая аритмия. Поэтому, следующим этапом регистрируют электрокардиограмму в течение длительного периода времени (обычно сутки), затем, с помощью специального компьютера запись расшифровывается. Этот метод обследования носит названия суточного мониторирования ЭКГ по Холтеру. В некоторых клиниках больным выдают на дом специальные устройства, позволяющие передавать ЭКГ при необходимости своему врачу. Этот способ так же позволяет зафиксировать редкие нарушения ритма. Часто физическая нагрузка провоцирует аритмии, поэтому для измерения уровня допустимой физической активности и оценки профилактического действия антиаритмических лекарств иногда применяют пробу с физической нагрузкой.
Нарушения ритма сердца
Аритмия сердца – патологическое состояние, при котором происходят нарушения частоты, ритмичности и последовательности возбуждения и сокращения сердца. Аритмия — любой ритм сердца, отличающийся от нормального синусового. При аритмии нарушается нормальная сократительная активность сердца, что может привести к целому ряду серьёзных осложнений. Термин «аритмия» объединяет различные по механизму, клиническим проявлениям и прогностическому значению нарушения образования и проведения электрического импульса.
Наиболее частые причины нарушений сердечного ритма и проводимости:
- Кардиальные причины:
- ИБС;
- сердечная недостаточность;
- кардиомиопатия;
- пороки сердца (приобретенные, врожденные);
- миокардиты;
- пролапс митрального клапана.
- Лекарственные воздействия:
- сердечные гликозиды;
- антиаритмические препараты (проаритмическое действие);
- диуретики;
- симпатомиметики.
- Электролитные нарушения
- Токсические воздействия:
- курение;
- алкоголь;
- тиреотоксикоз.
- Идиопатические аритмии
В основе нарушений ритма сердца лежит изменение условий формирования возбуждения сердечной мышцы или аномалия путей его распространения. Аритмии могут быть вызваны как функциональными нарушениями, так и тяжёлыми органическими поражениями сердца. В некоторых случаях причиной нарушений сердечного ритма являются врождённые особенности проводящей системы сердца. Определённую роль в возникновении аритмии играет состояние нервной системы. Например, психическое, эмоциональное напряжение вызывает изменения в темпе, а зачастую — и в ритме сердечных сокращений, в том числе, и здоровых людей. Аритмия нередко возникает у людей с заболеваниями центральной и вегетативной нервной системы.
Разные заболевания, сопровождающиеся нарушением анатомической структуры сердца или происходящих в нем обменных процессов, вызывают различные по продолжительности и характеру виды аритмии, и установить диагноз может только врач, выводы которого основываются на клинико-электрокардиографических данных.
Симптомы аритмий
Достаточно часто пациенты не ощущают наличие аритмий. В этих случаях аритмия выявляется при обычном диспансерном обследовании. Однако у многих пациентов возникают различные ощущения в грудной клетке, которые чаще всего включают:
- ощущение сердцебиения и перебоев в груди;
- очень частое биение сердца;
- чрезвычайно медленное биение сердца («замирание» сердца);
- боли в груди;
- головокружение;
- потерю сознания или ощущение, близкое к обмороку.
Классификация аритмий
1. Нарушения автоматизма:
а) номотопные (водитель ритма — в синусовом узле):
- синусовая тахикардия;
- синусовая брадикардия;
- синусовая аритмия;
- синдром слабости синусового узла (СССУ).
б) гетеротопные (водитель ритма — вне синусового узла):
- нижнепредсердный ритм;
- атриовентрикулярный ритм;
- идиовентрикулярный ритм.
2. Нарушения возбудимости:
- по источнику: предсердные, атриовентрикулярные, желудочковые;
- по количеству источников: монотопные, политопные;
- по времени возникновения: ранние, интерполированные, поздние;
- по частоте: единичные (до 5 в минуту), множественные (более 5 в минуту), парные, групповые;
- по упорядоченности: неупорядоченные, аллоритмии (бигеминия, тригеминия, квадригеминия).
б) пароксизмальные тахикардии (предсердная, АВ, желудочковая)
3. Нарушения проводимости:
а) увеличение проводимости (WPW синдром);
б) уменьшение проводимости (блокады: синоаурикулярная, внутрипредсердная, АВ, блокада ножек пучка Гиса).
4. Смешанные (трепетание/мерцание предсердий, желудочков)
Диагностика
ЭКГ является основным методом диагностики аритмий. Однако не всегда можно выявить аритмию при снятии ЭКГ покоя. В таких случаях в клинике «К+31» проводится суточное мониторирование ЭКГ (холтеровское мониторирование). Часть аритмий провоцируется физической нагрузкой, в таких случаях для их диагностики используются нагрузочные пробы (тредмил).
Осложнения
Ряд нарушений ритма может привести к развитию тяжелых осложнений. При неправильном ритме сокращений в сердце замедляется кровоток, что приводит к формированию тромбов в предсердиях. При отсутствии адекватной терапии эти тромбы могут разносится с током крови по организму, приводя к закупорке артерий головного мозга (инсульту), артерий кишечника, нижних конечностей. Длительное существование некоррегируемой аритмии часто приводит к развитию сердечной недостаточности.
Лечение аритмий
- если аритмия является следствием какого либо заболевания (например, тиреотоксикоза), наши доктора проводят терапию основного заболевания;
- назначаются антиаритмические препараты (влияющие на проводящую систему сердца, а также на различные ионные каналы).
Для предотвращения развития осложнений рекомендуется динамическое наблюдения врача-кардиолога за пациентом даже в период ремиссии.

 Полина Мирошникова
Полина Мирошникова Антон Чугунов
Антон Чугунов Андрей Панов
Андрей Панов
