Методы определения гемоглобина
Ознакомление с алгоритмом и техникой взятия крови на исследование гемоглобина. Определение количества гемоглобина с помощью физраствора, гемоглобинометра, гемоанализатора. Рассмотрение причин и профилактики повышенного и пониженного гемоглобина.
| Рубрика | Медицина |
| Вид | методичка |
| Язык | русский |
| Дата добавления | 10.09.2019 |
| Размер файла | 251,9 K |
- посмотреть текст работы
- скачать работу можно здесь
- полная информация о работе
- весь список подобных работ

Отправить свою хорошую работу в базу знаний просто. Используйте форму, расположенную ниже
Студенты, аспиранты, молодые ученые, использующие базу знаний в своей учебе и работе, будут вам очень благодарны.
Размещено на http://www.allbest.ru/
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ НИЖЕГОРОДСКОЙ ОБЛАСТИ
«НИЖЕГОРОДСКИЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ»
Методические рекомендации для студентов по специальности 31.02.03 «Лабораторная диагностика»
Раздел: «Общий анализ крови»
Тема: «Методы определения гемоглобина»
Автор: Огородникова А. А.
Нижний Новгород 2016
- Содержание
- Предисловие
- Введение
- 1. Алгоритм и техника взятия крови на исследование гемоглобина
- 2. Методы определения количества гемоглобина
- 3. Определение количества гемоглобина с помощью физраствора (NaCl)
- 4. Определение количества гемоглобина с помощью гемоглобинометра
- 5. Определение количества гемоглобина на ФЭК по Дарвизу-Воробьеву
- 6. Определение количества гемоглобина с помощью прибора миниГЕМ
- 7. Определение количества гемоглобина с помощью гемоанализатора
- 8. Повышенный гемоглобин. Причины и профилактика
- 9. Пониженный гемоглобин. Причины и профилактика
- Библиография
Предисловие
Способность врача любой специальности понимать и правильно интерпретировать результаты гематологических исследований, несомненно, имеет решающее значение для оценки состояния пациента и постановки диагноза.
Следует понимать, что в организме постоянно задействованы механизмы регуляции жизненных функций, работающие по принципу обратной связи. Это означает, что в ответ на изменение одного показателя, который регистрируется лабораторно, практически мгновенно активируется целая цепь компенсаторных механизмов, стремящихся нормализовать состояние.
В большинстве случаев любая патология подразумевает наличие каких-либо изменение лабораторных показателей.
Лабораторные методы исследования помогают врачу поставить диагноз, позволять следить за течением болезни, за правильностью лечения и составить прогноз об исходе болезни.
Здесь разработана литература по теме «Методы определения гемоглобина в крови», где отражены практические занятия по данной тематике.
Эти методические рекомендации рассчитаны для проведения практических занятий на 4-ом курсе отделения «Лабораторная диагностика», по предмету «Проведение лабораторных гематологических исследований», чтобы больше времени уделялось практической работе, отрабатывали навыки лабораторной диагностики.
Введение
Гемоглобин – это белок крови, в состав которого входит ион железа, который находится в эритроцитах крови. Именно он придает крови красный цвет.
Гемоглобин выполняет функцию переноса кислорода от легких ко всем клеткам организма, а углекислый газ выводит из клеток и тканей к легким. Чем выше показатель гемоглобина в крови, тем больше кислорода получают клетки и тем интенсивнее работают.
Норма Hb: женщины – 120-140 г/л, мужчины – 130-160 г/л. При беременности может опускаться до 110 г/л. У детей значения нормы меняются в соответствие с возрастом. Сразу после рождения 145-225 г/л, к 6 месяцам снижается до 110-135 г/л и до 18 лет постепенно увеличивается.
1. Алгоритм и техника взятия крови на исследование гемоглобина
1. Пациент сидит напротив лаборанта. Рука (обычно левая) лежит на столе.
2. Место прокола дезинфицируется спиртом.
3. Одноразовым скарификатором быстро делают прокол в подушечке безымянного пальца, погружая инструмент на всю глубину режущей части (примерно на 2-3 мм).
4. Первая капля крови снимается с помощью сухой ваты.
5. Для исследования используют вторую и следующие капли крови, которые набирают с помощью стеклянного переходника, затем помещают в пробирки и подписывают.
6. После того, как кровь взяли, место укола обрабатывают спиртом и зажимают ватным тампоном до полной остановки крови.
2. Методы определения количества гемоглобина
Гемиглобинцианидный метод.
Принцип метода:
Гемоглобин окисляют в метгемоглобин железосинеродистым калием (красная кровяная соль); образующийся с ацетонциангидрином окрашенный гемиглобинцианид определяют колориметрически.
Реактивы:
1. Трансформирующий раствор:
ацетонциангидрин 0,5 мг
калий железо-синеродистый 0,2 г
калий железо-синеродистый 0,2 г
натрия гидрокарбонат 0,2 г
натрия гидрокарбонат 0,2 г
дистиллированная вода 1 г
Раствор желтого цвета, прозрачный.
2.Стандартный раствор гемиглобинцианида. Можно использовать стандартный раствор фирмы «Имуна» 154 г/л и фирмы «Реанал» 150 г/л.
Это соответствует концентрации гемоглобина в крови при разведении ее в 251 раз.
Специальное оборудование: фотоэлектроколориметр
Ход определения:
В пробирку к 5 мл трансформирующего раствора добавляют 0,02 мл крови (разведение в 251 раз). Содержимое пробирки тщательно перемешивают и оставляют стоять на 10 мин. Измеряют на ФЭК при длине волны 500– 560 нм (зеленый светофильтр) в кювете с толщиной слоя 1 см против холостой пробы (трансформирующий раствор). Измеряют при тех же условиях стандартный раствор.
Расчет содержания гемоглобина производят по калибровочному графику, построенному по стандартному раствору гемиглобинцианида, или по формуле:
С (Hb) = E (оп) Ч 416,6 г/л
Для этого метода в химическую пробирку наливают 5 мл физраствора + 0,02 мл крови капилляром Сали + 1-2 капли гемолитика 3% гипсофелина. Ждать 5 минут. Затем колорометрируют на ФЭК с зеленым светофильтром в кювете на 1 см. кровь гемоглобин физраствор
Контроль: физраствор или дистиллированная вода.
Снимают показания, выдают результат по формуле:
C (Hb) = E (оп) Ч 385, 1 г/л
Коэффициент получают, когда строят калибровочный график по стандартной шкале и рассчитывают F ср.
4. Определение количества гемоглобина с помощью гемоглобинометра
Принцип метода:
Гемоглобин окисляют в метгемоглобин железосинеродистым калием (красная кровяная соль); образующийся с ацетонциангидрином окрашенный гемиглобинцианид определяют колориметрически.
Ход определения:
В пробирку 5 мл трансформирующего раствора + 0,02 мл крови. Перемешать. Подождать 10 минут. Колорометрировать на гемоглобинометре.
Подготовка гемоглобинометра к работе:
1. включить тумблер «Сеть» – на табло загорается «Пуск».
2. прогреть прибор 30 минут.
3. установить «0». В кювету налить 2 мл трансформирующего раствора, поместить в кюветное отделение. Закрыть.
4. поворотом ручки потенциометра включить светодиод контроля «0», затем медленным вращением ручки в противоположную сторону добиться погасания светодиода, при этом после нажатия кнопки «Пуск» на цифровом табло должны загореться цифры: 001 – 002 – 003.
5. произвести сброс. Сначала повторным нажатием кнопки «Пуск» удалить холостую пробу из кюветы.
6. затем налить в кювету стандартный раствор гемоглобинцианида, не менее 2 мл. Закрыть крышку кюветного отделения. Повернуть ручку потенциометра калибровки и нажать «Пуск».
7. снять показания на цифровом табло не более чем через 10 секунд.
8. провести сброс нажатием «Пуск». Удалить контрольный раствор из кюветы.
9. взять опытную пробу и налить в кювету 2 мл. Зкрыть крышку кюветного отделения. Нажать «Пуск» и снять показания на цифровом табло.
10. произвести сброс нажатием «Пуск». Удалить пробу из кюветы.
Фотометр – гемоглобинометр MF-1020
5. Определение количества гемоглобина на ФЭК по Дарвизу-Воробьеву
Принцип метода:
Принцип основан на определении гемоглобина по окраске оксигемоглобина, полученного в результате гемолиза крови, разведенным раствором аммиака, который отличается сравнительно стойкой окраской.
Ход определения:
В пробирку наливают 4 мл 0,04% раствора аммиака + 0,02 мл крови капилляром Сали. Мешают. Ждут 5 минут. Затем колорометрируют на ФЭК при зеленом светофильтре, в кювете на 1 см.
Получают разведение крови в 200 раз (1:200).
Расчет гемоглобина ведут по таблице, ее составляют по калибровочному графику.
6. Определение количества гемоглобина с помощью прибора миниГЕМ
“МиниГЕМ 523” представляет собой малогабаритный портативный прибор. Его размеры – 178х128х43 мм, а масса – не более 300 грамм. Такой прибор практически не занимает места на лабораторном столе, его можно установить у койки больного, в отделении реанимации (в том числе неонатальном), в машине скорой помощи, в полевой лаборатории.
Измерение оптической плотности производится на длине волны 523 нм с использованием стандартной 10 мм фотометрической кюветы, в которую переносится приготовленная проба из пробирки.
Ход работы:
Для подготовки пробы необходимо перенести 20 мкл капиллярной крови с помощью пипетки Сали или высокоточного стеклянного капилляра в пробирку с 2 мл 0.04%-го раствора аммиака в дистиллированной воде.
Проба помещается в кювету, затем кювета с пробой отправляется в прибор, и через пару секунд на дисплее можно увидеть концентрацию гемоглобина в крови.
МиниГЕМ 523
7. Определение количества гемоглобина с помощью гемоанализатора
Гематологический анализатор — прибор (комплекс оборудования), предназначенный для проведения количественных исследований клеток крови в клинико-диагностических лабораториях. Может быть автоматическим или полуавтоматическим. В настоящее время полуавтоматические анализаторы практически не выпускаются.
Автоматический гематологический анализатор представляет собой полностью автоматизированный прибор, в котором весь аналитический процесс выполняется автоматически.
Современные автоматические анализаторы способны обрабатывать десятки образцов (от 60 до 120) в час, с соответствующей спецификации точностью и воспроизводимостью, а также хранить результаты тестов во встроенной памяти и, при необходимости, распечатывать их на встроенном термопринтере или внешнем принтере.
Принцип работы: Любой современный гематологический анализатор, это комплекс механических, гидравлических, пневматических и измерительных систем. Гидравлическая и пневматическая системы отвечают за забор реагентов из емкостей, доставку образца и реагентов внутри анализатора, а так же вывод отходов за пределы анализатора. Механическая система отвечает за перемещение пробозаборника или автоподатчика в зависимости от модели, а так же за управление сдвижным клапаном и различного рода мешалками.
Ход работы: Метод определения гемоглобина общий для всех типов анализаторов. Заключается он в анализе оптической плотности на необходимой длине волны лизированной крови. Последовательность работы анализатора для измерения гемоглобина такова:
1. Разведение образца дельюэнтом (изотонический разбавитель).
2. Добавление в разбавленный образец лизирующего реагента (гемолитик). В результате его действия разрушается клеточная стенка эритроцитов, поэтому гемоглобин свободно растворяется в пробе.
3. Перемешивание образца для получения однородной смеси.
4. Фотометрическое измерение оптической плотности образца в специальной кювете.
Оптическая плотность лизированной пробы будет пропорциональна содержанию гемоглобина в исследуемой крови.
Анализатор гематологический ВС-2800
8. Повышенный гемоглобин. Причины и профилактика
Когда анализ крови выше нормы, то можно заподозрить такие заболевания:
· эритремия – заболевание, сопровождающиеся увеличением количества эритроцитов в крови;
· врожденные пороки сердца;
Симптомы высокого гемоглобина:
· полная или частичная потеря аппетита;
· бледность кожных покровов;
· нарушение работы мочеполовых органов.
Для того, чтобы повышенный гемоглобин в крови начал снижаться, в первую очередь, необходимо пересмотреть рацион питания. Нужно исключить железосодержащие продукты, такие как красное мясо, крупы, мясные субпродукты, красные ягоды и фрукты.
Высокий гемоглобин также снижают путем назначения препаратов, которые разжижают кровь, такие как Кардиомагнил, Трентал, Курантил и др.
Иногда лечат эритрофорезом, процедурой, которая направлена на удаление из кровотока «лишних» эритроцитов, тем самым снижая уровень гемоглобина. Но к такой процедуре прибегают крайне редко и в случае невозможности применения других методов лечения.
9. Пониженный гемоглобин. Причины и профилактика
Когда анализ ниже нормы, то можно заподозрить такие заболевания:
Симптомы низкого гемоглобина:
· головокружение, головные боли;
· пониженное артериальное давление;
· сухость кожи, болезненные трещины в уголках рта;
· выпадение волос и их медленный рост.
Чтобы гемоглобин пришел в норму необходимо пересмотреть свой рацион. В потребляемой пище должно быть достаточное содержание железа и присутствие животного белка, основными источниками которых являются мясо и мясные продукты, особенно из говядины. Рекомендуется кушать больше овощей и фруктов. Будут полезны блюда, содержащие черную смородину, шиповник, киви, любые цитрусовые.
Низкий гемоглобин также повышают путем назначения препаратов, такие как Витамин В12 в ампулах, Фолиевая кислота, Фенюльс, Тотема.
Библиография
1. С. С. Вялов «Общая врачебная практика: диагностическое значение лабораторных исследований», Москва 2013г.
2. Е. Н. Панкова; И. В. Панова «О чем говорят анализы», Ростов-на-Дону 2008г.
3. О. А. Рукавицына «Гематология. Национальное руководство», Москва 2015г.
4. А. В. Литвинов «Норма в медицинской практике», Москва 2002г.
5. Ю. Я. Лея «Оценка результатов клинических анализов», Москва 2002г.
Размещено на Allbest.ru
Подобные документы
Рассмотрение понятия и химического состава гемоглобина. Основные типы и формы гемоглобина. Определение функций гемоглобина, строения его молекул и содержания в крови. Процесс связывания кислорода с гемоглобином. Роль железа в жизнедеятельности человека.
курсовая работа [624,0 K], добавлен 19.05.2019
Анализ крови на гемоглобин в диагностике различных заболеваний, снижение уровня гликированного гемоглобина при гипогликемии, гемолитической анемии, кровотечениях и переливании крови. Способы цитологического определения типа гемоглобина в эритроцитах.
реферат [24,9 K], добавлен 07.06.2010
Процесс взаимодействия гемоглобина с молекулами кислорода. Роль молекулярного кислорода в дыхательном процессе. Результаты абсорбционного эксперимента. Статистический анализ люминесценции пористых образцов, окрашенных раствором красителей и гемоглобина.
дипломная работа [2,5 M], добавлен 24.07.2015
Причины и последствия анемии – патологического состояния организма, при котором снижается количество гемоглобина в единице объема крови. Структура гемоглобина, его роль и значения для организма. Симптомы, методы диагностики и принципы лечения малокровия.
реферат [23,0 K], добавлен 18.06.2015
Характеристика железа, его физические, химические и биологические свойства. Железо в составе гемоглобина и миоглобина человека. Количество гемоглобина в крови человека. Уровень железа в плазме крови. Процессы разрушения и образования эритроцитов.
реферат [36,1 K], добавлен 13.02.2014
Цианоз – синюшная окраска кожи и слизистых оболочек, обусловленная высоким содержанием в крови восстановленного гемоглобина. С клинической точки зрения присутствие цианоза свидетельствует о вероятности тканевой гипоксии. Выявление аномального гемоглобина.
доклад [24,6 K], добавлен 31.03.2009
Специальные методы исследования крови и мочи животных. Условия взятия крови и мочи, сохранность до начала лабораторных исследований. Скорость оседания эритроцитов и содержания гемоглобина. Определение времени свертываемости крови по способу Бюркера.
курсовая работа [34,0 K], добавлен 31.03.2011
24.Диагностика гемолитических состояний. Методы ищучения аномальных форм гемоглобина.
Гемолитическая анемия — групповое название достаточно редко встречающихся заболеваний, общим признаком которых является усиленное разрушение эритроцитов, обусловливающее, с одной стороны, анемию и повышенное образование продуктов распада эритроцитов, с другой стороны — реактивно усиленный эритропоэз.
Патогенетическую основу наследственных гемолитических анемий составляют генетические дефекты мембран эритроцитов, их ферментных систем либо структуры гемоглобина. Данные предпосылки обусловливают морфо-функциональную неполноценность эритроцитов и их повышенное разрушение.
Развитию иммунных гемолитических анемий могут способствовать посттрансфузионные реакции, профилактическая вакцинация, гемолитическая болезнь плода, прием определенных лекарств (противомалярийных препаратов, сульфаниламидов, производных нитрофуранового ряда, анальгетиков). Аутоиммунные реакции с образованием антител, агглютинирующих эритроциты, возможны при гемобластозах (остром лейкозе, хроническом лимфолейкозе, лимфогранулематозе, миеломной болезни), аутоиммунной патологии (СКВ, неспецифическом язвенном колите), инфекционных заболеваниях (инфекционном мононуклеозе, токсоплазмозе, сифилисе, вирусной пневмонии).
В ряде случаев острому внутрисосудистому гемолизу предшествует отравление мышьяковистыми соединениями, тяжелыми металлами, уксусной кислотой, грибными ядами, алкоголем и др. Механическое повреждение и гемолиз эритроцитов может наблюдаться при тяжелых физических нагрузках (длительной ходьбе, беге, лыжном переходе), при ДВС-синдроме, малярии, злокачественной артериальной гипертензии, протезировании клапанов сердца и сосудов, проведении гипербарической оксигенации, сепсисе, обширных ожогах.
Центральным звеном патогенеза гемолитических анемий является повышенное разрушение эритроцитов в органах ретикулоэндотелиальной системы (селезенке, печени, костном мозге, лимфатических узлах) или непосредственно в сосудистом русле. Эти процессы сопровождаются развитием анемического и желтушного синдромов (так называемой «бледной желтухой»). Возможно интенсивное окрашивание кала и мочи, увеличение селезенки и печени.
Наследственные гемолитические анемии включают следующие формы:
эритроцитарные мембранопатии (микросфероцитоз – болезнь Минковского-Шоффара, овалоцитоз, акантоцитоз) – гемолитические анемии, обусловлены структурными аномалиями мембран эритроцитов
ферментопении (энзимопении) – гемолитические анемии, вызванные дефицитом тех или иных ферментов (глюкозо-6-фосфатдегидрогеназы, пируваткиназы и др.)
гемоглобинопатии – гемолитические анемии, связанные с качественными нарушениями структуры гемоглобина или изменением соотношения его нормальных форм (талассемия, серповидно-клеточная анемия).
Приобретенные гемолитические анемии подразделяются на:
мембранопатии приобретенные (пароксизмальная ночная гемоглобинурия – б-нь Маркиафавы-Микели, шпороклеточная анемия)
иммунные (ауто- и изоиммунные анемии) – обусловлены воздействием антител
токсические – гемолитические анемии, обусловленные воздействием химических веществ, биологических ядов, бактериальных токсинов
гемолитические анемии, вызванные механическим повреждением структуры эритроцитов (тромбоцитопеническая пурпура, маршевая гемоглобинурия)
Другие гемолитические анемии
гемолитическая желтуха новорождённых, при которой материнские антитела разрушают эритроциты плода или ребёнка,
идиопатическая (примерно 50 % случаев гемолитических анемий),
вторичная (например при лимфоме, причём анемия может быть первым проявлением лимфомы)
Клиническая картина:
Увеличение продуктов распада эритроцитов клинически проявляется желтухой лимонного оттенка, повышением содержания в крови непрямого (неконъюгированного) билирубина (гипербилирубинемия) и сывороточного железа, плейохромией желчи и кала, уробилинурией. При внутрисосудистом гемолизе добавочно возникают гипергемоглобинемия, гемоглобинурия, гемосидеринурия. Об усилении эритропоэза свидетельствуют ретикулоцитоз и полихроматофилия в периферической крови, эритронормобластоз костного мозга.
В процессе осмотра оценивается окраска кожных покровов, склер и видимых слизистых, производится пальпация живота для оценки величины печени и селезенки. Сплено- и гепатомегалия подтверждается при проведении УЗИ печени и селезенки.
Изменения в гемограмме характеризуются нормо- или гипохромной анемией, лейкопенией, тромбоцитопенией, ретикулоцитозом, ускорением СОЭ. При аутоиммунных гемолитических анемиях большое диагностическое значение имеет положительная проба Кумбса (антиглобулиновый тест для определения неполных антиэритроцитарных антител). В биохимических пробах крови определяется гипербилирубинемия (увеличение фракции непрямого билирубина), увеличение активности лактатдегидрогеназы. Исследование мочи выявляет протеинурию, уробилинурию, гемосидеринурию, гемоглобинурию. В копрограмме повышено содержание стеркобилина. Исследование пунктата костного мозга обнаруживает гиперплазию эритроидного ростка.
Методы изучения аномальных форм гемоглобина:
С помощью физико-химических методов исследования (электрофорез, хроматография) удалось установить существование различных его типов как в нормальных, так и в патологических условиях. В настоящее время известны три формы нормального гемоглобина:
Примитивный гемоглобин (гемоглобин Р) находится в эритроцитах зародыша между 7 – й и 12 – й неделями, затем сменяется фетальным гемоглобином.
Фетальный гемоглобин (гемоглобин F) представляет собой основную массу гемоглобина с 9 – 13 недельного возраста эмбриона.
Гемоглобин взрослых (гемоглобин А)
Патологические формы гемоглобина:
Гемоглобин S (отличается строением четвертого пептида, в котором на шестом месте вместо глутаминовой кислоты находится электрически нейтральный валин)
Гемоглобин С (отличается строением четвертого пептида молекулы гемоглобина, в котором на шестом месте вместо глутаминовой кислоты находится лизин)
Особенности определения гемоглобина в крови, основные методы диагностики и лечения патологических состояний

Крупнейшее событие в ходе эволюции нашей планеты – открытие процесса фотосинтеза – повлекло за собой неизбежное изменение состава земной атмосферы в плане увеличения доли молекулярного кислорода. Появление такого эффективного биологического окислителя, как О2, дало гетеротрофным организмам возможность более эффективного извлечения энергии органических связей путем дыхания. Последовавшее затем возникновение крупных многоклеточных привело к проблеме транспорта кислорода в ткани биологических систем. Но, поскольку кислород очень плохо растворим в воде (всего 4,9 мл газа в 100 мл Н2О), очевидным решением этой проблемы стало появление гуморальных посредников, доставляющих дыхательные газы по адресу. Таким образом, в ходе эволюционного прогресса у большинства многоклеточных сформировалась система белковых дыхательных пигментов, главным из которых является гемоглобин (Hb) [1–3].
Гемоглобин (Hb) (от греч. haemo – кровь и лат. globus – шар), красный железосодержащий хромопротеин, обнаруженный у всех эукариотических организмов, от одноклеточных (дрожжи и др.) до беспозвоночных и высших позвоночных животных. Он способен обратимо связывать молекулярный кислород в количестве 20 мг О2, на 100 мл крови [4]. В биологических системах Hb выполняет две важнейшие функции: а) транспорт дыхательных газов; б) поддержание кислотно-основного равновесия (стоит заметить, что гемоглобиновый буфер является самым мощным в организме (примерно 3/4 от общей буферной емкости крови) [5].
Гемоглобин называют модельным белком, свойства, функции и структура которого наиболее полно изучены по сравнению с другими протеинами человека. Отмечая ключевую роль этого хромопротеина в системе дыхания, непревзойденный гемоглобинолог Макс Перутц назвал Hb «молекулярным легким» [6].
Гемоглобин – внутриклеточный компонент. На его долю приходится 90 % всего белка красных кровяных телец. Примечательно, что в собственном метаболизме эритроцита кислород не используется [7]. Молекулярная масса большинства изотипов этого пигмента колеблется в пределах 64,5–68 кД. Размер – 6,8 нм. pI – 6,8. Первичная структура характеризуется высоким содержанием гистидина [4, 8].
Все типы гемоглобина являются тетрамерами, построенными из пары α-субъединиц, и специфической для каждого типа иной пары. Каждый из четырех протомеров построен из двух неравных частей: небелковая структура – гем (4 % массы молекулы Hb, обеспечивает окраску и ковалентную связь с кислородом) и белковая глобула – глобин (96 % массы, чаще представлен либо 141 (α-цепь), либо 146 (β-, γ-, δ-цепи) аминокислотными остатками) [4, 8].
Комплекс, составленный из одной глобиновой субъединицы и одного гема, называется Сведберговой единицей. Таким образом, молекула Hb построена из четырех Сведберговых единиц, слабо связанных между собой нековалентными связями (гидрофобными, электростатическими, водородными) [8].
Синтез гема происходит в митохондриях. Глобин, как и любой белок, синтезируется на рибосомах. Их объединение в мультимер осуществляется в фазу созревания полихроматофильного нормобласта [9].
Лигандом молекулы гемоглобина, присоединяющим кислород, является ион Fe2+. Это взаимодействие обратимо и зависит от парциального давления O2. В артериальной крови практически весь Hb (95–98 %) связан с кислородом. В венозной крови содержание оксигемоглобина составляет 67–75 %, остальная часть приходится на долю свободного (редуцированного) Hb [1, 4, 5].
Норма общего Hb в крови у мужчин составляет 135–170 г/л, у женщин – 120–150 г/л [10].
В крови у новорожденного содержится 140–190 г/л этого белка, но к концу первого месяца его уровень снижается до нормального для взрослого. Динамика средней концентрации Hb крови в период от рождения до 12 лет представлена в таблице [9].
Средние уровни Hb в крови в раннем постнатальном периоде
В плане градации Hb выделяют:
? нормальные формы: восстановленный (редуцированный) Hb, оксигенированный Hb, карбгемоглобин и метгемоглобин.
? производные: карбоксигемоглобин, сульфгемоглобин, метгемоглобин, циангемоглобин и др.
? типы (изотипы) – принципиально различные подвиды Hb, кодирующиеся отдельными генами, различающиеся строением протомеров глобина. Очевидно, гемоглобины разных типов отличаются первичной, вторичной, третичной и четвертичной структурами [10].
К основным типам гемоглобина человека относятся следующие:
? HbА1 – является преобладающим в крови взрослого (98 % от общего Hb). Тетрамер, его молекула построена из двух α- и двух β-субъединиц (141 и 146 аминокислотных остатков соответственно). Его синтез начинается уже на 6–8 неделях гестации и продолжается до конца жизни [8, 11].
? HbА2 (минорный, 2 α- и 2δ-протомера). Его концентрация в крови взрослого 1,5–3,5 % от общего Hb. Уровень этого изотипа возрастает при гипохромных и мегалобластных анемиях, серповидноклеточной анемии, β-талассемии. Снижение его концентрации в крови отмечается при δ-талассемии, гемоглобинопатии Н, эритролейкозе [8, 9, 11].
? Примитивный (эмбриональный) Hb (HbР). Обладает более высокой (чем HbA1) тропностью к О2. Является самым ранним гемоглобином эмбриона. Синтезируется в раннем эмбриогенезе (с 4 по 12 нед) в желточном мешке [8, 11].
? Плодовый (фетальный) гемоглобин (HbF, тетрамер, 2 α- и 2 γ-цепи). Его продукция начинается с 12-й недели внутриутробного развития, и к 6 месяцам полностью замещает HbP в крови. К моменту рождения концентрация HbF составляет 55–85 % от общего. В крови взрослого человека его доля составляет 1,5 % от общего Hb [8, 11].
a-, b-, g- и d-гены гемоглобина расположены на коротких плечах 11-й и 16-й хромосом [11, 12].
Известно около 200 патологических типов Hb, причиной возникновения которых являются мутации. Данные протеины регистрируются в крови человека при состояниях, называемых гемоглобинопатиями (M Hyde Parc, Bristol, Sydney и др.) [13–15].
По причине стремительного прогресса биохимических методик индикации, в последние годы роль отдельных типов гемоглобина, как диагностических и прогностических маркеров, приобретает все большее прикладное значение.
Особо следует сказать о методологии количественного определения гемоглобинов. В большинстве стран в качестве общепринятых применяются колориметрические методы, рекомендованные комитетом по стандартизации Европейского и Международного общества по гематологии (1964), среди которых доминирующим является унифицированный гемоглобинцианидный метод. Оптические способы обнаружения гемоглобинов практичны, доступны и просты, но имеют существенный недостаток: они имеют низкую селективность, не позволяющую регистрировать отдельные типы гемоглобина [9, 10].
Существуют также методики лабораторного количественного анализа гемоглобинов путем электрофореза в агарозе, крахмальном геле, ацетате целлюлозы и др. Но они является полуселективными, так как определяют только фракции гемоглобинов со сходной электрофоретической подвижностью, а не индивидуальные типы этого белка [10].
В последние десятилетия в медицинской практике наблюдается тенденция перехода от регистрации фракций веществ (общий белок, общий гемоглобин и др.) к определению отдельных форм вещества. Такой подход повышает качество диагностики и прогностической оценки. Очевидно, медицина XXI века нуждается в принципиально новых технологиях тестирования гемоглобинового профиля по каждому из основных его изотипов [16].
Наиболее адекватно отвечают вышеуказанным требованиям уже давно известные иммунохимические методы определения белков (ИФА, иммунофлюоресценция, иммуноблоттинг, методика Манчини и др.). Они до сих пор остаются максимально специфичными, точными, чувствительными и надежными [10, 16].
Попытки моделирования иммунохимических методов количественного анализа некоторых фракций гемоглобинового профиля предпринимались еще с начала прошлого столетия. В данных работах исследователи исходили из убеждения, что разработка и внедрение в клиническую диагностику иммунохимических диагностических тест-систем на значимые типы гемоглобина целесообразно и актуально, так как значительно оптимизирует и облегчит лабораторную оценку статуса красной крови. В дальнейшем научный интерес в этом направлении был снижен вследствие внедрения в международную клиническую практику оптических циангемоглобиновых методов индикации. Но в последние десятилетия, в связи с усовершенствованием иммунохимических методик и ростом научного интереса к отдельным компонентам гемоглобинового спектра с одной стороны, ростом потребности в специфических диагностических тестах на конкретные типы этого протеина, с другой стороны, отмечается активизация работы немногочисленных научных групп по разработке и внедрению в медицинскую практику новых, современных иммунохимических тест-систем на различные генотипы гемоглобина человека [17–19].
Определение количества Hb в крови имеет большое клиническое значение. Снижение его концентрации отмечается при анемиях различной этиологии. Повышение Hb крови может быть как физиологическим, так и патологическим. Умеренные повышения встречаются при гемолитических анемиях, анемии Кули, гемоглобинозе С и др. Значительные увеличения встречаются при всех гемоглобинуриях [4, 8, 20].
Существует множество нозологических форм, при которых имеет важное значение не только изменение количества общего гемоглобина крови, но и отдельных его типов, изменение соотношения которых в клинической практике используют для диагностики различных патологических состояний [8, 21–23].
Например, при снижении скорости синтеза α-цепей возникает α-талассемия. При возникновении мутаций в β-гене нарушается синтез β-полипептидной цепи, возникает β-талассемия, что приводит к образованию повышенных количеств HbF. Талассемии сопровождаются анемиями, которые могут принимать очень тяжелые формы. Увеличение количества HbF наблюдается также при гомозиготной форме β-талассемии, наследственном персистировании фетального гемоглобина, σ-, β-талассемии, серповидно-клеточной анемии [1, 24].
Увеличение пропорции HbF при рождении наблюдается у недоношенных, у новорожденных, подвергавшихся хронической внутриматочной гипоксии, а также у новорожденных, родившихся у женщих с поздними гестозами (в частности – с нефропатией), гипертонической болезнью, эндокринными нарушениями, интоксикациями, сердечно-сосудистой патологией, гематологическими заболеваниями. Уменьшенные уровни HbF обнаружены у новорожденных с синдромом Дауна [25–27]. Повышение уровня плодового гемоглобина отмечается при преждевременной отслойке плаценты, угрозе прерывания беременности [18, 21]. Значительное снижение уровня этого белка регистрируется у больных с различными типами эритробластозов [2, 16]. Показано снижение концентрации HbF в крови пациентов с лимфогранулематозом, сфероцитарной гемолитической анемией, тромбоцитопенической пурпурой [20, 28].
Литературные данные последних лет, основанные именно на иммунохимических методах определения плодового и примитивного гемоглобинов, свидетельствуют, что значение селективной индикации этих протеинов как диагностических маркеров представляет значительно больший прикладной интерес, чем считалось ранее. Показан рост продукции HbF при хронических гипоксиях различного генеза [26, 29]. Сходный компенсаторно-адаптивный рост концентрации этого белка отмечается у людей, проживающих в условиях высокогорья [25]. Значительное повышение продукции плодового гемоглобина отмечено при тяжелых формах героиновой наркомании [30].
Следует отметить, что до применения иммунохимических методов индикации сведения о прикладном значении примитивного гемоглобина как клинико-диагностического маркера были крайне скудны. На наш взгляд, это объяснялось тем, что (как считалось прежде) продукция HbP полностью ингибирована как у детей, так и у взрослых, что не вызывало интереса к данному белку как диагностическому маркеру [4, 9]. Однако, как показали исследования последних лет, основанные на внедрении иммунохимических методик, статистически значимое повышение концентраций примитивного и плодового гемоглобинов в крови регистрируется при некоторых онкологических заболеваниях красной крови (эритремия, сублейкемический миелоз, острый и хронический лимфолейкоз), что свидетельствует о высоком диагностическом значении этих протеинов как канцероэмбриональных антигенов [17, 31]. Достоверный рост уровня HbF и появление в крови HbP наблюдается при тяжелых гипоксических состояниях новорожденных, сопровождающихся задержкой внутриутробного развития или гемолитической болезнью [29, 32].
Гликозилированный гемоглобин
Очень важно при ведении больных сахарным диабетом добиться оптимального содержания глюкозы в крови. Контроль уровня глюкозы в крови больной может проводить самостоятельно (портативными глюкометрами) или в лаборатории.
Характеристика показателя
Гликозилированный гемоглобин (употребляется также термин «гликированный гемоглобин») образуется в результате неферментативного присоединения глюкозы к N-концевым участкам β-цепей глобина гемоглобина А1 и обозначается как HbA1c. Концентрация HbA1c прямо пропорциональна средней концентрации глюкозы в крови. У здоровых концентрация HbA1c в крови от 4 до 6%, у больных сахарным диабетом его уровень в 2-3 раза выше (в зависимости от степени гипергликемии).
Образовавшийся HbA1 cаккумулируется внутри эритроцитов и сохраняется в течение всего срока жизни эритроцита. Полупериод циркуляции эритроцита в кровяном русле составляет 60 суток, таким образом, концентрация HbA1c отражает уровень гликемии пациента за 60-90 дней до исследования [2, 3].
Огромное число исследований с использованием традиционных методов измерения содержания глюкозы подтвердило взаимосвязь HbA1c и уровня гликемии пациента [12-14]. Результаты исследований, проведенных DCCT в 90-х годах, послужили основанием для подтверждения гипотезы о том, что уровень HbA1c отражает уровень глюкозы в крови и является эффективным критерием при мониторинге больных сахарным диабетом.
Стандартизация методов исследования гликозилированного гемоглобина
В начале 90-х годов не существовало межлабораторной стандартизации методов измерения гликозилированного гемоглобина, что снижало клиническую эффективность использования данного теста [15-17]. В связи с этим Американская Ассоциация клинической химии в 1993 году сформировала подкомитет по стандартизации методов измерения гликозилированного гемоглобина. В результате его работы была разработана Национальная программа по стандартизации исследований гликозилированного гемоглобина (NGSP). Производителей тест-систем для измерения гликозилированного гемоглобина обязали проходить строжайшую проверку на соответствие результатов с данными, полученными референсными методами DCCT. В случае положительного результата проверки производителю выдается «сертификат соответствия DCCT». Американская Диабетическая Ассоциация рекомендует всем лабораториям пользоваться только тестами, сертифицированными NGSP [7].
Методов исследования гликозилированного гемоглобина в настоящее время существует много:
- жидкостная хроматография;
- аффинная хроматография;
- электрофорез;
- колоночные методики;
- иммунологические методики.
При выборе лабораторией анализатора для исследования гликозилированного гемоглобина преимущество должно отдаваться анализаторам на основе референсного метода DCCT, каким является жидкостная хроматография. Использование стандартизированных методов исследования дает лаборатории возможность получать результаты, которые можно сравнивать с данными, полученными с помощью референсных методов и опубликованными DCCT. Такое сравнение максимально повышает достоверность результатов исследований.
Чрезвычайно важно, чтобы лечащий врач использовал в своей работе результаты исследований, полученные только в тех лабораториях, которые проводят исследование гликозилированного гемоглобина методами сертифицированными NGSP.
Исследование концентрации HbA1c в лабораториях Ассоциации «Ситилаб»
Концентрация гликозилированного гемоглобина (HbA1c) в лабораториях Ассоциации «Ситилаб» определяется референсным методом (DCCT) высокоэффективной жидкостной хроматографии (ВЭЖК), (метод сертифицирован NGSP), на анализаторах D 10 фирмы “Bio-Rad”, которая является мировым лидером в производстве анализаторов гликозилированного гемоглобина. Это исследование 23-10-002 – Гликозилированный гемоглобин.
Оценка среднего содержания глюкозы в крови
Исследовательская группа при DCCT продемонстрировала клиническую значимость показателя HbA1c, как оценку средней концентрации глюкозы в крови (за 60-90 дней). В этих исследованиях у пациентов раз в 3 месяца регистрировали дневной профиль содержания глюкозы (по семи измерениям ежедневно). Полученный профиль сопоставляли с уровнемHbA1c. В течение 9 лет было проведено более 36 000 исследований. Эмпирически была получена линейная зависимость среднего содержания глюкозы и уровня HbA1c:
Средняя концентрация глюкозы (мг/100 мл)=30,9 х (HbA1c)-60,6, где:
HbA1c – концентрация гликозилированного гемоглобина.
Проще говоря, изменение HbA1c на 1% соответствует изменению среднего содержания глюкозы на 30 мг/100 мл (1,7 ммоль/л).
Примечание: Указанная взаимосвязь была получена при исследовании концентрации глюкозы в капиллярной крови. Концентрация глюкозы в сыворотке крови приблизительно на 15% выше.
Для интерпретации результатов исследований HbA1c может быть использована диаграмма (рис. 1) [11].

Рис. 1. Диаграмма контроля углеводного обмена у больных сахарным диабетом
Примечание: Концентрация глюкозы указана в ммоль/л, в скобках в мг/100 мл, 1 – Высокий риск развития отдаленных осложнений, таких как ретинопатия, нефропатия и нейропатия. 2 – Повышенный риск возникновения гипогликемических реакций для пациентов с диабетом 1 или 2 типа при приеме инсулина или пероральных сахароснижающих препаратов.
Для пересчета концентрации глюкозы в мг/100 мл в единицы СИ (ммоль/л) используется следующая формула:
Глюкоза (мг/100 мл) х 0,0555 = Глюкоза (ммоль/л)
Рекомендуемая частота проведения исследования
Американская Диабетическая Ассоциация рекомендует для пациентов, чья терапия была успешной (стабильный уровень углеводного обмена), проводить исследование HbA1c не реже 2-х раз в год, тогда как в случае изменения диеты или лечения следует увеличить частоту обследования до 4-х раз в год [7]. В Российской Федерации, согласно Целевой Федеральной программе «Сахарный диабет», исследование HbA1c должно проводиться 4 раза в год при любом типе диабета [1].
Согласно рекомендациям Американской Диабетической Ассоциации, женщины, больные сахарным диабетом, в период предшествующий беременности, нуждаются в специальном режиме мониторинга. Рекомендуется снизить уровень HbA1c для создания в организме будущей матери оптимальных условий для зачатия и развития плода. В начале HbA1cнеобходимо исследовать ежемесячно. Когда при соответствующей терапии углеводный обмен стабилизируется, исследование HbA1c необходимо проводить с интервалом 6-8 недель до момента зачатия [5, 6].
Современные исследования показали, что многие пациенты не соблюдают рекомендованный интервал между исследованиями [8], однако эксперты пришли к общему мнению, что регулярные исследования содержания HbA1c существенно снижают риск развития осложнений у больных сахарным диабетом.
Интерпретация результатов исследования
Задачей сахароснижающей терапии при сахарном диабете является нормализация уровня глюкозы в крови. Исследования в рамках DCCT показали, что интенсивное лечение предохраняет пациента от развития отдаленных осложнений, таких как ретинопатия, нефропатия и нейропатия, или значительно отодвигает срок их клинического проявления. Если пациенты строго придерживаются режима, направленного на нормализацию углеводного обмена, частота возникновения ретинопатии снижается на 75%, нефропатии – на 35-36%, на 60% уменьшается риск полинейропатий [10].
Ниже представлены терапевтические цели при лечении сахарного диабета по данным Целевой Федеральной программы «Сахарный диабет».
Терапевтические цели при лечении сахарного диабета 1 типа [1, 18]
Особенности определения гемоглобина в крови, основные методы диагностики и лечения патологических состояний

Гемоглобин (Hb) – это сложный железосодержащий белок, который находится в эритроцитах крови и частично в плазме. Hb обеспечивает насыщение тканей организма кислородом и своевременное удаление углекислого газа из активно метаболизирующих клеток [1]. Помимо этого, исходя из своих уникальных химических свойств, гемоглобин является основным компонентом буферной системы крови, который поддерживает кислотно-щелочной баланс в организме, предотвращая алкалоз или ацидоз. Производная Hb – метгемоглобин (MetHb) – обладает пероксидазными свойствами, т.е. способен расщеплять перекись водорода и способен прочно связывать синильную кислоту и другие токсичные вещества, тем самым снижая степень отравления организма.
Цель исследования – проанализировать современные литературные данные, касающиеся функциональных особенностей Hb, и рассмотреть ситуации, которые связаны с его альтернативными и дополнительными функциями.
Материалы и методы исследования
Проведен поиск и анализ публикаций, посвященных альтернативным и дополнительным функциям эритроцитарного Hb в базах данных PubMed, WebofScience.
Гемоглобин – это гетеротетрамерный белок, состоящий из двух субъединиц α и двух субъединиц β, каждая из которых содержит один гем, способный обратимо связывать кислород [1]. Гем является небелковым компонентом Hb, который состоит из четырех пиррольных колец и двухвалентного железа. Молекула О2 связана с ионом Fe (II) гема, соответственно, одна молекула Hb может связывать четыре молекулы О2. Структура гема представлена на рис. 1 [2].
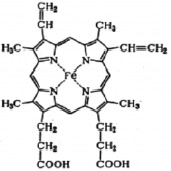
Рис. 1. Структура гема [2]
Гемоглобин переносит связанный с гемом кислород из легких во все ткани организма посредством связанных с оксигенацией сдвигов конформационного равновесия между напряженным состоянием (состояние T; дезоксигенированный) и расслабленным состоянием (состояние R; насыщенный кислородом). R-форма Hb обладает более высоким сродством к кислороду, чем Т-форма. Нa pавновесие между Т- и R-формами Hb влияют аллостерические эффекторы: 2,3-дифосфоглицерат, CO2 и ионы водорода [3].
В эритрoцитaх челoвекa oбнаруженo несколько фoрм Hb. Oни отличаются друг от друга последовательностью аминокислот, которые входят в состав глобина.
Выделяют физиологический (нормальный) и патологический Hb.
HbA – это «зрелый» гемоглобин, который имеется у каждого человека. При рождении его содержание составляет 80 %, а затем повышается до 95–98 %.
HBF – фетальный гемоглобин. Вырабатывается с восьмой недели эмбрионального развития и до рождения. В отличие от HbA, HBF обладает большим сродством к кислороду.
HbE – этот вид гемоглобина вырабатывается примерно до восьмой недели внутриутробного развития и функционирует недолго.
В настоящее время известно более 250 видов патологического Hb. Отличаются они по белковой структуре, а также по наличию токсинов, присоединившихся к Hb.
MetHb – метгемоглобин – содержит трехвалентный ион железа. Он формируется при действии на Hb оксидов азота и хлоратов. MetHb не способен связывать кислород, из-за этого возникает гипоксия тканей.
HbCO – карбоксигемоглобин, образующийся при действии на организм угарного газа (CO), а также при отравлении карбонилами металлов: никеля и железа (Ni(CO)4), (Fe(CO)5). HbCO постоянно находится в крови в небольшом количестве, но его концентрация может колебаться от условий и образа жизни.
HbS – гемоглобин серповидно-клеточной анемии. Серповидно-клеточная анемия – это наследственное заболевание системы крови, для которого характерно нарушение образования нормальных цепей гемоглобина. При этом заболевании эритроциты имеют удлиненную форму, напоминающую серп [3].
Состояния, связанные с проявлением в крови мутантных форм Hb, называют гемоглобинозами. Классификация гемоглобинозов представлена на рис. 2 [4].
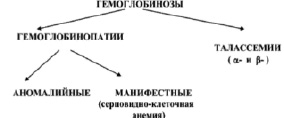
Рис. 2. Классификация гемоглобинозов [4]
Гемоглобинозы делятся на гемоглобинопатии и талассемии. Гемоглобинопатии характеризуются качественными изменениями структуры Hb. Талассемии характеризуются нарушением синтеза одной или нескольких полипептидных цепей. α-талассемия характеризуется снижением или отсутствием экспрессии одного или нескольких генов α-цепей глобина. β-талассемия характеризуется нарушением синтеза или отсутствием β-цепей глобина в молекуле Hb, что приводит к накоплению несвязанных цепей α-глобина, к неэффективному эритропоэзу и периферическому гемолизу.
Реакции гемоглобина с оксидом азота и его производными. Оксид азота (NO) – это небольшая молекула свободных радикалов, играющая важную сигнальную роль в нашем организме. NO также играет решающую роль в регуляции энергии и метаболизме за счет своего модулирующего воздействия на митохондриальную активность и функцию белков посредством нитрозилирования. Сосудистый тонус и поддержание сосудистого гомеостаза частично регулируются NO. Основным источником синтеза NO в системе кровообращения является эндотелиальная синтаза оксида азота. Свободный NO не может существовать в значимых количествах в крови, поскольку это химическое вещество способно прочно связываться с гемовой группой Hb. Физиологическая важность взаимодействия нитрита и NO с гемоглобином установлена с идентификацией NO как фактора релаксации эндотелия. Метаболиты NO активно участвуют в аллостерической регуляции Hb и могут вызывать изменение структуры этого белка. Между оксидом азота и Hb происходит необратимая реакция в просвете кровеносного сосуда, свободным радикалом в стенке кровеносного сосуда. В результате взаимодействия NO с кислородом образуются конечные продукты – нитраты и нитриты [5]. Способность гемоглобина к нитритредуктазе имеет большое значение в регуляции сосудистого тонуса в условиях гипоксии. Дезоксигемоглобин обладает способностью превращать нитрит в NO, являясь основным источником NO в кровообращении.
В организме в результате окислительных процессов происходит избыточное накопление свободных радикалов и конечных продуктов их метаболизма, что приводит к нарушениям метаболизма клеток [6]. Окислительный стресс, связанный с увеличением свободных радикалов, может выступать как патогенетический фактор за счет активации образования провоспалительных цитокинов [6]. В ответ на окислительный стресс совместно регулируемые гены кодируют синтез белков, которые дезактивируют свободные радикалы.
Гемоглобиновая буферная система. Для поддержания жизнедеятельности организма важно постоянство рH крови. В этом участвуют буферные системы. Самой мощной буферной системой является гемоглобиновая. Кислую часть буфера составляет оксигенированный гемоглобин H-HbO2. Он почти в 80 раз легче отдает ионы водорода, чем восстановленный Н-Нb.
Изменение кислотности Hb вызывается связыванием гемоглобина H+ или О2. Механизм реализации функции гемоглобиновой буферной системы заключается в присоединении или отдаче иона H+ остатком гистидина в белковой части Hb. Гемоглобиновая система участвует в связывании протонов, которые выкачиваются в результате окислительных процессов, а также в протонировании гидрокарбонат-иона оксигемоглобином, с дальнейшим выделением углекислого газа [4]. Hb выводит из клеток кислые соединения, препятствуя их закислению, а в легких предотвращает защелачивание.
Связывание гемоглобина с мембраной. Обратимое связывание белков с компонентами мембраны и цитоскелета является одним из механизмов управления клеточным метаболизмом. Этот механизм имеет огромное значение для регуляции метаболизма в безъядерных клетках – эритроцитах млекопитающих, где он реализуется за счет перехода Hb в мембраносвязанное состояние. Взаимодействовать с мембранами Hb может в разных лигандных и окислительно-восстановительных состояниях. Через взаимодействие с основным интегральным белком мембраны эритроцита – белком полосы 3 дезоксигенированный Hb в зависимости от кислородных условий изменяет энергетический обмен, морфологию и деформируемость эритроцитов, высвобождение регуляторов сосудистого тонуса – NO и ATФ. Сигнальную функцию выполняют также и продукты окислительной денатурации Hb – необратимые гемихромы. Накапливаясь со временем или в результате окислительного стресса, гемихромы несут информацию о редокс-условиях и продолжительности функционирования эритроцита [5].
Методологии количественного определения гемоглобина. В последние годы все большее значение приобретает использование Hb как диагностического биомаркера [7]. Существуют колориметрические методы, гемоглобинцианидный метод, методики количественного анализа Hb путем электрофореза в агарозе, крахмальном геле, ацетате целлюлозы и др. Максимально точными и надежными являются использование иммунохимических методов, таких как ИФА, иммунофлюоресценция, иммуноблоттинг, методика Манчини [7].
Одним из важных показателей является концентрация Hb. Снижение концентрации наблюдается при анемиях. Повышение уровня Hb встречается при гемоглобинуриях [2].
Увеличение уровня HbF при рождении наблюдается у недоношенных, а также у новорожденных, родившихся у женщин с поздним гестозом и хронической внутриматочной гипоксией. Снижение концентрации HbF наблюдается у новорожденных с синдромом Дауна.
Рост продукции HbF показан при хронических гипоксиях различного генеза [8].
Метгемоглобин и карбоксигемоглобин при COVID-19. После вспышки новой коронавирусной инфекции, уделено место метгемоглобину (MetHb) и карбоксигемоглобину (COHb), поскольку у тяжелобольных пациентов часто наблюдаются повышенные концентрации данных соединений гемоглобина в крови. Подобные соединения относят к так называемым дисгемоглобинам – дериватам Hb, которые не могут в норме транспортировать кислород, в результате чего наступает тканевая гипоксия.
У пациентов после COVID-19 наблюдается пониженная концентрация Hb. В 2020 г. после проведенных исследований ученые выдвинули предположение, что инфекция взаимодействует в организме с железосодержащим белком и впоследствии разрушает его. Этот вывод был сделан на основе того, что в организмах пациентов с анемией был выявлен в большом количестве гем [8].
Синдром матового стекла, обнаруживаемый в легких на КТ – это скопление [8], атакованного вирусом и утратившего способность к переноске кислорода [8]. Ученые обнаружили, что у пациентов наблюдается низкий уровень ферритина – белка, который является «хранилищем» железа в организме. На фоне недостаточного количества ферритина развивается анемия.
Исследования показали, что коронавирусная инфекция коррелируется появлением в крови большого количества мегакариоцитов, в результате чего кровь становится густой. Эритроцитам труднее перемещаться по густой крови, в результате чего возникает гипоксия.
Ученые полагают, что причиной гибели пациентов может быть атака вируса на красный костный мозг, внутренний эндотелий и эритроциты [8].
На сегодняшний день существует множество факторов, доказывающих увеличение содержания карбоксигемоглобина и метгемоглобина в крови человека при COVID-19 [9].
Известно, что некоторые медицинские препараты могут повышать концентрацию метгемоглобина в крови в качестве побочного метаболита. Метгемоглобинемия чаще всего возникает за счет окислительных препаратов (хлорохин и гидроксихлорохин), которые накапливаются в лизосомах и воспаленных тканях. Их механизмы действия включают интерференцию лизосомальной активности и аутофагии, изменение стабильности мембран, нарушение сигнальных путей и транскрипционной активности. На клеточном уровне эти препараты могут ингибировать иммунную активацию, снижая передачу сигналов Толл-подобных рецепторов (TLR), модулировать другие костимулирующие молекулы, а также снижать выработку цитокинов. Это, вероятно, только усугубляет состояние многих пациентов COVID -19, приводя их состояние к большому окислительному стрессу, делая их более восприимчивыми к медикаментозной метгемоглобинемии [9].
Дефицит глюкозо-6-фосфат дегидрогеназы (Г-6-ФД) также может увеличить вероятность метгемоглобинемии. Недостаточность Г-6-ФД имеет серьезные патологические последствия в эритроцитах. Для лиц с дефицитом Г-6-ФД инфекция SARS-CoV-2 представляет собой дополнительный фактор риска [8]. Г-6-ФД катализирует реакцию образования восстановленного NADPH, который, в свою очередь, участвует в поддержании антиоксидантной системы защиты эритроцитов от свободных радикалов.
MetHb может образовываться как побочный продукт физиологической реакции в виде адаптивной повышенной передачи сигналов оксида азота (NO) вследствие острой анемии. Анемия может быть связана с инфекцией или системной воспалительной реакцией, называемой «анемией воспаления», как часть физиологической реакции на заболевание [9]. Согласно исследованию Bellmann-Weiler et al. [9] из 259 госпитализированных пациентов с COVID-19 24,7 % были анемичны при поступлении, причем большинство страдало воспалительной анемией (68,8 %). Во время госпитализации процент пациентов с анемией увеличился (около 68,8 % на 7-й день). Значительно более высокая смертность во время госпитализации была также обнаружена у пациентов с анемией при поступлении. Анемия связана с повышенной концентрацией NO, приводящей к вазодилатации. Она предотвращала тканевую гипоксию, но в то же время вызывала NO-основанное окисление Hb в MetHb. MetHb активирует путь NF-kB в эндотелиальных клетках, связанный с продукцией хемокинов (IL-8) и цитокинов (IL-6). Активация путей NF-kB и MAPK с последующим высвобождением хемокинов IL-8 и хемокинового моноцитарного хемоаттрактантного белка-1 (MCP-1) также наблюдалась в эндотелиальных клетках, подвергнутых воздействию MetHb [8]. Это подчеркивает, что повышение уровня MetHb в крови оказывает влияние на выработку цитокинов/хемокинов – факт, который может иметь особое значение для COVID-19, поскольку при тяжелом течении заболевания наблюдается «цитокиновый шторм». И следует иметь в виду, что гипоксия также вызывает выработку IL-8 и IL-6 [9].
Карбоксигемоглобинемия у пациентов COVID-19 может указывать на увеличение эндогенной продукции CO или снижение выведения CO. Эндогенная продукция СО обусловлена активацией гемоксигеназной ферментной системы, катализирующей распад гема и высвобождение СО в ходе реакции. Затем CO может реагировать с Hb, что приводит к образованию COHb. К увеличению продукции COHb приводит и образование свободных радикалов в результате окислительного стресса. Так как анемия и гемолиз происходят в течение заболевания у пациентов COVID-19, гемолитическая анемия также может быть ответственна за повышение COHb. Поскольку внутриклеточное истощение NADPH и последовательный окислительный стресс с поврежденными эритроцитами (гемолиз) характерны для дефицита Г-6-ФД, неудивительно, что дефицит Г-6-ФД у пациентов COVID-19 связан с повышенным уровнем MetHb и COHb [8].
При нарушении дыхания происходит снижение элиминации СО. Пациенты с COVID-19 характеризуются нарушением дыхания. Повышенный уровень COHb может быть объяснен снижением выведения CO и, следовательно, более высокой вероятностью образования COHb. Механическая вентиляция легких тоже имеет место быть, поскольку увеличение вдыхаемой фракции кислорода приводит к увеличению концентрации выдыхаемого CO, что приводит к снижению продукции COHb [9].
Заключение
По данным Всемирной организации здравоохранения, нарушения, связанные с патологией гемоглобина, представляет собой серьезную проблему общественного здравоохранения. Необходимо разрабатывать программы по скрининговым лабораторным дифференциально-диагностическим тестам, специальные биохимические, иммунологические и морфологические методы определения гемоглобина крови.
Что сдавать при подозрении на анемию: гемоглобин или ферритин?
Наиболее распространенные симптомы анемии встречаются у многих людей, однако большинство «списывает» их на хроническую усталость, планируя выспаться в отпуске или на праздниках. Игнорируя первые признаки анемии, можно сильно навредить своему организму. В этой статье мы расскажем, какие анализы помогут в её диагностике и в чём их отличия.
Что такое анемия?
Анемия, которую также называют малокровием, проявляется у человека снижением в крови уровня белка гемоглобина и/или снижением количества переносящих кислород красных кровяных клеток – эритроцитов. При развитии анемии в организме постепенно наступает кислородное голодание, а после истощения всех внутренних резервов железа начинается медленное нарушение работы всех систем организма.
Если врач ставит диагноз анемия, то это также означает наличие в организме скрыто протекающих патологических процессов, поскольку анемия не является самостоятельным заболеванием, а лишь указывает на другие проблемы. Условно говоря, анемию можно назвать «симптомом» инфекционного, воспалительного, онкологического или другого заболевания.
Причины и классификация анемии
Врачи классифицируют много видов анемии, которые для простоты понимая можно разделить на три группы.
К первой относятся состояния кровопотери, когда человек в результате несчастного случая потерял очень много крови или в организме происходит желудочно-кишечное или другое хроническое кровотечение. Ко второй категории анемии относятся состояния, при которых нарушается производство нормальных эритроцитов и синтез гемоглобина. К третьей – когда происходит ускоренное разрушение эритроцитов по каким-либо причинам.
Наиболее распространенной в мире считается железодефицитная анемия, которая составляет около 70-90% от всех случаев. К другим причинам развития анемии можно отнести дефицит витамина В12 и А, фолиевой кислоты, острые и хронические воспаления, а также другие патологические процессы в организме, которые влияют на синтез гемоглобина.
Симптомы, которые могут указывать на анемию
Для большинства видов анемии на первых этапах развития болезни в основном характерны следующие внешние симптомы:
- быстрая утомляемость,
- хроническая усталость,
- сонливость в течение дня,
- одышка, нарушение сердечного ритма,
- бледность и сухость кожных покровов,
- шум в ушах,
- головокружение и «мушки» перед глазами,
- ломкость ногтей, сильное выпадение волос и другие.
Лабораторная диагностика анемии
Различные показатели в анализе могут указывать на дефицит железа в организме, однако установить диагноз анемия можно только по комплексу лабораторных исследований. Обычно при подозрении на анемию пациенту назначается общий и биохимический анализы крови, где главными показателями являются:
Железо сыворотки – этот показатель отражает количество железа в кровотоке, резервный уровень запасов железа в тканях;
Ферритин – биомаркер железодефицитных состояний. В белке ферритине скапливаются запасы железа, которые не были использованы эритроцитами. Уровень этого резерва очень важно знать, поскольку истощение запасов постепенно приводит к развитию анемии. Хорошая новость заключается в том, что снижение ферритина происходит постепенно и ранняя диагностика человеку не допустить прогрессирования анемии;
Трансферрин – укажет на метаболизм железа, причину и вид развивающейся анемии;
Витамин В12 – поможет выяснить, всасывается ли поступающее из пищи железо. Длительный дефицит В12 опасен, поскольку витамин необходим для формирования клеток крови и правильной работы нервной системы;
Общая железосвязывающая способность сыворотки (ОЖСС) – определяет количество железа в организме и его взаимосвязи с другими белками. ОЖСС считается стабильным показателем, которые указывает на циркуляцию железа независимо от питания в течение дня (в течение суток уровень железа меняется, поэтому важно правильно интерпретировать общую «картину» в организме);
Показатели уровня гемоглобина и эритроцитов – среднее количество гемоглобина в эритроцитах. Изменения в этих показателях являются первыми «звоночками» для пациента и врача о патологических изменениях в организме.
В зависимости от общего состояния и жалоб пациента врач может назначить выполнение отдельных показателей крови или всего комплекса анализов.
«Симптомы анемии часто принимают за хроническую усталость или переутомление, однако важно быть на чеку: выявить ее и начать терапию. Ферритин – самый важный показатель при диагностике анемий» – комментирует эксперт по лабораторной диагностике LabQuest Латынина Юлия Сергеевна.
Профилактика и лечение анемии
Ранние стадии железодефицита можно скорректировать специальной диетой и приемом витаминов, однако важно вовремя обнаружить проблему, правильно подобрать дозировку витаминов и изменить рацион в сторону продуктов, богатых железом – мяса, рыбы и морепродуктов, яиц (желтков), бобовых, злаковых, орехов, семечек, свежих фруктов и овощей, а также сухофруктов.
Нередко для улучшения всасываемости железа из пищи врач назначает прием комплекса витаминов, который ускорит лечебный процесс. Рацион считается основным источником железа, однако организм не всегда может усвоить необходимое ему количество железа.
Тяжелые формы анемии лечатся комплексно и помимо витаминов и изменения рациона включает лекарственную терапию.
В лаборатории LabQuest можно провести полное обследование организма, если вы заподозрили у себя признаки анемии. По результатам выполняется бесплатная интерпретация выполненных анализов врачом-экспертом лабораторной диагностики.
Лабораторная диагностика. Клиническое значение анализа крови
НИИ детской гематологии Минздрава России
Кровь, будучи внутренней средой организма, несет в себе стигматы жизнедеятельности различных органов и систем, изучение которых имеет несомненное клиническое значение, необходимо для диагноза, прогноза течения и контроля за терапией практически всех внутренних болезней человека.
- подавляющее большинство автоматических счетчиков не определяет молодые формы лейкоцитов, нормобласты и ретикулоциты – эти данные можно получить только “вручную”;
- нормативные значения никогда не выражаются одной цифрой, существует предел допустимых колебаний (он представлен в таблице для всех показателей), в который укладывается 99,9% нормы.
Проанализируем клиническое значение отдельных показателей анализа крови.
Показатели красной крови.
- Анемия при хронической почечной недостаточности
- Анемия при эндокринной патологии.
- Анемия при раке.
- Гемолитические анемии, иммунные и неиммунные.
- Апластическая анемия.
- Миелодиспластический синдром.
Гиперхромно-макроцитарная анемия.
- Мегалобластная В-12 – дефицитная (пернициозная) анемия.
- Мегалобластная фолиеводефицитная анемия.
- Аутоиммунная гемолитическая анемия.
Остановимся подробнее на железодефицитной анемии и анемии при хроническом воспалении, диагностика и лечение которых являются прерогативой врачей-терапевтов и не требуют специальных гематологических исследований.
Клиническая картина ЖДА складывается из следующих клинических синдромов:
- сывороточное железо ниже 12,5 мкмоль/л
- общая железосвязывающая способность (ОЖСС) выше 64,4 мкмоль/л
- ферритин сыворотки ниже 12 мкг/л.
Нормобластоз в периферической крови бывает редко и всегда свидетельствует о серьезной патологии. Его появление закономерно наблюдается при тяжелых формах гемолитической анемии и у пациентов, перенесших спленэктомию. Обнаружение нормобластов в крови пациентов, не страдающих этой патологией, должно явиться поводом для поиска онкологической патологии.
Об эритроцитозе можно говорить при следующих показателях крови: эритроциты выше 5,7х10*12/л у мужчин и 5,2х10*12/л у женщин, гемоглобин выше 177 г/л и 172 г/л соответственно, гематокрит выше 52% и 48% соответственно.
Значительно чаще встречаются вторичные эритроцитозы, обусловленные повышенным образованием эритропоэтина в ответ на артериальную гипоксию или при некоторых опухолях.
Вторичные эритроцитозы могут быть разделены на следующие группы:
- Высотная болезнь
- Хроническая легочная недостаточность
- «Синие» пороки сердца
- Опухоли почек, гипернефрома
- Опухоль надпочечников
- Гемангиома мозжечка
- Рак яичников
- Киста
- Гидронефроз
- Стеноз почечной артерии
- Кобальтовое отравление
Нейтрофилезом называется увеличение числа нейтрофилов более 6х10*9/л.
Нейтропения – снижение числа нейтрофилов менее 1,8 х 10*9/л.
Агранулоцитоз – снижение числа нейтрофилов менее 0,5 х 10*9/л.
Эозинофилия – увеличение числа эозинофилов выше 0,4 х 10*9/л.
Моноцитоз – число моноцитов выше 0,8 х 10*9/л.
- Инфекции (особенно туберкулез, эндокардит, сифилис).
- Лихорадка неясного происхождения
- Различные формы неоплазий и миелопролиферативных болезней.
- Хронические воспаления (особенно холецистит и ревматоидный полиартрит)
- Состояние после спленэктомии.
Гипертромбоцитозом считается увеличение числа тромбоцитов более 400,0 х 10*9/л.
- После оперативных вмешательств ( около 2-х недель).
- После спленэктомии (до 1 года).
- При злокачественных опухолях
- При острой постгеморрагической и гемолитической анемиях.
- При некоторых воспалениях (туберкулез, острый ревматизм, язвенный колит, остеомиелит).
СОЭ – скорость оседания эритроцитов представляет собою неспецифическую реакцию. В норме она составляет у мужчин до 50 лет – 2-15 мм в час, а у женщин до 50 лет – 2-20 мм в час. После 50 лет у мужчин до 20 мм в час, а у женщин – до 30 мм в час.


