Лазерная нуклеопластика
- МЕНЮ РАЗДЕЛА









- м. Ясенево, Литовский бульвар, д 1А
- м. Ленинский проспект,
ул. Фотиевой, д 10
- м. Ленинский проспект,
ул. Фотиевой, д 10, стр 1
- ckb@ckbran.ru
Наши специалисты свяжутся с вами в ближайшее время



Лазерная нуклеопластика или лазерная вапоризация – одна из методик оперативного лечения межпозвоночной грыжи. Ее особенность состоит во введении лазерного световода в межпозвоночный диск.
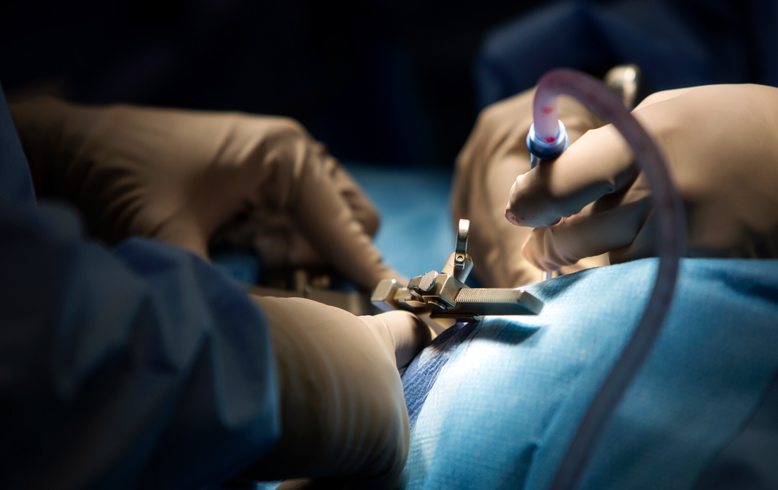
Преимущества метода:
- Малая травматичность;
- Отсутствие осложнений;
- Короткое время проведения операции;
- Быстрое восстановление;
- Местное обезболивание;
- Отсутствие необходимости длительное время находиться в стационаре;
- Не нарушается функции позвоночника и связочного аппарата;
- Можно работать с несколькими дисками;
- Процедура проходит практически без потери крови;
- Можно использовать пациентам, которым полноценная операция противопоказана.
Пункционная лазерная нуклеопластика является эффективной и малотравматичной манипуляцией, не вызывающей осложнений. Лечение межпозвонковой грыжи лазером эффективно, если диск не поврежден, а размер грыжи небольшой. Своевременно проведенная процедура позволит:
- Избавиться от боли;
- Вести привычный образ жизни;
- Предупредить рецидивы в будущем.
Показания и ограничения
Лечение грыжи позвоночника лазером рекомендуется, если у пациента:
- диагностируется дискогенный болевой синдром;
- имеется протрузия диска (диагноз подтвержден МРТ);
- консервативная терапия не дает результатов более 3-х месяцев.
Лазерная нуклеопластика межпозвоночных дисков не позволяет устранить все виды межпозвоночных грыж. Его применение не рекомендуется, если у больного:
- Отсутствует целостность фиброзного кольца;
- Протрузии превышают треть размера спинномозгового канала;
- Вдвое и больше снижена высота кольца;
- В позвоночнике имеется опухоль;
- Диагностирован стеноз;
- Нестабильность или смещение позвонков;
- В области предполагаемого прокола имеется инфекция;
- Хронические заболевания в стадии декомпенсации.
Правила подготовки к нуклеопластике
Отбор пациентов для проведения этой операции происходит по определенным критериям. Нейрохирургу необходимо иметь полную информацию о патологии:
- Локализация дефекта;
- Состояние фиброзного ядра, спинного мозга, позвоночного канала и суставов;
- Размеры протрузии.
Эту информацию позволяет получить МРТ. При необходимости назначают уточняющие обследования:
- Дискографию;
- МРТ с контрастным веществом;
- Миелографию.
Для получения информации о работе жизненно важных органов проводится стандартное обследование:
- ЭКГ;
- Анализ крови и мочи;
- Флюорография;
- Осмотр терапевта.
Особенности проведения операции
Накануне пациенту делается очистительная клизма. Перед операцией вводятся противовоспалительный и успокоительный препараты. Как правило, анестезия местная, но это не обязательно. Важно, чтобы пациент не двигался в течение 20 минут. Если выполнение этого условия вызывает сомнение, решается вопрос о внутривенном наркозе.
Место ввода иглы в каждом отдельном случае выбирается индивидуально.
Лазерная нуклеопластика межпозвоночных дисков проводится под рентгенологическим наблюдением. В процессе работы лазера происходит нагревание и выпаривание тканей диска и декомпрессия – так устраняется избыточное давление. Снижение давления в диске запускает восстановительный процесс:
- Его объем становится меньше;
- Фиброзное кольцо занимает прежнее положение;
- Патология устраняется.
Осложнения после операции
Возможны негативные последствия:
- Воспаление диска;
- Прокол сосуда;
- Повреждение нерва.
Квалифицированный нейрохирург не допускает ошибок, поэтому осложнения – явление редкое. Считается, что эффективность нуклеопластики составляет 80%. Главный риск процедуры – отсутствие эффекта. Такие случаи составляют 20% от общего количества.
Где сделать нуклеопластику в Москве?
Нуклеропластику проводят в клинике РАН, в Москве. Цена формируется с учетом квалификации врача и используемого оборудования. Отзывы пациентов говорят о том, что:
- Операция проходит без боли;
- Болевой синдром устраняется в течение короткого времени;
- Можно обойтись без больничного листа;
- Стоимость операции соответствует затратам на многолетнее лечение консервативным способом.
Записаться на прием к специалисту можно на сайте или воспользоваться для этого контактной информацией.
Как проводится лазерная вапоризация грыжи позвоночника?
Лазерная вапоризация грыжи позвоночника – малоинвазивный метод удаления грыжевого образования путем воздействия на него тока или лазерного луча, что приводит к нагреванию и постепенному выпариванию мягких и хрящевых тканей и уменьшению патологического образования.

Эффективность данного метода лечения
Несмотря на широкое применение методики вапоризации грыжи позвоночника, нельзя назвать этот метод столь уж эффективным. Объясняется это тем, что после проведения процедуры пациент получает лишь кратковременное облегчение из-за уменьшения образования, благодаря чему снижается интенсивность симптоматической картины. Но через некоторое время образование начнет вновь увеличиваться и потребуется повторное проведение операции по удалению грыжи позвоночника.
После вапоризации рецидив грыжи присутствует всегда, вопрос только во времени, поэтому эффективность данного метода удаления межпозвоночного диска под большим вопросом. Тем не менее к данному методу прибегают часто, особенно в тех случаях, когда провести другую операцию не представляется возможным из-за наличия у пациента противопоказаний.
Можно сказать, что вапоризация с помощью лазера является способом быстрого купирования болезненной симптоматической картины, но не методом лечения.
Эффективность лазерной вапоризации в устранении признаков сложно недооценить. Большинство пациентов отмечают, что неприятные симптомы, вызванные наличием грыжи, пропадают уже в ходе малоинвазивной процедуры. Полное устранение признаков патологии происходит через 2-4 дня после вапоризации. Редко случается так, что на восстановление диска и постепенное устранение боли уходит до полугода.
Преимущества лазерной терапии
Вапоризация грыжевого выпячивания относится к наиболее безопасным хирургическим манипуляциям. Она имеет ряд преимуществ:
- отсутствие боли и дискомфортных ощущений;
- проведение без общего наркоза, применяется местная анестезия;
- отсутствие полостных разрезов кожи и мягких структур;
- отсутствие кровопотерь;
- длительность процедуры – не более 60 минут;
- короткий восстановительный период, занимающий по времени не более 4 суток;
- возможность удаления грыжи всех отделов – шейного, поясничного, грудного.






Хотя есть и более эффективные методы удаления грыжи, большинство из них требует применения общей анестезии, к которой многие пациенты (из-за наличия хронических и тяжелых заболеваний) имеют противопоказания, в связи с чем и прибегают к вапоризации. Преимущество этой методики и в том, что вероятность задеть кровеносные сосуды и нервные окончания во время процедуры, если вапоризацию проводит опытный врач, исключается.
Показания к проведению
Выпаривание мягких структур грыжи межпозвоночного диска проводится в следующих случаях:
- возраст пациента 20-50 лет;
- небольшой диаметр патологического образования, не более 6 мм;
- начальные стадии развития грыжевого выпячивания;
- отсутствие положительной динамики от медикаментозной терапии;
- выраженная симптоматическая картина, а также при частых или постоянных болях в спине;
- остеохондроз.






При грыжах большого размера вапоризация не проводится из-за ее малой эффективности.
Противопоказания
Лазерная вапоризация межпозвонковой грыжи запрещена к проведению в следующих случаях:
- грыжа оказывает давление на спинной мозг, который во время процедуры можно повредить;
- наличие спондилеза и похожих нарушений;
- грыжа секвестрированного вида;
- выпадение пульпозного ядра;
- поражение патологическим образованием корешков нервных окончаний;
- возрастная группа – от 50 лет и старше;
- наличие дегенеративного стеноза;
- дисковое окостенение.

Не проводится вапоризация лазером в тех случаях, когда у пациента присутствуют инфекционные и вирусные заболевания в острой стадии или имеются поражения кожи и дерматиты в месте введения пункционной иглы в ходе хирургического вмешательства. В таких случаях операция откладывается до полного выздоровления, чтобы не спровоцировать у пациента возникновения осложнений и побочной симптоматической картины.
Перед проведением процедуры пациент проходит тщательное медицинское обследование на предмет выявления возможных противопоказаний.
Подготовка к процедуре
Применение лазера хоть и является безопасной процедурой, но, т. к. к ней имеются противопоказания, врачу необходимо получить все данные о состоянии пациента, чтобы хирургическая манипуляция стала максимально безопасной. Подготовка к вапоризации включает прохождение медицинского обследования, в числе тестов:
- анализы мочи и крови;
- исследование крови для проверки уровня глюкозы;
- электрокардиограмма;
- компьютерная томография.






Подготовка включает прохождение консультации у нейрохирурга и терапевта. Терапевт по результатам проведенного обследования делает заключение о возможности проведения операции для каждого пациента. Обязательно пациента консультирует анестезиолог, проводятся аллергенные пробы с препаратом, который будет использоваться для местной анестезии.
Этапы лазерной вапоризации
Хирургическая манипуляция проводится по следующему алгоритму:
- Проведение обезболивания. Наркоз вводится в спинномозговую жидкость, благодаря чему пациент будет находиться в сознании, но чувствовать ничего не будет.
- Врач вводит длинную иглу в хрящевые структуры диска. Глубина прокола составляет не более 2 см.
- Введение через иглу специальной кварцевой нити, являющейся светодиодом.
- Выставление иглы, через которую будет проходить луч лазерного излучения.
- Подача лазерного луча, который нагревает мягкие структуры грыжевого образования. Температура достигает 70°.

Под воздействием высокой температуры хрящевая ткань диска испаряется и размер грыжи уменьшается благодаря ее вытягиванию. Все операция проходит под постоянным контролем рентгена или компьютерной томографии.
Возможные последствия
Осложнения после вапоризации с помощью лазера могут быть следующими:
- Методика дает лишь кратковременное облегчение и избавление от болевого симптома. Облегчение состояния наступает сразу, но через некоторое время боль вновь возвращается. Связано это с тем, что выпаривание тканей приводит только к устранению признаков грыжи, но не влияет на причины ее развития.
- Еще одно последствие лазерной методики – развитие в межпозвоночных дисках дегенеративных процессов. Регенерация тканей, которая активизируется во время уменьшения объема патологического выпячивания – это временный и только визуальный эффект, который достигается за счет того, что после процедуры формируется обширный отек. Как только отечность тканей уменьшается, в диске вновь начинают происходить дегенеративные процессы.
- Вапоризация приводит к постепенному разрушению хрящевых структур межпозвоночного диска. После нагревания диска он лишается большей части жидкости, что провоцирует развитие дегенеративных процессов.
- Воздействие на грыжу лазером не только дает лишь кратковременный эффект, но и ускоряет в дальнейшем процесс стремительного развития образования. В связи с этим вапоризация проводится только среди пациентов не старше 50 лет. У пожилых людей регенерация происходит крайне медленно, а процесс разрушения дисковых структур протекает намного быстрее.

Диску, который подвергся вапоризации, уже невозможно будет вернуть прежнюю опорную функцию. По этой причине у пациента вновь будут появляться боли, вызванные грыжей. Не исключается и распространение болезненного синдрома на суставы, особенно если проводилась вапоризация грыжи поясничного отдела. Усиление боли будет наблюдаться при активной физической нагрузке.
Восстановление после процедуры
После проведенной операции пациент остается в больничном стационаре под врачебным наблюдением в течение 4-6 дней. В течение 1-2 недель после проведенной вапоризации категорически запрещено совершать следующие действия:
- заниматься спортом, в т. ч. плаванием;
- ездить на велосипеде;
- долго сидеть;
- длительное время находиться в позе, подразумевающей нагрузку на область спины (работа в саду, огороде).
Пункционные методы лечения межпозвоночных грыж
Радиочастотная нуклеотомия и лазерная вапоризация – разновидности малоинвазивных хирургических вмешательств. Предназначены для удаления грыж межпозвоночных дисков и лечения остеохондроза. Возникновение новых технологий и усовершенствование уже существующих позволило сделать подобные операции более доступными для пациентов.



Мягко, приятно, нас не боятся дети




Мягко, приятно, нас не боятся дети

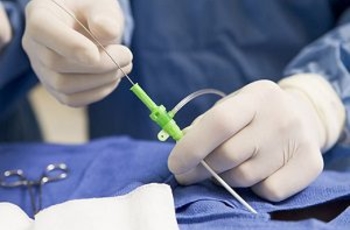
Актуальность лечения остеохондроза и грыж межпозвоночных дисков в настоящее время общеизвестна. Заболевание поражает людей трудоспособного возраста, вызывая социальные и экономические проблемы. Большинство специалистов склоняются к дискогенной природе возникновения патологии, так как именно хрящевые ткани диска поражаются в первую очередь и уже вторично страдают остальные структуры позвоночного столба и нервная система.
Современные представления об этиологии и патогенезе возникновения позвоночных грыж дают право сделать вывод, что при терапии заболевания целесообразно воздействовать на первоисточник болезни (межпозвоночный диск).
Консервативные методы лечения грыжи не всегда оправдывают надежды пациентов и врачей на свою эффективность. Это послужило основой для развития малоинвазивных техник оперирования и возникновения пункционного удаления грыжевого выпячивания. Подобные методики надежно заняли свое место между классической терапией и хирургическим вмешательством. Безусловно, их эффективность намного выше, когда операции проводятся на ранних стадиях заболевания межпозвоночных дисков.
Пункционные малоинвазивные операции так же, как и классические методы хирургического вмешательства, предусматривают технически одинаковый доступ к межпозвонковому диску. Как правило, это задний или заднебоковой, в шейном отделе может применяться передний.
Далее используются различные виды воздействия на пульпозное ядро диска:
- механические (фенестрация и декомпрессия, нуклеотомия и нуклеоэктомия);
- физические (лазерная вапоризация, радиочастотная деструкция);
- химические (хемонуклеозис, дерецепция).
Принцип методики заключается в разрушении и удалении части пульпозного ядра, склерозировании и фиброзе стенок фиброзного кольца, после чего в диске образуется отрицательное давление, которое втягивает назад грыжевое выпячивание. По этой же причине пораженный диск уже не может сместиться, устраняется опасность прогрессирования болезни и образования секвестров, следовательно, это своего рода профилактика заболевания.
В последнее время широкую распространенность получила лазерная вапоризация. Это объясняется возникновением и усовершенствованием полупроводниковых лазеров с высоким уровнем выходной мощности, что позволило одновременно снизить себестоимость лечения позвоночных грыж. Современные малогабаритные хирургические лазерные аппараты просты в использовании и могут работать от отечественной бытовой электросети.
Показания и противопоказания
Перед началом лечения пациенту проводится комплексное обследование, состоящее из:
- визуального осмотра ортопеда, невролога, нейрохирурга;
- лабораторных анализов;
- рентгенографии патологического участка, МРТ и КТ исследований, при необходимости миелографии с контрастным веществом.
Показанием к пункционным методам лечения является:
- компрессионные и рефлекторные синдромы;
- болевой синдром, не купирующийся консервативными методами терапии;
- локальные и/или иррадиирующие боли в позвоночнике и конечностях;
- ограничение подвижности в пораженном сегменте, онемение и слабость в конечностях;
- хронический прогрессирующий характер заболевания;
- нарушение статики и биомеханики скелета;
- нестабильность или гипермобильность патологического участка.
Противопоказанием к проведению операции является:
- секвестрация грыжи;
- слишком большой размер грыжи (более 9-10 мм);
- чрезмерное разрастание краевых остеофитов;
- спондилолистез или выраженная нестабильность оперируемого сегмента;
- стеноз позвоночного канала или наличие спаек и рубцов в эпидуральном пространстве.
Радиочастотная и лазерная вапоризация
Одной из перспективных малоинвазивных техник лечения грыж межпозвоночных дисков считается внутридисковая электротермотерапия, вариантами которой являются чрезкожная радиочастотная нуклеопластика, аннулопластика и лазерная или фотонная нуклеотомия (вапоризация). В основе методики заложены принципы работы электромагнитного поля, его частотных и энергетических характеристик и его влияние на биологические ткани.
Принцип радиочастотной терапии основывается на выделении тепловой энергии при прохождении тока ультравысоких частот через хрящевые ткани. Изменения мощности токов по-разному влияют на различные типы коллагена (один из составляющих межпозвоночного диска) и рецепторы органов.
Различные режимы «разогревания» коллагенсодержащих тканей могут разрушать или наоборот восстанавливать хрящи. Возможность контролировать мощность и температуру воздействия радиоволн позволяет врачу добиваться максимального лечебного эффекта и быть уверенным в безопасности процедуры.
Импульсы лазерного излучения вызывают эффект вапоризации на площади в несколько квадратных миллиметров, что способствует снижению внутридискового давления. Кроме этого отмечается явное сжатие тканей пораженного межпозвоночного диска за счет выпаривания молекул воды.
Для проведения лазерной нуклеопластики используются хирургические лазеры с длинной волны от 980 до 1064 НМ и мощностью излучения в 15-20 Вт. Дробная экспозиция воздействия 30-50 секунд, а суммарная энергия 500-1000 кДж. Единственным недостатком установки является отсутствие термистора на конце световода и невозможность контролировать температуру разогрева в мишени и окружающих тканях.
При радиочастотной и лазерной вапоризации пульпозное ядро и фиброзное кольцо сжимаются, тем самым уменьшая размеры диска и грыжи, и, следовательно, снижая раздражение ноцицептивных рецепторов и компрессию ущемленного нервного корешка. Радиочастотные и лазерные аппараты с регулирующейся мощностью и частотой волн могут применяться и в онкологической практике для создания ожога или разрушения опухолей.
Проведение операции
Все манипуляции на позвоночнике проводятся под местным наркозом, заднебоковым доступом и под контролем флюороскопического оборудования. В пораженный диск вводится канюля, через которую спускается радиочастотный спиральный зонд или лазерный световод. При радиочастотной нуклеопластике зонд укладывается по внутренней поверхности фиброзного кольца и направлен в зону грыжевого выпячивания. Затем проводится температурное воздействие по необходимой программе (42-67оС), время воздействия 90-120 секунд. Длительность операции составляет 20-30 минут.
При лазерной вапоризации световод помещают в центр пульпозного ядра и проводят воздействие в импульсном непрерывном режиме на протяжении 30-50секунд с мощностью волн 15-17 Вт. Для лечения спондилоартроза лазерный зонд вводится непосредственно в сустав или суставную капсулу.
Максимальная длительность воздействия на пораженные ткани составляет не более одной минуты, а время проведения операции не более 25-30 минут. Во время проведения процедуры (радиочастотного или фотонного воздействия на диск) и некоторое время после пациент может ощущать чувство тепла в позвоночнике и/или в какой-либо из конечностей.
В послеоперационный период пациентам рекомендуется соблюдение постельного режима в течение 2-3 часов, далее следует активация с ношением жесткого или полужесткого корсета сроком до 10 дней. В первые дни после вмешательства (2-3 дня) назначаются ненаркотические анальгетики, противоотечная и десенсибилизирующая терапия. Со вторых суток вводится специализированная ЛФК, массажи, плавание, позволяющие восстановить объем движений и мышечный корсет тела.
Сравнительная характеристика методов
Клинические наблюдения и испытания нейрохирургов и вертебрологов показывают, что пункционные методы лечения остеохондроза и позвоночных грыж достаточно эффективны и значимы. Оценивая две вышеизложенные технологии можно подчеркнуть:
- Оба метода являются малотравматичными для позвоночных структур и при соблюдении всех правил техники выполнения, тщательности и безукоризненности проведения манипуляций практически не имеют осложнений и побочных эффектов.
- Радиочастотное воздействие более безопасно, так как существует возможность мониторить температуру внутри диска до, после и во время операции, а также избегать пагубного влияния температуры на фиброзное кольцо, спинномозговые корешки и кровеносные сосуды, расположенные в позвоночном канале. При лазерной вапоризации разогрев тканей не контролируется, и возрастает риск ожога хрящевых тканей диска и близлежащих мягких.
- Радиочастотная нуклеопластика основывается на изменении структуры коллагена, что делает возможным применять ее неограниченное число раз на одном и том же пораженном межпозвоночном диске. Лазерное вмешательство при рецидиве болезни крайне нежелательно использовать повторно во избежание развития осложнений.
- Разработка новейших хирургических технологий позволяет сделать нуклеопластику и вапоризацию еще более безукоризненными операциями, которые показывают отличный результат.
Секвестрированные и фораминальные грыжи
Хотя секвестрация грыжи межпозвоночных дисков является противопоказанием к поведению малоинвазивных операций, существует ряд удачных опытов на эту тему. Перед операцией пациенту вводилось контрастное вещество, которое определяло место расположения секвестра, и взаимодействие его с прочими костными структурами. Через 5 минут производили лазерную вапоризацию.
Изначально световод устанавливался в задних отделах диска и максимально близко к секвестру. Далее подавалось лазерное излучение суммарной дозой в 1600-1800 Дж. В ходе вапоризации размещение зонда несколько раз менялось: сначала он продвигался в сторону центра пульпозного ядра, затем ближе к секвестру (между задним краем замыкательной пластины позвонка и секвестром). Таким образом, контрастная миелография позволяет достаточно точно пунктировать секвестрированные грыжи.
Фораминальные или латеральные грыжевые выпячивания – это образования, располагающиеся внутри межпозвоночных отверстий и прилегающие к нему как изнутри, так и снаружи. Чаще всего фораминальные грыжи формируются в поясничном отделе позвоночного столба, и их диагностика и лечение достаточно затруднительны.
Это объясняется тем, что на поясничном уровне они представляют собой корешковые каналы протяженностью 1,5-2 см и в сочетании с массивностью суставных отростков остаются незамеченными при исследовании, а также малодоступными для манипуляций.
Вапоризация фораминальных грыж, как правило, проводится под флуороскопическим контролем. Это дает возможность контролировать нахождение конца световода в межпозвонковом диске (до 1 мм) и максимально точно продвигать его к позвонковому отверстию и основанию грыжи.
После лазерного воздействия на центр студенистого ядра, суммарной нагрузкой в 600-700 Дж, зонд продвигается к межпозвоночному отверстию, где длительность импульсов снижается до 0,5 с (чтобы избежать термического повреждения нервного корешка) и вапоризация продолжается. Общая суммарная лазерная нагрузка при этом не превышает 1600 Дж.
В некоторых случаях во время проведения операции пациенты ощущали распространение тепла в позвоночнике и пораженной конечности в сочетании с обострением болевого синдрома. Скорее всего, этот феномен объясняется термическим воздействием на спинномозговой корешок, но к концу вапоризации боль существенно стихала или полностью исчезала. Таким образом, радиочастотная нуклеопластика и фотонная вапоризация – значимая альтернатива консервативным методам лечения позвоночных грыж, а также открытым хирургическим вмешательствам.
Лечение грыжи позвоночника лазером
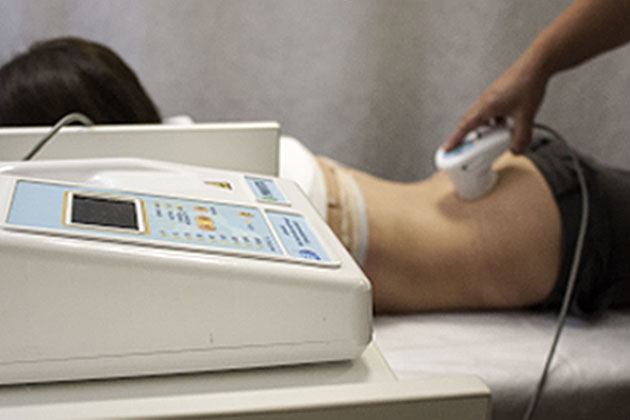
Межпозвоночная грыжа лечение лазером без операции — методы и аппараты для лечения. Можно ли лечить грыжу межпозвонковых дисков в домашних условиях? Какой аппарат выбрать для лечения грыжи позвоночника лазером в домашних условиях?
Методы лечения грыжи позвоночника лазером
Огорельцев Д.В., Центр традиционной медицины “ОРФЕЙ”, г. Ижевск. Благодаря комплексному подходу с использованием методов лечения межпозвоночной грыжи лазером 12 человек избежали оперативного лечения при грыже дисков с радикулопатией на фоне остеохондроза позвоночника с выраженным болевым синдромом и грубыми ортопедическими нарушениями. Все они были обследованы в условиях нейрохирургических отделений республиканских больниц с проведением ядерно-магнито-резонансной томографии и последующего консервативного лечения в течение 4-6-8 месяцев. Из них 7 чел. отказались от второй группы инвалидности, 3 чел. трудоустроены, одному человеку определена вторая группа инвалидности, но болевой синдром и ортопедические нарушения у него уже не выражены. Все они прошли по 5-7 курсов лечения грыжи позвоночника лазером, и за три года наблюдения рецидивов с интенсивными болями у них не возникало.
Р.А. Бодрова и Д.К. Рафикова показали эффективность комбинированного лечения грыжи позвоночника лазером и КВЧ больных с пояснично-крестцовой радикулопатией. Под наблюдением находились 75 пациентов с поражением пояснично-крестцовых корешков, обусловленных грыжами межпозвоночных дисков на уровне L4-L5 , L5-S1 в возрасте от 32 до 69 лет с длительностью заболевания от 3 до 15 лет. На фоне стандартного комплекса лечения также проводилась КВЧ и лазерная терапия на пояснично-крестцовый отдел позвоночника паравертебрально и по ходу иррадиации болей.
Ведутся работы по изучению возможности клинического применения метода пункционной лазерной декомпрессии при лечении больных с грыжами межпозвонковых дисков пояснично-крестцового уровня. Суть метода заключается в селективном нагреве лазерным излучением самой грыжи, результатом чего является снижение ее плотности, уменьшение компрессии корешка и регресс неврологической симптоматики. Применяют либо диодный лазер с длиной волны 970 нм и мощностью 3–4 Вт, либо волоконный эрбиевый лазер с длиной волны 1560 нм и мощностью до 5 Вт. Однако некоторые технологические сложности (например, контроль положения световода) не позволяют пока этой методике в полной мере реализоваться на практике.
В домашних условиях и по назначению врача можно самостоятельно проводить магнито-лазерную терапию импульсным инфракрасным лазером. Основными зонами воздействия при лечении грыжи позвоночника лазером являются паравертебральные (околопозвоночные) зоны позвоночника на уровне поражения. Дополнительно проводится освечивание лазером позвоночных сегментов выше и ниже пораженного участка.
Какой аппарат выбрать для лечения грыжи позвоночника лазером в домашних условиях?
Здравствуйте! Подскажите, пожалуйста, для лечения грыжи позвоночника (дочери 34 года) какой аппарат лучше приобрести? Заранее благодарна.
Здравствуйте. У меня диагноз – межпозвоночная грыжа. Врачи прописали лазерную терапию в комплексе с лечебной физкультурой. Собираюсь приобрести у вас МИЛТА Ф-5-01, чтоб делать это самому. Но не понимаю, как определиться с мощностью, 5-7 Вт или 7-9 Вт? У вас в описании товара сказано, что 7-9 Вт дает возможность быстрее получить лечебный эффект. Отличия только в этом? Или же есть какие-то еще отличия и рекомендации по применению, например, в частности, с моим диагнозом? Спасибо.
Аппараты лазерной терапии производятся с 1980-х годов и выпускались мощностью 4-5 Вт. По мере накопления статистических данных при лечении разных заболеваний, стало ясно, что этой мощности недостаточно при лечении ряда заболеваний, в частности лечения межпозвоночной грыжи лазером. Это связано тем, что более плотные структуры имеют более сильный коэффициент отражения и преломления лазерного луча и меньшую степень поглощения. Чтобы получить терапевтический эффект требуется более продолжительное время воздействия, что не всегда хорошо.
Аппараты большей мощности глубже и быстрее проникают в биоткань, быстрее оказывают клеточную активацию, скорее вызывают обезболивающий и другие эффекты, что позволяет не затягивать процедуру. Поэтому лечение грыжи позвоночника лазером предпочтительней проводить аппаратом мощностью 9-15 Вт.
Грыжи межпозвонковых дисков: использование лазера для их вапоризации

Актуальность поисков новых способов лечения дегенеративных заболеваний позвоночника и совершенствования ставших классическими (микродискэктомия) заключается в прогрессивном увеличении заболеваемости. Затраты на лечение и реабилитацию лиц с резистентными к лечению формами дегенеративных заболеваний позвоночника очень высоки.
Боль в спине чаще всего связана с дегенеративным процессом в межпозвонковом диске [2; 3; 8], который приводит к грыжеобразованию. Поэтому манипуляции, направленные на коррекцию межпозвонкового диска, можно считать не только патогенетическими, но и этиотропными (обоснованными с позиций этиологии заболевания). Хирургическое лечение грыж межпозвонковых дисков применяется уже около 100 лет. Из метода, сопряженного с повышенной травматичностью и практически 100%-ной инвалидизацией, он эволюционировал в метод выбора при лечении большинства форм остеохондроза. В последние десятилетия особое значение отводится минимально инвазивным операциям, таким как перкутанная лазерная нуклеотомия. Популяризаторами и основоположниками лазерного направления в нейрохирургии стали австрийские нейрохирурги F. Неррnег и P. Ascher (1976, 1977). Наибольшее распространение при этом получил ниодимовый иттриево-алюминиево-гранатовый (YAG) лазер, который генерирует излучение в спектре 1,06 мкм. При такой длине волны наблюдается достаточно высокая проникающая способность, что вызывает равномерное распределение энергии излучения внутри объекта. При нагреве биологической ткани до 60-65 °С происходит коагуляция белка, до 100 °С и более – испарение внутритканевой жидкости и сморщивание ткани, т.е. уменьшение ее в объеме (W.P. Ascher, 1988). При дальнейшем повышении температуры происходит карбонизация ткани [3; 6].
Удаление небольшого количества ткани диска под действием лазерного излучения (лазерной абляции), а также иные проявления других физических эффектов, возникающих в хрящевой ткани под действием лазерного излучения – термосжатие, стягивание внешних отделов фиброзного кольца и др., вызывают значительное уменьшение давления на окружающие анатомические структуры и, как следствие, разгрузку нервного корешка [3; 6]. Кроме того, происходит дерецепция фиброзного кольца, что также приводит к регрессу болевого синдрома.
Хирургу во время операции важно выбрать правильную дозу лазерного излучения, чтобы избежать «обугливания» ткани [1]. Не менее значимым условием эффективности лечения является равномерное распределение лазерной энергии по всему диску. Существуют различные рекомендации по проведению процедуры, которые зачастую противоречат друг другу [2; 3; 5]. Это приводит к ошибочным действиям хирурга и ухудшению результатов лечения.
Целью настоящего исследования стало изучение особенностей воздействия лазерного излучения на межпозвонковый диск при проведении нуклеотомии в эксперименте.
Материалы и методы
Статья выполнена на базе морфологической лаборатории кафедры патологии МГУ им. Н.П. Огарева на материале препаратов 40 трупов человека (в период с 2005 по 2011 год). Материал исследования получен в патологоанатомических отделениях ГУЗ «МРКБ» и МУЗ «4-я ГКБ» г. Саранска с соблюдением законодательства РФ (Харченко Т.В., Мурзакматов М.А., 2004).
Макро- и микроскопическое изучение межпозвонковых дисков человека проведено на интактном трупном материале. Возраст умерших колебался от 30 до 50 лет (41,9±6,0 лет), рост – от 160 до 180 см (171,1±6,1 см). Проводилась блок-резекция L3-S1 сегмента позвоночника с последующим разделением препарата на позвоночные сегменты L3-L4, L4-L5, L5-S1.
Межпозвонковые диски подвергнуты лазерной вапоризации под визуальным и рентгеновским контролем C-дуги (МТН-R, фирма Дорнье). Тонкое световолокно, соединенное с Nd YAG лазером («Medilas fibertom» 5100, фирма Дорнье), через пункционную иглу до 2,5 мм в диаметре вводилось в диск. В дальнейшем по этому волокну передавалось лазерное излучение. Облучение проводилось в импульсном режиме. Мощность одного импульса 15 Вт, длина импульса 1с с секундным перерывом. Эти характеристики идентичны тем, что применяются в практической медицине при операциях на поясничном отделе позвоночника.
Через пункционную иглу косвенно можно оценивать изменения, происходящие в диске. Так, при коагуляции белка (60-65 °С) можно ощутить характерный запах «вареного мяса». При достижении 100 °С отмечается активное испарение жидкости (через иглу выделяется водяной пар). Если температура в диске поднимается еще выше, то на световоде можно видеть фрагменты обугленной ткани (карбонизация диска).
Проведено 2 серии экспериментов.
- Материал от 4 трупов был использован для определения глубины проникновения излучения и особенности изменения ткани в зависимости от количества потраченной энергии. Использовалось облучению мощностью от 250 до 600 Дж в одной точке.
- Большая часть препаратов (материал от 36 трупов) подверглась лазерному облучению разной мощности с целью определения оптимального дозирования в зависимости от уровня позвоночного сегмента. На дисках L3-L4 применялось излучение в диапазоне 600-1400 Дж, L4-L5 – 700-1500 Дж, L5-S1 – 700-1600 Дж. Интервал дозирования составлял 100 Дж.
Гистологические препараты из ткани межпозвонкового диска и фотографии макропрепарата выполнялись после вапоризации. Материал заливался в парафин, затем готовили фронтальные, сагиттальные и поперечные гистологические срезы толщиной от 7 до 10 мкм. Из каждого блока брали не менее 4 срезов. Окраска последних проводилась гематоксилином-эозином по стандартной методике. С гистологических препаратов на микроскопе MedMic 2 были сделаны микрофотографии цифровой фотокамерой (Nikon COOLPIX 4500). Проводилось измерение размеров диска, глубины воздействия лазера на ткань, оценивалась выраженность изменений в межпозвонковом диске после вапоризации.
Результаты и их обсуждение
При облучении диска в диапазоне от 250 до 600 Дж на расстоянии до 7 мм (5,9 ± 0,5 мм) от световода отмечалось равномерное распределение энергии, о чем можно было судить по практически равномерной гистологической картине в указанном радиусе (рисунок 1). Даже при больших дозах облучения (600 Дж) этот показатель не менялся.
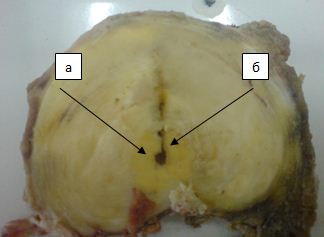
Рисунок 1. Макропрепарат. Поперечный распил межпозвонкового диска L5-S1, диск после лазерной вапоризации (350 Дж): а – место положения световода; б – область действия лазера.
Размеры нормального диска в среднем составляют 4 см в поперечнике, 4,5 см сагиттальной плоскости и около 1 см в высоту. В большинстве случаев у людей с поясничным остеохондрозом, тем более при наличии грыжи диска, отмечается снижение его высоты. Поэтому вапоризация должна выполняться в нескольких точках, иначе ближние к игле участки диска получат большое количество энергии, в то время как дальние останутся практически интактными. Кроме того, при асимметричном расположении световода по высоте возрастает риск повреждения гиалиновой мембраны, что является нежелательным исходом операции.
Минимальные макроскопические изменения начинают отчетливо появляться при подаче 350 Дж энергии на одну точку. Ткань диска становится желтой, но ее структура меняется мало (сохраняется циркулярный ход волокон и их целостность, консистенция несколько уплотняется) (рисунок 1). Микроскопически в зоне воздействия лазера отмечается лишь незначительное уплотнение матрикса за счет коагуляции тканей и единичные минимальные очаги деструкции (рисунок 2). Размельчения структур волокнистого хряща практически не происходит. За пределами указанной области (в радиусе 6 мм) ткань оставалась интактной.
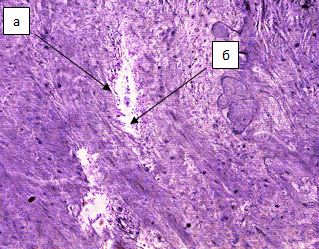
Рисунок 2. Гистологический препарат ткани пульпозного ядра в зоне воздействия 350 Дж энергии лазера, увеличение х110: а – небольшие очаги деструкции хряща; б – зоны разволокнения хряща. Окраска – гематоксилин-эозин.
Оптимальные результаты были получены при использовании энергии в 400-450 Дж на 1 точку. Макропрепарат в зоне действия лазера приобретал насыщенно желтый цвет с коричневатым оттенком и плотную консистенцию. В нескольких случаях отмечались редкие мелкие вкрапления черного цвета (карбонизация ткани). Микроскопически на фоне уплотнения матрикса отмечались небольшие очаги деструкции хряща, окруженные зонами его разволокнения. Появляются единичные «сотовые» участки в результате парообразования.
При энергетической нагрузке в 500 Дж зона «вспенивания» прилежащего матрикса становится отчетливо видна, нарушается расположение коллагеновых волокон, выявляются единичные мелкие очаги карбонизации хряща. Макроскопически диск становится светло-коричневым с мелкими очагами черного цвета. Ткань плотная. При повышении дозы лазерного облучения (550, 600 Дж) появляются радиарные разрывы хряща, заметные и на макропрепарате, и образование «сотовых» структур на отдалении, выраженное «обугливание» хряща в зоне непосредственного воздействия (рисунок 3).
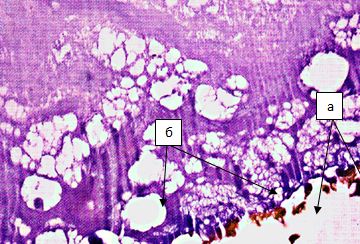
Рисунок 3. Гистологический препарат ткани пульпозного ядра в зоне воздействия 550 Дж энергии лазера, увеличение х110: а – карбонизация хряща по ходу лазерного луча; б – зона «вспенивания» прилежащего матрикса с нарушением расположения коллагеновых структур. Окраска – гематоксилин-эозин.
Во время эксперимента с оптимальным количеством энергии через иглу начинал выделяться водяной пар и ощущался запах «вареного мяса». Когда применялась энергия в 550 Дж и выше на 1 точку, уже во время проведения эксперимента можно было предположить, что ткань диска подвергается карбонизации (помимо водяного пара, из иглы отмечалось выделение более резкого запаха, а на конце световода появлялись фрагменты обугленной ткани). Таким образом, отмечалась высокая степень соответствия морфологических изменений в диске и объективных данных, получаемых во время эксперимента. Этот факт может быть использован в практической медицине для более точного подбора дозы лазерного облучения при вапоризации диска.
Для определения наиболее подходящего количества энергии лазера на каждом из исследуемых уровней мы учитывали данные первого эксперимента. Поэтому энергия подавалась не в одну точку, а в несколько (две, три или четыре). При этом в препаратах, где расстояние между рабочими позициями световода было меньше 1,1 см, отмечалось перекрытие зон действия лазера. Это сопровождалось излишним повреждением тканей в этих областях.
Согласно полученным данным, оптимальным режимом дозирования лазерной энергии на уровне L3-L4 стала подача энергии в 2 точки на расстоянии 1,5 см друг от друга, по 450 Дж на каждую. На уровне L4-L5 энергию лучше подавать в 3 точки, по 400 Дж в каждую (рис. 4), а L5-S1 – 3 точки по 450 Дж (рисунок 4).
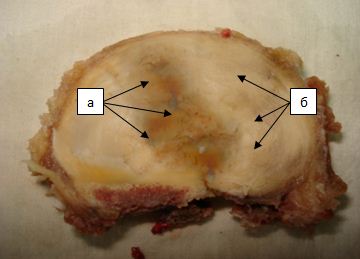
Рисунок 4. Макропрепарат. Поперечный распил межпозвонкового диска L4-L5 диск после лазерной вапоризации (1150 Дж; 3 точки приложения сверху вниз: 400Дж, 400 Дж и 350 Дж): а – область воздействия лазера; б – интактный диск.
Такие результаты объясняются особенностями анатомического строения поясничного отдела позвоночника. Межпозвонковый диск L3-L4 меньше дисков L4-L5 и L5-S1 в аксиальном, сагиттальном и поперечном размерах. Поэтому для его вапоризации достаточно осуществить процедуру в 2-х точках с оптимальным уровнем энергии, при этом зоны воздействия не перекрываются. Несколько большее количество энергии, необходимое для выпаривания диска L5-S1 по сравнению с сегментом l4-L5, объясняется тем, что у него больший диаметр (т.е. сагиттальный и поперечный размеры), поэтому и площадь зон перекрытия при работе на нем несколько меньше. Таким образом, расстояние между точками приложения лазерной энергии должно быть в пределах 1-1,5 см. Максимальное количество шагов 3.
Выводы
- Оптимальный объем энергии в одной точке при проведении пункционной лазерной нуклеотомии составляет 400-450 Дж, допустимо использование 350 и 500 Дж.
- Оптимальными режимами дозирования лазерной энергии в зависимости от уровня позвоночного сегмента являются следующие: на уровне L3-L4 – 800-900 Дж (2 точки по 400-450 Дж на каждую), L4-L5 – 1100-1200 (3 точки по 350-400 Дж на каждую), L5-S1 – 1100-1300 Дж (3 точки по 400-450 Дж на каждую).
- Во время проведения процедуры для более точного подбора дозы лазерной энергии можно использовать косвенные данные об изменениях в диске, чтобы учесть индивидуальные особенности строения и функционирования организма пациента.
Рецензенты:
- Блинов Д.С., д.м.н., зав. кафедрой общественного здоровья и здравоохранения ФГБОУ ВПО «МГУ им. Н.П. Огарева», г. Саранск.
- Плотникова Н.А., д.м.н., профессор, зав. кафедрой патологии с курсом патологической физиологии медицинского института ФГБОУ ВПО «МГУ им. Н.П. Огарева», г. Саранск.
Удаление межпозвоночной грыжи лазером
Удаление межпозвоночной грыжи лазером: цена процедуры

Иногда консервативные методы при лечении грыжи оказываются малоэффективными. В таких случаях требуется оперативное вмешательство.
Разработано множество методов хирургического удаления патологии. Но с недавних пор достойную альтернативу подобным методикам составил лазер.
В чем же преимущества лазерного удаления? Есть ли у него недостатки? Кому показано воздействие лазером? Существуют ли противопоказания к использованию лазера? Как подготовиться к операции? Как проходит лечение? Какие ограничения следует соблюдать в послеоперационный период?
Классификация лазерного воздействия

Использование лазера рекомендовано на ранних стадиях болезни (на протяжении полугода после формирования межпозвоночной грыжи), когда диаметр патологического выроста не превышает 6 миллиметров.
Лазерное воздействие производят двумя способами. Различают лазерную вапоризацию (удаление) и чрезкожную лазерную реконструкцию (лечение) грыжи.
Показания к использованию лазера

К лазерному удалению прибегают при:
- непрекращающихся сильных болях;
- покалывании (постоянном или периодическом) и жжении в области спины и шеи;
- ослаблении чувствительности;
- головных болях и головокружениях, онемении пальцев на руках (эти симптомы свидетельствуют о том, что патология локализуется в шейном отделе позвоночника);
- беременности и лактации, когда противопоказано классическое операционное вмешательство;
- отсутствии результатов при консервативном лечении.
Чрезкожная лазерная реконструкция – процедура, обеспечивающая регенерацию и рост хрящевой ткани. Она назначается при острых болях, вызванных нарушением хряща, входящего в состав диска, а также поле проведения лазерной вапоризации, чтобы избежать рецидивов.
Восстановительные процессы имеют индивидуальный характер и могут растянуться на 3-6 месяцев.
Рекомендуется сочетать воздействие лазером с массажем, иглоукалыванием, лечебной физкультурой.
Противопоказания
Противопоказаны лазерные технологии при:
- аномалиях в структуре позвонков;
- нарушении строения спинномозгового канала (наличии комбинированных стенозов);
- секвестрированной грыже;
- воспалениях в межпозвоночных дисках.
Нежелательно использовать лазер, если:
- диаметр грыжи превысил 6 миллиметров:
- пациент старше 50 лет;
- больной мало двигается.
Лазерное удаление грыжи: плюсы и минусы
В наше время известно много различных методов лечения грыжи межпозвоночного диска. Самый молодой среди них – воздействие лазером на поврежденный диск, что имеет свои преимущества и недостатки.
Преимущества использования лазера многочисленны:
- малоинвазивность;
- нет необходимости в общем наркозе;
- не требует много времени (манипуляции занимают не более часа);
- можно воздействовать одновременно на несколько участков, расположенных в любых отделах позвоночного столба;
- травмирование позвоночника сводится к минимуму;
- процедура бескровная;
- не оставляет рубцов;
- болевой синдром исчезает через 4-5 дней;
- госпитализация не превышает трех дней;
- может применяться для лечения беременных и лактирующих женщин (при традиционных методах необходим наркоз, а при воздействии лазера достаточно местной анестезии).
Но есть у этого метода и недостатки. Несмотря на то, что позвоночник почти не повреждается, из-за разрушения структуры межпозвоночного диска и сращивания позвонков существует вероятность, что прежняя биомеханика позвоночного столба не восстановится.
Все манипуляции проводят под местной анестезией. Конечно, в некоторых случаях это может быть полезно (например, при аллергии на некоторые медикаменты, беременности, кормлении грудью), но пациент при поведении манипуляций может ощущать дискомфорт.
К тому же пока еще не полностью изучены возможные осложнения. Лазер для лечения и удаления грыжи применяется недостаточно продолжительное время, чтобы можно было судить о рецидивах.
Многие пациенты жалуются, что через некоторое время после лазерного воздействия болезнь возвращается. Но подобная ситуация может быть вызвана несоблюдением предписаний врача в период реабилитации.
К тому же если вы решитесь на удаление межпозвоночной грыжи лазером, цена окажется достаточно высокой. Но все же она ниже, чем стоимость операционного лечения.
Подготовка к лечению

Перед проведением как к лазерной вапоризации, так и к чрезкожной лазерной реконструкции, пациенту потребуется пройти стандартное исследование, которое включает:
- компьютерную томографию позвоночника;
- электрокардиограмму;
- общий анализ крови и мочи;
- анализ крови на сахар.
При необходимости врач направит на дополнительные обследования.
Также понадобится записаться на прием к нейрохирургу, терапевту и анестезиологу.
Как проходит лазерная вапоризация?
Удаление межпозвоночной грыжи лазером производится в несколько этапов. Сначала делают местное обезболивание. Затем прокалывают кожный покров и вводят иглу необходимого диаметра в пораженный межпозвоночный диск. К диску подводят гибкий световод, служащий для подачи энергетического потока. Под воздействием лазерного луча жидкость, заполняющая диск, переходит в парообразное состояние и испаряется, проходя через иглу.
В результате операции уменьшаются размеры грыжи, понижается давление внутри диска, что приводит к мгновенному исчезновению болевого синдрома. При этом облучение сводится к минимуму.
Этапы лазерной реконструкции
Технология лазерного лечения несколько отличается от методов лазерной вапоризации. Сначала, как и при удалении грыжи, делают местное обезболивание. Затем к месту локализации патологии через иглу внедряют лазерный кабель. Он нагревает диск до 60-70 градусов, но не повреждает его структуру.
Реабилитационный период

Чтобы закрепить полученный результат, минимизировать риск появления послеоперационных осложнений и предотвратить рецидивы, после лечения межпозвонковой грыжи следует строго придерживаться рекомендаций лечащего врача на протяжении всего периода реабилитации, занимающего 1-2 месяца.
Первые сутки придется провести в стационаре. Если лечащий врач решит, что состояние пациента неудовлетворительное, он продлит время госпитализации.
Обязательно следует принимать назначенные доктором противовоспалительные лекарства.
На пару месяцев придется отказаться от занятий спортом и ограничить физические нагрузки.
После окончания реабилитационного периода придется пересмотреть свой образ жизни: избавиться от лишних килограммов, что может потребовать кардинального изменения рациона, укрепить мышечный корсет, что поможет ослабить нагрузку на позвоночник, регулярно заниматься спортом (особенно рекомендовано плавание). Существенную пользу (но только после полного выздоровления) принесут массаж и физиотерапевтические процедуры.
Если необходимо удаление межпозвоночной грыжи лазером, цена будет зависеть от уровня сложности оперативного вмешательства, а также репутации хирурга и клиники. Стоимость процедуры рассчитает доктор, учитывая степень и тяжесть болезни, возраст пациента и наличие других заболеваний.
Гигрома

Гигрома сустава запястья
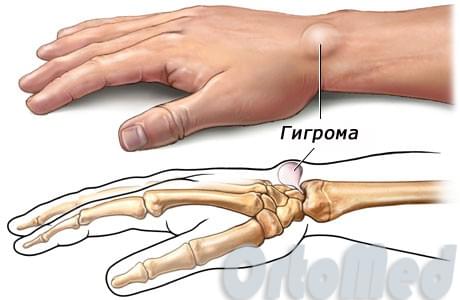
Гигрома представляет собой небольшой, грыжевой мешок с синовиальной жидкостью, который чаще образуется на тыльной поверхности лучезапястного сустава.
Это руководство поможет вам понять:
- какие структуры запястья вовлечены в процесс
- какие варианты лечения доступны
Анатомия лучезапястного сустава
Анатомия лучезапястного сустава и костей запястья является чрезвычайно сложной, вероятно, самой сложной из всех суставов организма человека. Суставы и кости запястья позволяют нам совершать разнообразные движения во всех плоскостях. В то же время, связки запястья должны обеспечивать прочность суставов.
Запястье состоит из восьми отдельных мелких костей, называемых костями запястья. Кости запястья соединяются с одной стороны с лучевой костью, с другой – соединяются с пястными костями.
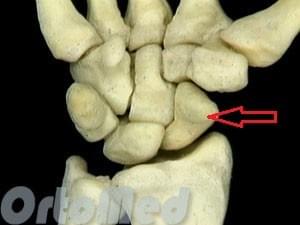
Связки удерживают все кости запястья вместе и позволяют кисти двигаться во всех направлениях. Эти связки сливаются вместе, чтобы сформировать капсулу суставов запястья. В суставе находится жидкость, называемая синовиальной жидкостью, которая смазывает суставные поверхности при движении их друг относительно друга. Почти все движения кисти передаются сухожилиями мышц сгибателей и разгибателей. Гигрома, увеличиваясь в размерах, как правило, раздвигая окружающие ткани, сухожилия, связки. Как шарик, с содержимым внутрисуставной жидкостью (гиалуроновой кислотой).
70 процентов гигром запястья образуются на тыльной стороне запястья.
Гигрома ладонной поверхности запястья или лучезапястного сустава значительно реже и обычно локализуется в проекции лучевой артерии – там где проверяют пульс.
Причины возникновения гигромы лучезапястного сустава
Основные причины появления гигромы:
- Травма лучезапястного сустава
- Большие нагрузки на кисть и лучезапястный сустав;
- Последствия операций на кисти.
- Повторяющиеся травмы, такие как игра в теннис или гольф.
Гигромы на руке образуются, когда капсула сустава истончается в следствие повреждения или дегенеративных изменений. Поврежденная ткань образует слабое месте в суставной капсуле, как слабое место на автомобильной шине, что позволяет внутреннему слою образовать грыжу. Суставная жидкость начинает выдавливать ослабленный слой капсулы, раздвигая окружающие ткани. Со временем она становится больше. Но если ограничить нагрузку на лучезапястный сустав это приведет к снижению продукции внутрисуставной жидкости и остановке роста гигромы. Описаны случаи самопроизвольного излечения гигромы после уменьшения нагрузки.
Симптомы гигромы кисти
Гигрома может появиться внезапно и резко вырасти до двух см в диаметре за пару дней или может развиваться в течение долгого времени.
Иногда пациент замечает гигрому кисти только, когда она проявит себя болью в окружающих тканях. Тем не менее каждый пациент должен понимать, что гигрома абсолютно безопасное образование. Это не опухоль и она не может переродиться в рак.
Диагностика гигромы
Как правило, осмотра врача хирурга-ортопеда достаточно для постановки диагноза.
Из дополнительных методов диагностики можно выделить УЗИ, МРТ.
Лечение гигромы кисти
Лечение гигромы запястья может быть хирургическим и консервативным. Относительные риски и преимущества какого либо метода лечения должны быть тщательно проанализированы.
Консервативное лечение
Раньше гигромы лечили просто, раздавливая их. То есть при давлении «шарик лопался», содержимое изливалось в окружающие ткани. Это абсолютно безвредная процедура. Внутрисуставная жидкость стерильна и никак не может воспалить окружающие ткани. Но 90% всех раздавленных гигром рецидивируют, т.к. края этой лопнувшей капсулы очень быстро срастаются и жидкость снова начинает скапливаться. Данный вид лечения сейчас используется только самими пациентами по незнанию.
50% гигром могут самостоятельно исчезнуть если уменьшить нагрузку на кисть и лучезапястный сустав.
Пункция гигромы
Достаточно эффективный метод, но возможен лишь на ранних стадиях заболевания, когда размер гигромы не превышает 1 см.
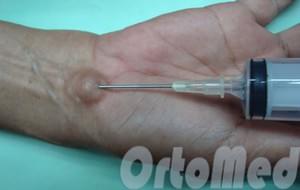
Методика:
Над областью гигромы выполняется местная анестезия. Далее гигрома прокалывается и её содержимое удаляется шприцом. Не удаляя иглы, меняется шприц и вводится склерозирующий препарат. Накладывается давящая повязка и ортез на лучезапястный сустав 5 недель, для того чтобы дать возможность слипнуться и срастись краям опустошенной гигромы.
Если пациент не будет носить ортез после процедуры, то движения в лучезапястном суставе будут провоцировать выделение внутрисуставной жидкости и неокрепший внутренний рубец не сможет противостоять давлению. Что может вызвать рецидив образования гигромы.
Поэтому одно из обязательных условий и строжайшая рекомендация – ношение ортеза.
Если гигрома более 1 см или имеет ячеистую структуру (образована несколькими мешочками), в таком случае есть показания для операции, если гигрома конечно вообще беспокоит пациента.
Хирургическое и лазерное удаление гигромы сустава
Операция проводится специалистом по хирургии кисти, который отлично знает анатомию верхней конечности, соответственно, расположение всех артерий, нервов, мышц и сухожилий. Это очень важно, поскольку сводится к нулю риск повреждения данных структур.
Операция выполняется только в том случае, если гигрома ограничивает функцию кисти, либо беспокоит пациента эстетически. Операция выполняется под местной или проводниковой анестезией.
Удаление гигромы довольно эффективный метод, но и в данном случае иммобилизация лучезапястного сустава в ортезе на 5 недель обязательное условие. Иначе риск рецидива увеличивается в несколько раз.
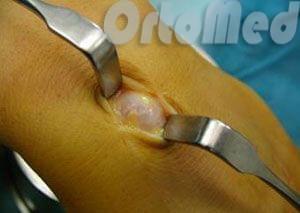
Лазерное удаление гигромы мало чем отличается от хирургического. Многие пациенты заблуждаются в том, что лазером можно удалить гигрому без разреза и рубца. Это абсолютно не так. Лазером так же происходит рассечение кожи и обнажение гигромы. И исход операции будет зависеть не от использования лазера, а от действий хирурга, его опыта. Частота рецидивов никак не связана с использованием того или иного метода хирургического лечения. Она связана с правильными действиями врача, соблюдением рекомендаций и индивидуальных особенностей организма.
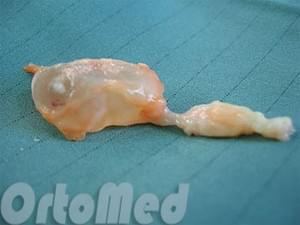
Удаление гигромы производится через небольшой доступ. Аккуратно отделяются окружающие ткани и гигрома иссекается. Но очень важный момент – это прошивание выходного отверстия, для того чтобы внутрисуставная жидкость оставалась в суставе. Рана зашивается. Накладывается стерильная повязка. Сустав фиксируется ортезом. Далее производятся ежедневные перевязки, обработка послеоперационной раны. Швы удаляются через 12-14 суток.
Безусловно, риск повторного появления гигромы есть при любом методе лечения. Но четкое выполнение вышеперечисленных рекомендаций сводит этот риск к нулю.
При возникновении болях в кисти читайте так же контрактура Дюпюитрена .


