Имплантация стент-графта при аневризме аорты и других сосудов.
Что происходит во время проведения эндоваскулярной имплантации стент-графта?
Подготовка к вмешательству
Операция по установке импланта в коронары может осуществляться в плановом и экстренном порядке. Минимальный объем подготовки допускается при экстренной медицинской помощи: ОАК, ОАМ, ПТИ (протромбиновый индекс), общая биохимия, группа крови, тропонины, ЭКГ, ФЛГ или снимок легких. В исключительных случаях операция может быть проведена до получения результатов анализов, это необходимо, чтобы не пропустить предельные 6 часов от момента приступа, и проводится у крепких, физически развитых, молодых пациентов.
Если стентирование плановое, то плюсом к клиническому минимуму проводят все назначенные врачом тесты. Обязательным исследованием перед стентированием является коронарография. Объем обследования строго индивидуален, коррелируется сопутствующей патологией, внешними и внутренними факторами.
Операцию проводят натощак, то есть прием пищи прекращается за 8 часов до вмешательства. Прием Варфарина или других антикоагулянтов-антиагрегантов нужно обсудить с врачом. Антиагреганты на основе Аспирина обычно не отменяют.
- под местной анестезией пунктируется бедренная артерия в паху или лучевая на предплечье;
- в просвет артерии вводится катетер, по которому проводится специальное устройство, облегчающее доставку необходимых инструментов, катетера с системой стент-баллон;
- по мере движения катетера к сердцу по аорте, вводят контраст (Триомбраст, Верографин), который контролируется рентгеном на цифровом мониторе и необходим для определения точной локализации бляшки атеросклероза и объема стентирования;
- на конце катетера есть специальный стент-баллон, который при достижении места установки расширяется воздухом или жидкостью до необходимого диаметра по размеру артерии, вдавливает бляшку в эндотелий и остается на нужном месте;
- все задействованные инструменты и катетер поочередно извлекаются из сосуда.
Cтент-графт предотвращает инсульт
Стенотическое поражение сонной артерии – это состояние, при котором происходит сужение
(стеноз) или полное закрытим (окклюзия) сонной артерии. У человека имеются две сонные
артерии, располагающиеся на шее. Эти сосуды приносят кровь к головному мозгу и лицу. В
иерусалимской Университетской клинике Хадасса проведен ряд исследований, показавших, что
наиболее частой причиной сужения или окклюзии сонной артерии является отложение на
внутренних стенках сосудов атеросклеротических бляшек.
Бляшка состоит из рубцовой ткани, клеток крови, холестерина и других жирных веществ.
Увеличение бляшки сужает артерию и замедляет кровоток. На бляшках могут образовываться
сгустки крови (тромбы), еще больше препятствующие кровотоку. Части тромба или
атеросклеротической бляшки, могут отделяться и стоком крови попадать в артерии головного
мозга. В результате чего происходит так называемая эмболия сосудов головного мозга,
приводящая к развитию ишемического инсульта. Окклюзия сонной артерии может привести к
развитию инсульта или внезапной быстрой смерти. Риск возрастает при наличии поражения
сонных артерий с обеих сторон.
Нарушения мозгового кровообращения.
Профилактика и лечение острых нарушений мозгового кровообращения по ишемическому типу
является наиболее актуальной задачей клинической неврологии и нейрохирургии.
инсульта составляет от 360 до 526.2 случаев на 100 000 населения в год. Инсульт уверенно
занимает первое место среди причин стойкой утраты трудоспособности. Летальность в течение
первого года после инсульта составляет – 35-38%, а в целом нарушения мозгового
кровообращения являются причиной четверти всех смертельных исходов.
Клинические проявления ишемической болезни могут быть классифицированы следующим
1. Бессимптомное (малосимптомное) течение: у пациента доминируют клинические
проявления дисциркуляторной энцефалопатии, без признаков пирамидной
недостаточности или чувствительных нарушений, указаний на перенесенные эпизоды
преходящей ишемии головного мозга или глазного яблока.
2. Больные с острыми или анамнестическими приходящими нарушениями мозгового или
3. Больные с острыми или анамнестическими пролонгированными ишемическими атаками.
4. Больные с последствиями ишемического инсульта в каротидном бассейне.
При первой стадии окклюзии единственным симптомом может быть депрессия. Наиболее
частыми симптомами являются транзиторные (т.е. приходящие) ишемические атаки, которые
иногда называются малым инсультом. Монокулярные зрительные расстройства представлены в
виде преходящей “серости”, “затуманивания”, нечеткости зрения, иногда полной слепоты.
По данным разных исследователей, Транзиторная Ишемическая Атака (ТИА) является
существенным и грозным фактором риска ишемического инсульта. ТИА следует быстро
диагностировать, поскольку промедление с установлением диагноза рискованно, ведь, как уже
указывалось выше, риск инсульта наиболее высок сразу после ТИА и составляет приблизительно
5% в течение первого месяца.
Инсульт возникает при резком снижении кровоснабжения по сосуду, питающему головной мозг,
или при его окклюзии. В зависимости от страдающего участка мозга, инсульт появляется
параличом руки иили ноги, нарушениями зрения и речи, изменениями поведения. Чем больше
поражается участок мозга, чем больше риск для жизни.
Диагностика
Ведущее значение в определение показаний к хирургическому лечению атеросклеротического
поражения магистральных артерий головы и шеи играют методы ультразвуковой и лучевой
сосудистой диагностики. Они позволяют определять характер и степень окклюзирующего
поражения, состояние компенсаторных механизмов, функциональное состояние церебральной
Ультразвуковая допплерография является ведущим методом при подозрении на окклюзионно-
стенотические поражения магистральных артерий головы и шеи. Спиральная КТ-ангиография
(СКТА) является современным неинвазивным методом комплексной визуализации просвета
сосудистого русла, сосудистой стенки паравазальных структур.
Лечение .
В университетской клинике Хаасса в Иерусалиме широко применяются различные способы
хирургической реваскуляризации мозга, которые являются составной частью комплекса мер
вторичной профилактики ишемического инфаркта мозга:
– каротидная эндортерэктомия и другие реконструктивные операции
– чрескожная транслюминальная ангиопластика со стентированием
– коррекция деформаций внечерепных отделов магистральных артерий.
Стентирование и стент .
Стентированием называется установка в суженную часть артерии стента, который представляет
собой металлическую трубочку, состоящую из ячеек. Стентирование сонной артерии является
альтернативной для хирургической эндартерэктомии сонной артерии при лечении
экстракраниального стеноза сонной артерии. Процедура стентирования предусматривает
минимально инвазивный подход, исключающий некоторые интраоперационные осложнения,
возникающие при хирургическом вмешательстве.
Стентирование сонной артерии ставит своей главной задачей устранение стеноза с
восстановлением исходного просвета артерии, а также сдерживание нарастания
атеросклеротических и тромботических наслоений. К настоящему времени стентирование все
больше широко применяется для лечения как симптомных, так и асимптомных поражений. Для
того, чтобы осуществить стентирование главных артерий шеи, врач проводит специальный зонд
катетер через бедренную артерию, аорту в собственно сонную артерию к месту сужения.
Устройство оборудовано специальным дополнительным фильтром, который автоматически
открывается во время выполнения процедуры стентирования. Обрывки разрушенных тканей и
частички атеросклеротической бляшки оседают на этом фильтре, а значит, не попадают в сосуды
мозга, а это очень важно. Раскрываясь, стент изнутри раздвигает суженные стенки артерии и
постоянно поддерживает их в расправленном состоянии. Благодаря этому восстанавливается
внутренний просвет артерии и тем самым улучшается кровоснабжение головного мозга.
Стентирование сонных артерий может выполняться с защитой или без защиты от микроэмболии
сосудов головного мозга во время операции. В конце вмешательства удаляется фильтр, баллон
(если его использовали) и проводниковый катетер. Стент остается в артерии постоянно,
поддерживая ее в раскрытом состоянии. В последнее время используются стенты с
лекарственным покрытием (например, стент с сиролимусом). После установки стента в течение
нескольких недель из него высвобождается препарат, препятствующий тромбообразованию.
В недавно проведенном в клинике Хадасса исследовании выяснилось, что покрытые
специальным лекарственным составом стенты, применяющиеся для стентирования особенно
эффективны. Лекарство постепенно выделяется в кровь, постоянно разжижая ее, предупреждая
тем самым образование тромбов. Эта технология стала революцией в лечении.
Стент – графт .
Среди стент систем, используемых для эндоваскулярного протезирования сонных артерий, в 90%
случаев применяются саморасправляющиеся стенты. Эти стенты изготавляют с помощью
сложной лазерной технологии из никель-титанового сплава (нитинола), обладающего свойством
термической памяти. Нитиноловые стенты обладают низким профилем системы доставки,
высокой гибкостью, оптимальной адаптацией к форме и физиологическим изгибам артерии при
хорошей радиальной устойчивости.
Преимуществами стент-графтоф являются легкость, безопасность и точная доставка, уникальная
технология К-складывания баллона, два маркера для точного позиционирования стента.
Технология стента – тефлоновый слой между двумя ультратонкими металлическими слоями.
Благодаря полимерному покрытию стенок, стент-графт, являясь супер ригидным устройством,
позволяет стентирование извитых и труднодоступных участков сосуда.
Источники:
Понравилась статья? Подпишитесь на канал, чтобы быть в курсе самых интересных материалов
катетер через бедренную артерию, аорту в собственно сонную артерию к месту сужения.
Что такое стентирование сосудов?
Что такое стентирование сосудов?
Стентирование – это медицинская операция, основная задача которой – установить стент, то есть специальный каркас, в просвет какого-либо полого органа (сосуд, желчный проток), и тем самым расширить его до необходимых размеров. Стентирование, а также использование других внутрисосудистых технологий, таких как тромбоэкстракция и эмболизация, стали настоящим технологическим прорывом для нейро- и кардиохирургии: у нас появился шанс существенно снизить смертность от инфаркта миокарда, инсульта и других тяжелых заболеваний.
Константин Борисович Фролов, к.м.н, врач сердечно-сосудистый хирург, руководитель центра сосудистой, рентгенэндоваскулярной хирургии и малоинвазивной флебологии Первой Градской больницы им. Н.И. Пирогова
Анна Евгеньевна Удовиченко, к.м.н., заведующая отделением рентгенхирургических методов диагностики и лечения Первой Градской больницы им. Н.И. Пирогова
Метод стентирования особенно ценен при хирургическом лечении атеросклероза, заболевания, при котором на внутренней оболочке сосудистой стенки артерии постепенно вырастают холестериновые отложения (атеросклеротические бляшки). В результате, сосуд деформируется, просвет в нем сужается, нарушается кровоснабжение органа, питаемого через пораженную артерию. В зависимости от локализации артерии, страдать может практически любой орган, чаще всего – сердце, а также головной мозг, почка, нижняя конечность.
Коронарное стентирование – частный случай, при котором оперируются сосуды сердца. Характеризуется более высоким риском для пациента, так как при малейшей ошибке сосудистого хирурга возрастает риск инфаркта на операционном столе.
Что из себя представляет стент?
Это очень тонкий, гибкий и упругий металлический каркас, имеющий форму трубки и состоящий из проволочных ячеек. В ходе операции он вводится в пораженный сосуд, затем раздувается специальным баллоном (или раскрывается сам), расширяется, вжимается в стенки сосуда и увеличивает просвет.
Стенты изготовляют из особого сплава, совместимого с органами и тканями человека и достаточно гибкого, чтобы подстроиться под состояние пораженного сосуда.
Диагностика
Чтобы подтвердить диагноз, пациенту назначается коронарная ангиография – малоинвазивное исследование, позволяющее с точностью определить степень сужения коронарных сосудов, точную локализацию сужений и их характер. Для этого по специальному катетеру через лучевую или бедренную артерию вводится контрастное вещество (препарат на основе йода), которое с током крови заполняет коронарные артерии и позволяет при помощи рентгеновского аппарата рассмотреть все имеющиеся деформации и сужения сосудов.
Снимки делаются под несколькими углами, результат выводится на монитор, а затем архивируется.
Ход операции
Стентирование проводится преимущественно эндоваскулярным методом – то есть, без разреза, через небольшой прокол на коже пациента. Далее все действия проводятся через сосуды при помощи специализированного, очень тонкого и маневренного оборудования. Ход операции контролируется при помощи рентгеновского излучения.
Поскольку стентирование – это рентгенассистированная операция, проводится оно только в специально оборудованной операционной. Такие операционные есть в ряде стационаров, подведомственных системе ДЗМ.
Операция проводится под местным обезболиванием; пациент находится в сознании, он может говорить, сообщать о своем самочувствии, при необходимости выполняет просьбы врача (задержать дыхание, делать вдох и т.д.).
Через небольшой кожный прокол в сосуд пациента вводится специальный инструмент – интродьюсер. Через него проводится тонкий металлический проводник, снабженный баллончиком, на котором установлен сжатый стент. Введенный баллочник раздувается, расширяя стент и вдавливая его во внутреннюю стенку сосуда. После этого баллон сдувается и удаляется из артерии через тот же прокол вместе с проводником и катетером. Иногда, если участок поражения сосуда велик, используется несколько стентов. Существуют также самораскрывающиеся стенты, которые раскрываются в месте сужения за счет «памяти формы».
Баллонная ангиопластика может выполняться как самостоятельная процедура или дополнять стентирование (как правило).
Противопоказания
Абсолютным противопоказанием к стентированию и другим эндоваскулярным процедурам мргут служить:
непереносимость йода (он входит в состав рентгенконтрастных препаратов);
почечная недостаточность (контрастные препараты могут усугубить ее).
Также есть целый ряд относительных противопоказаний, которые, к счастью, несут временный характер. Иными словами, к плановому стентированию можно подготовиться, стабилизируя какие-либо заболевания, вылечив инфекции, улучшив показатели крови (проводить эндоваскулярные операции запрещено пациентам с тяжелой формой анемии, а также в случае, когда нельзя назначить антитромбоцитарную терапию).
Роль доступных рентгенхирургических операций для пациента
Чтобы понять значение малоинвазивных эндоваскулярных операций для каждого пациента, мы можем провести сравнение открытых и эндоваскулярных операций на сосудах.
Открытые операции на сосудах
Ангиография (подробности, точность, визуализация и т.д.)
Общий наркоз или спинальная анестезия.
Местное или в сочетании с медикаментозным сном.
Средняя продолжительность операции
Может быть очень разной, в зависимости от сложности ситуации
От 20 минут до 2 часов, однозначно короче открытых операций шп тьщь
Время восстановления (до выписки)
Все осложнения, свойственные любым открытым операциям
Гематома в месте пункции сосуда; очень редко – инфаркт, нарушение ритма сердца или значительное кровотечение
Срок нахождения в стационаре
Зависит от характера операции, но в любом случае не менее 7 суток
Другие параметры? Что-то еще важное
Наличие кожных швов
Как правило, нет
Необходимость приёма противосвёртывающих лекарственных препаратов в течение длительного времени
Также есть целый ряд относительных противопоказаний, которые, к счастью, несут временный характер. Иными словами, к плановому стентированию можно подготовиться, стабилизируя какие-либо заболевания, вылечив инфекции, улучшив показатели крови (проводить эндоваскулярные операции запрещено пациентам с тяжелой формой анемии, а также в случае, когда нельзя назначить антитромбоцитарную терапию).
Показания к эндопротезированию аневризм артерий
Для доступа используется небольшой разрез в бедре, в который оперирующий врач вводит гибкий проводник-катетер с размещенным внутри сложенным стент-графом. Под визуальным рентгенологическим контролем хирург продвигает катетер по артериальному руслу к месту аневризмы. По достижении места установки эндопротез выдвигается из проводника, самопроизвольно раскладывается и встает в просвет патологически измененной артерии. Специальный баллон внутри металлической сетки служит для ее более полного раскрытия и плотной установки внутри сосуда. После этого катетер и баллон выводятся наружу, место прокола ушивается сосудистым швом с установкой дренажа и закрывается тугой асептической повязкой.
Осложнения связанные с стент-графтом
- Миграция эндопротеза
- Разрыв аневризмы
- Тромбоз стент-графта
- Подтекания (эндолики) в полость аневризмы
Существует 5 типов подтеканий:
Тип I – Протекание в верхем и нижнем местах крепления стент-графта ( в области почечных и подвздошных артерий). Последний практически свободно лежит в аорте и аневризме не выполняя своей защитной функции для аневризмы.
Тип II – Ретроградный кровоток в полость аневризматического мешка из ветвей аорты таких как поясничные и нижняя брыжеечная артерия. Такой тип подтеканий возникает чаще всего и несет меньше всего рисков. Немедленного лечения не требуется, так как полость может затромбироваться и эндолик спонтанно исчезнет.
Тип III – протекание между перекрывающимися частями стента (например между основным телом стент-графта и левой ножкой) или разрыв покрытия эндопротеза.
Тип IV – протекание через стенку стент-графта из-за пористости материала покрытия. С развитием технологии изготовления стент-графтов такой вид эндоликов исчезает.
Тип V – расширение аневризматического мешка без выявленных подтеканий. Спонтанный рост аневризмы, причины которого не ясны.
Если операция эндопротезирования выполнена корректно и с хорошим непосредственным результатом, то риск разрыва аневризмы уменьшается во много раз и через год после этой процедуры сравнивается с результатами открытой операции резекции аневризмы. Через 2-3 дня после операции пациент может быть выписан домой. С учетом низкой послеоперационной летальности после эндоваскулярного метода лечения риск эндопротезирования значительно меньше, чем риск открытой операции. Поэтому в западных странах эндоваскулярным методом оперируется более 80% больных с аневризмой брюшной аорты. Однако для стойкого положительного результата пациент должен находиться под динамическим наблюдением.
Структура статьи
- Статистика и факты
- Диагностика
- Лечение
- Эндопротезирование
Очень часто пациенты не предъявляют никаких жалоб. Но если симптомы появляются, то они носят неспецифичный характер. Среди наиболее распространенных симптомов следует отметить боль в брюшной полости, спине или в области грудной клетки. Пациенты описывают эту боль по-разному: одни чувствуют умеренную или сильную боль или болезненные ощущения в средней или верхней части живота, или же в пояснице, другие – ощущают саму аневризму, как бьющуюся и пульсирующую массу в брюшной полости. Но, как отмечалось, многие могут не ощущать никаких симптомов.
Что такое коронарные стенты и зачем нужны?

Коронарный стент – это медицинское устройство, представляющее собой каркас в форме металлического цилиндра, устанавливаемый в узкие места в артерии (с холестериновыми отложениями) для их расширения, за счет чего обеспечивает нормальный кровоток.
Стенты позволяют бороться со стенозом артериальных сосудов, возникающим из-за отложения атеросклеротических бляшек. Холестерин откладывается на стенках артерий и сужает просвет, тем самым препятствует течению крови. Плохой кровоток вызывает кислородное голодание и недостаток питательных веществ в органах. Одним из нескольких способов устранения таких узких мест в системе артерий является стентирование. Установка стента показана пациенту не всегда, а только в некоторых тяжелых случаях, когда нет противопоказаний, но об этом чуть позже.
Рассмотрим алгоритм стентирования на примере сердца. Катетер, на котором зафиксирован элемент, проводится через бедренную артерию, через интродьюсер. Проводник нужно передвигать в назначенный участок, где планируется установить расширитель. Как только катетер заведен, искусственный каркас фиксируется, раздуваясь под действием баллончика, и нормализует кровоснабжение в сердечной мышце.
Стентирование / Реканализация коронарных артерий. Имплантация окклюдеров, клапанов сердца, стент-графтов в аорту.
Довольно большая группа врождённых пороков и некоторые из приобретённых пороков сердца в настоящее время устраняются с помощью малоинвазивных технологий. Маленьким детям операции проводятся под наркозом, остальным — под местным обезболиванием.
12. После операции
Вы можете быть доставлены в отделение послеоперационного наблюдения или в свою палату, где за вашим состоянием будут наблюдать. Вам могут дать кислород через маску или трубку, может также требоваться переливание крови. Вы сможете начать есть и пить, как только вы почувствуете себя достаточно хорошо. Будет проводиться обезболивание в виде инъекций, таблеток или через катетер в спине (эпидуральный). В ближайшие 1-2 дня, по мере улучшения состояния, различные трубки и катетеры, будут удалены.
- Вождение: Как правило, разрешается через 4 недели после операции. В случае сомнений проконсультируйтесь с врачом.
- Купание: Если швы сухие, можно принимать ванну/душ нормально.
- Работа: Вы можете вернуться к работе через 1-3 месяца после операции. В случае сомнений проконсультируйтесь с врачом.
- Физическая нагрузка: следует избегать поднятия тяжестей или напряжения (в том числе натуживания, сильного кашля) в течение 6 недель после операции.
















![]()
- Русский
- Українська
- English (US)
- Magyar
- العربية
- Français (France)
- Türkçe
- Tiếng Việt
- Polski
- Español
- Português (Brasil)
- Регистрация
- Вход
- Messenger
- Facebook Lite
- Watch
- Люди
- Страницы
- Категории Страниц
- Места
- Игры
- Места
- Marketplace
- Facebook Pay
- Группы
- Oculus
- Portal
- Местные
- Благотворительные акции
- Услуги
- О нас
- Создать рекламу
- Создать Страницу
- Разработчикам
- Вакансии
- Конфиденциальность
- Файлы cookie
- Выбор рекламы
- Условия использования
- Справка
- Настройки
- Журнал действий
![]()
ЧТО ТАКОЕ СТЕНТ ГРАФТ И ГДЕ ЭТО ПРИМЕНЯЕТСЯ ❓
Эндоваскулярное лечение аневризмы производится изнутри пораженного сосуда и не требует открытых разрезов. При этом применяется особое устройство: Стент-графт.
✅ Стент графт это сетчатый металлический каркас, покрытый специальным материалом, выполняющий функцию внутрисосудистого протеза (эндопротеза) мешковидно расширенного участка аорты.
По длине стент-графты соответствуют длине аневризмы, которую исключают из кровотока, а по диаметру – просвету аорты в нормальном состоянии.
Для каждого пациента стент-графт производится в индивидуальном порядке, в соответствии с размерами аневризмы.
Под контролем рентгена стент-графт, в сложенном состоянии вводится через сосуды в аорту, затем расширяется до нужного диаметра и прочно фиксируется в таком положении, формируя нормальные стенки сосуда. Будучи установленным в аорту, стент-графт герметично прилегает к ее стенкам выше и ниже аневризмы. Полость аневризмы в этом случае оказывается исключенной из кровотока.
Эта операция не требует наркоза и проводится под местным обезболиванием.
Через 10 дней прооперированный пациент может вернуться к нормальной жизни вне стен больницы.
Под контролем рентгена стент-графт, в сложенном состоянии вводится через сосуды в аорту, затем расширяется до нужного диаметра и прочно фиксируется в таком положении, формируя нормальные стенки сосуда. Будучи установленным в аорту, стент-графт герметично прилегает к ее стенкам выше и ниже аневризмы. Полость аневризмы в этом случае оказывается исключенной из кровотока.
Стентирование против шунтирования: побеждает…
Доказательная медицина только на первый взгляд упрощает жизнь: это полезно, а это нет. Любая попытка углубиться в проблему рождает сложные вопросы. Например, почему именно этот вывод делается на основании этих исследований? И насколько мой конкретный случай сопоставим с имеющейся доказательной базой? И какова вообще логика? Чем можно объяснить имеющиеся данные? Ведь человеческий мозг лучше всего оперирует не мозаикой плохо связанных фактов вроде таблиц с классами рекомендаций и уровнями доказательств, а логическими структурами: это так, потому что.
Например острый коронарный синдром с элевацией сегмента ST. Название маскирует суть. Более логично было бы это назвать, скажем, так: острый коронарный синдром, обусловленный окклюзией крупной субэпикардиальной коронарной артерии. На мой взгляд, это название упрощает сразу понимание и патогенеза, и диагностики (ведь может быть не только элевация ST при таких окклюзиях), и лечения этого синдрома.
Есть много «ила, тины и мутной воды» в теме реваскуляризации при стабильной ишемической болезни сердца. Мне попался очень изящный обзор на эту тему, который, кроме перечисления имеющихся фактов, увязывает их в симпатичную логичную парадигму.
В этой статье я приведу мой сокращенный перевод источника. Кое-что я перепроверил и изложил глубже.
Источник: Doenst T, Haverich A, Serruys P, Bonow RO, Kappetein P, Falk V, Velazquez E,
Diegeler A, Sigusch H. PCI and CABG for Treating Stable Coronary Artery Disease:
JACC Review Topic of the Week. J Am Coll Cardiol. 2021 Mar 5;73(8):964-976.
В идеале, лечение при ИБС должно:
– предупреждать стенокардию
– предотвращать инфаркт миокарда
– предотвращать преждевременную смерть
Есть три доступных подхода лечения ИБС:
1. медикаментозное лечение уменьшает частоту и тяжесть стенокардии, более или менее предотвращает рост атеросклеротических бляшек и вероятность коронарной окклюзии
2. чрезкожные вмешательства ориентированы на стенотические поражения, существенно лимитирующие коронарный кровоток
3. коронарное шунтирование
Проведено много исследований-сравнений эффективности этих подходов. Эти исследования дают такие выводы:
– чрезкожные вмешательства независимо от типа используемых стентов не дают снижения вероятности инфаркта миокарда и не влияют на выживаемость; они вызывают симптоматическое улучшение
– коронарное шунтирование, напротив, снижает вероятность инфаркта и повышает выживаемость
Наша стратегия использования реваскуляризации основывается на наличии коронарных стенозов, существенно лимитирующих кровоток.
Чрезкожные вмешательства могут убрать только существенный коронарный стеноз.
Однако инфаркт миокарда часто связан с атеросклеротическими бляшками небольшого размера, не способными вызвать существенный стеноз и, подчас, не заметными при коронарографии. Разрыв такой бляшки и острый локальный тромбоз ведет к окклюзии артерии и ИМ. При этом не имеет никакого значения тот факт, что этот же пациент успешно стентировался, скажем, две недели назад и убрал один (два, три, четыре, не важно) коронарных стеноза. Новая окклюзия обнулила значение проведенной процедуры.
Коронарное шунтирование создает коллатераль, которая не только сводит на нет значение существующего локального коронарного стеноза, но и любой окклюзии проксимальнее места впадения коронарного шунта. Иными словами, если шунтированная артерия закроется в любом месте до места впадения шунта, зависимая от нее область миокарда будет получать достаточно крови через шунт и инфаркт не произойдет. Коронарный атеросклероз мигрирует из проксимальных отделов коронарных артерий к дистальным. Иными словами, наличие стенозирующих и окклюзирующих атеросклеротических бляшек более вероятно в начальных отделах коронарных артерий, которые и защищены шунтами.
Итак, коронарное шунтирование не только убирает ишемию, но и создает коллатерали.
Поэтому коронарное шунтирование снижает вероятность ИМ и повышает выживаемость. Оценочно не более чем на 50% (в среднем на 30%). Выживаемость повышается вследствие снижения риска ИМ.
Коронарный стеноз считают существенным, если он превышает 70%.
Чем более выражен коронарный стеноз, тем вероятнее он приведет к окклюзии и, возможно, к ИМ. Поэтому наличие существенных коронарных стенозов опасно.
Проблема в том, что бляшек, гемодинамически не значимых, намного больше значимых. Поэтому большая часть ИМ связана с этим множеством бессимптомных и незаметных при коронарографии поражений. Их слишком много: одна из этого множества может изъязвиться, спровоцировать локальный тромбоз и инфаркт. Количество имеет значение.
Чем больше атеросклеротических бляшек в коронарных артериях, тем опаснее. Высокая концентрация бляшек при отсутствии существенных стенозов несет в себе такой же высокий риск, как и наличие существенно стенозирующих бляшек.
Поэтому логичен вопрос: с какой стати нам вообще ожидать снижения вероятности ИМ от чрезкожных вмешательств?
Пациент с поражением одной коронарной артерии на медикаментозном лечении ИБС имеет 1,4% риск умереть в течение года.
Такой же пациент с поражением трех артерий будет иметь риск более 4% в год и более.
В исследовании The STICH (Surgical Treatment for Ischemic Heart Failure) не было разницы в выживании пациентов с ишемической сердечной недостаточностью на оптимальном медикаментозном лечении и после коронарного шунтирования через 5 лет, но была через 10 лет. К сожалению, столь длительные наблюдения за пациентами проводились не во всех исследованиях, посвященных реваскуляризирующим вмешательствам..
Множество исследований было проведено, чтобы доказать позитивное влияние чрезкожных вмешательств на выживаемость и частоту ИМ, и это продемонстрировано фактически не было. 77% исследований показали лучшую выживаемость после коронарного шунтирования. В недавно опубликованном метаанализе (Windecker S, Stortecky S, Stefanini GG, et al. Revascularisation versus medical treatment in patients with stable coronary artery disease: network meta-analysis. BMJ 2014;348:g3859.) было показано позитивное влияние покрытых стентов нового поколения на выживаемость по сравнению с медикаментозным лечением (everolimus-eluting stents и Resolute zotarolimus-eluting stents, Medtronic, Dublin, Ireland). Но прямое сравнение медикаментозной терапии с everolimus-eluting stents не показало никакой разницы в выживаемости, а сравнения Resolute zotarolimus-eluting stents, Medtronic с медикаментозным лечением вообще никогда не проводилось.
Исследование NORSTENT (Trial of Drug Eluting Stent Versus Bare Metal Stent to Treat Coronary Artery Stenosis) показало одинаковую выживаемость при использовании металлических и покрытых стентов (Bonaa KH, Mannsverk J, Wiseth R, et al. Drug- eluting or bare-metal stents for coronary artery disease. N Engl J Med 2016;375:1242–52.).
Исследования «коронарное шунтирование против стентов» показывали преимущество шунтирования независимо от типа используемых стентов.
Чрезкожные вмешательства могут ухудшать коронарную вазомоторную функцию и увеличивать риск последующего коронарного шунтирования, и чем больше стентов установлено, тем опаснее (Thielmann M, Leyh R, Massoudy P, et al. Prognostic significance of multiple previous percutaneous coronary interventions in patients undergoing elective coronary artery bypass sur- gery. Circulation 2006;114:I441–7.). Так что если нужно делать шунтирование, не следует стентировать, оттягивая время. Будет дороже и опаснее.
По сравнению с медикаментозным лечением коронарное шунтирование дало лучшую выживаемость через 10 лет.
Эффект от коронарного шунтирования нельзя предполагать на основе оценки жизнеспособного миокарда или на основании наличия ишемии. Поэтому ценность предоперационной оценки этих факторов под сомнением, поскольку шунтирование может принести пользу при отсутствии жизнеспособного миокарда (оценивается с помощью гадолиниевого контрастного кардиального МРТ) и индуцированной ишемии.<>
Четверть всех шунтов закрываются в течение года.
Существующая сегодня тенденция определять цели шунтирования на основании FFR (фракционный резерв кровотока) может привести к уменьшению количества устанавливаемых за одну операцию шунтов и в итоге снизить позитивное влияние шунтирования на выживаемость. Ведь в таком случае шунтирование проводится с целью ликвидации ишемии, но не построения мощного коллатерального кровотока.
Терминология должна быть изменена. Коронарное шунтирование оказывает не только противоишемическое действие. Оно дает кардиопротективный эффект, снижая вероятность инфаркта миокарда в последующем и связянной с ним смерти.
Коронарный стеноз считают существенным, если он превышает 70%.
Ангиопластика и стентирование
Ангиопластика — это изменение формы сосуда. Наиболее часто этот термин употребляется для обозначения процедуры, направленной на расширение суженного участка сосуда. Сосуды, несущие кислород и питательные вещества во все органы и ткани, называются артериями. Они нередко поражаются атеросклерозом, болезнью при которой стенки сосудов утолщаются, сужая просвет. Сужение артерии, или стеноз, вызывает снижение кровотока и кислородное голодание, которое называется ишемией.
Наиболее часто применяемый вид ангиопластики — это расширение баллонным катетером суженного участка сосуда механическим путем. Несмотря на то, что баллонная ангиопластика не лечит причину болезни, она очень эффективно устраняет симптомы ишемии. Но недостаток метода состоит в том, что после расширения артерия, нередко, вновь сужается из-за эластических свойств. А иногда для достижения эффективного расширения приходится прилагать усилие, вызывающее расслоение стенки сосуда. Выход был найден около 30 лет тому назад, когда в клинической практике стали применять трубчатые распорки, называемые стентами. Стент – это трубка из тонкого металла ячеистой структуры, насаживаемая на баллонный катетер. После расширения баллоном, стент вживляется в стенку сосуда.
Стенты также не лишены определенных недостатков. При внедрении в живую ткань инородного тела, а таковой является стенка сосуда, нередко возникает ответная реакция в виде воспаления. Воспаление может привести к повторному сужению просвета, но уже не из-за роста атеросклеротических бляшек, а из-за размножения клеток, выстилающих внутреннюю поверхность стента. Так бывает, примерно, у каждого третьего пациента. Повторное сужение, рестеноз, может привести к сужению, еще большему чем исходно.
Ученные долго ломали голову над проблемой рестеноза. Применяли и противовоспалительные препараты и противоопухолевые цитостатики и локальное облучение, однако, эффективного метода профилактики рестеноза не было. Выход был найден только тогда, когда появились стенты, покрытые тонким полимерным покрытием, в толщу которого внедрили препарат, подавляющий избыточное размножение клеток. Такой «сэндвич» позволил дозировано, в течение длительного времени создавать высокую концентрацию препарата в «нужном месте и в нужное время». Препараты эти давно применяют в трансплантологии для профилактики отторжения чужеродной ткани и в онкологии для подавления роста опухолевых клеток.
Стенты 4-го поколения
Что это такое и для чего его делают?
Стентирование коронарных сосудов – процедура в числе самых эффективных и малоинвазивных способов лечения ИБС при помощи установки металлической сетки на суженный сегмент венечной артерии.
Перкутанное коронарное вмешательство (ПКВ) делают пациентам с критическим сужением просвета артерий миокарда. Стентирование сосудов сердца приобрело широкое распространение из-за того, что:
- техника выполнения процедуры относительно проста;
- операция практически бескровная (в отличие от АКШ);
- не требует много времени (по сравнению с аортокоронарным шунтированием);
- для операции не нужна общая анестезия;
- малое количество осложнений;
- максимально сокращен период восстановления.
- техника выполнения процедуры относительно проста;
- операция практически бескровная (в отличие от АКШ);
- не требует много времени (по сравнению с аортокоронарным шунтированием);
- для операции не нужна общая анестезия;
- малое количество осложнений;
- максимально сокращен период восстановления.
Методы лечения
В зависимости от заболевания, возможности вмешательства могут применяться следующие виды дренирования:
- наружное, при котором отток осуществляется по внешне расположенному приемнику. Основным недостатком такого способа является необходимость вводить обратно определенное количество желчи, чтобы восполнить нужное организму количество содержащихся в ней веществ, обычно в виде таблеток;
- наружно-внутреннее, в этом варианте отток разделяется, одна его часть направляется в кишку по проксимальному каналу, вторая поступает в наружный приемник.
- внутреннее с эндопротезированием. Устанавливается биллиарный дренаж, играющий роль стента и используемый при паллиативном методе лечения неоперабельной стадии онкозаболевания.
При наружном дренировании по специальному проводнику вводят дренаж в виде трубки с его наружной фиксацией и соединением с приемником желчи. Стентирование желчных протоков при опухоли, нарушении работы желчных путей позволяет улучшить состояние пациента, снизить нежелательное появление заболеваний почек, послеоперационной почечной недостаточности.
При использовании данной методики возможны также осложнения:
- обезвоживание организма;
- сепсис;
- смещением дренажа.
Проведенные исследования показывают, что дренажные устройства, установленные до операции при нарушении деятельности желчных путей, не приводят к снижению опасности летальных исходов, не помогают пациенту облегчить его восстановление в после операционный период.
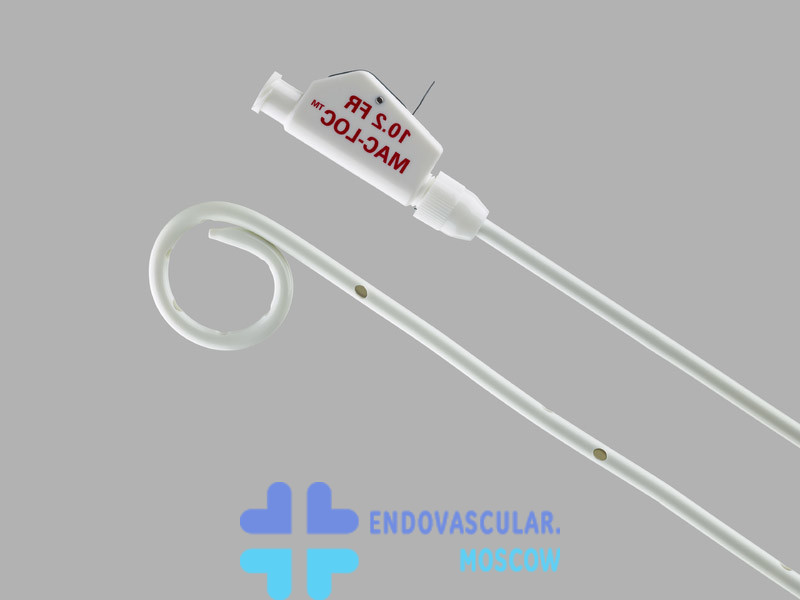
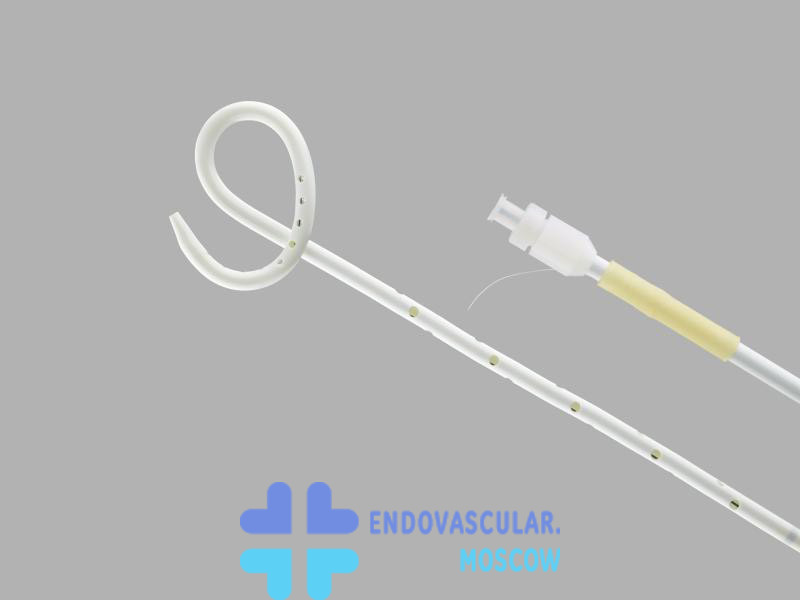
Сегодня чрескожное чреспеченочное дренирование и стентирование, эндоскопческие способы протезирования осуществляется по четко разработанной технологии без затяжной процедуры дренирования желчных путей. Данная методика помогает предотвратить побочные явления — психологические и физиологические, сопутствующие обычно таким состояниям.
При наружном и внутреннем дренировании используется катетер, предназначенный для вывода желчи, способствует задействованию проводникового элемента, проходящего через стриктуру и направляемую в дистальную область общего протока желчи или непосредственно в тракт кишечника. В области, где локализована стриктура протоков, размещается катетерное устройство, отверстия которого распределяются равномерно ниже и выше места, которое сужается. В данном варианте дренирования желчь поступает непосредственно в кишечник. Также она может направляться в специально предназначенные для этого приемник (при открытом прокладывании катетера).
Наружное введение дренажного устройства осуществляется на несколько дней с целью подготовки больного к запланированному эндопротезированию. Эта методика эффективна при длительной декомпрессии желчных протоков.
При чрезкожном введении эндопротеза в области стриктуры после введения катетера и после ЧЧХГ обеспечивается нормализация выхода желчи, попадающей в кишечник. Наиболее часто дренажная трубка находится в месте установки на протяжении 1-2 суток для проведения искусственной декомпрессии желчевыводящих путей и холангиографического контроля. Если достигнуты требуемые результаты, дренажная трубка изымается. Для эндопротезирования предназначены полиетиленовые и другие полимерные материалы, а также используются металлические эндопротезы, имеющие более длительный срок эксплуатации.
При использовании данной методики возможны также осложнения:


