Анализ крови после химиотерапии
Анализ крови после химиотерапии очень волнует пациента, но пугает не сам факт сбора крови — это делают всегда одинаково и по лабораторному стандарту, тревожит возможный результат, определяющий жизнь больного на ближайшие две недели и перспективы на следующий курс химиотерапии.
Женщины переносят химиотерапию с более выраженными осложнениями на кровь, мужской организм меньше реагирует на токсичность терапии, чему пока не нашли объяснения, и традиционно «перевели стрелку» на половые гормоны.
- Кровь после химиотерапии
- Как повысить лейкоциты после химиотерапии?
- Как повысить гемоглобин после химиотерапии?
- Как часто нужно делать анализ крови?
- Как подготовиться к анализу крови после химиотерапии?
- Противопоказания к химиотерапии
Кровь после химиотерапии
Применение большинства цитостатиков неблагоприятно отражается на кроветворении пациента, какие-то препараты убивают больше клеток крови, какие-то, как винкаалкалоиды, почти не изменяют анализа. Для каждого противоопухолевого препарата определён процент вероятности тяжелого падения лейкоцитов, но применение комбинаций лекарств, причём неоднократно на протяжении нескольких недель, отметает все прогнозы на благополучный исход — пройти химиотерапию без потерь для кроветворения.
Не все ростки крови повреждаются цитостатиками одинаково, больше всех страдают лейкоциты, не подготовленные природой к долгой жизни — срок их существования чуть меньше двух недель, а потому и нестойкие к превратностям противоопухолевого лечения.
Тромбоциты живут чуть меньше, но приемлемый уровень поддерживается большим числом — их в 30-40 раз больше лейкоцитов. Тромбоцитопения — снижение числа тромбоцитов ниже 150 тысяч развивается при использовании небольшого числа цитостатиков, к примеру, тиофосфамида, часто начинается вместе с лейкопенией, но нормализация численности тромбоцитов задерживается на несколько недель после завершения цикла химиотерапии. Критический уровень тромбоцитов 32-34 тысячи, когда существенно возрастает риск кровотечения.
Красное кровяное тельце — эритроцит должен жить почти 120 дней, только через 3-4 месяца ему на смену из костного мозга выйдет молодая клетка, поэтому он более устойчив к химиотерапии и по организму их циркулирует 2-4 миллиона. Анемия — снижение гемоглобина и числа эритроцитов характерно для очень небольшого числа цитостатиков, как правило, к ней приводят несколько циклов химиотерапии платиновыми производными. Последствия анемии фатальны — не только ухудшается качество, но снижается продолжительность жизни и меняется чувствительность к лекарственному лечению, и при глубокой анемии противопоказано проведение химиотерапии даже для спасения жизни. Особенность постхимиотерапевтической анемии в нормальном содержании железа, то есть она не железодефицитная, я связана с недостаточным воспроизводством популяции красных кровяных клеток.
Устойчивость оболочки эритроцита к внешнему воздействию, в том числе к химиотерапии, определяет скорость их выпадения в осадок, проверяемую реакцией оседания эритроцитов в пробирке за 60 минут — СОЭ. СОЭ возрастает при дефектах красных кровяных телец, химиотерапия способна деформировать эритроцит, но в большей мере от цитостатиков страдает именно воспроизводство клеток крови в костном мозге. В большинстве случаев СОЭ после ХТ изменяется относительно исходного показателя не очень сильно и часто параллельно содержанию в эритроците гемоглобина. Вопреки расхожему мнению, СОЭ мало реагирует на течение онкологического заболевания, но активно изменяется при воспалении или инфекции, нередко сопровождающих распространенную злокачественную опухоль. Высокая СОЭ часто сочетается с анемией.
Активнее всех на химиотерапию реагируют лейкоциты, составляемые пятью фракциями: нейтрофилы, эозинофилы, лимфоциты, моноциты и базофилы. Самые чувствительные к цитостатикам — нейтрофилы, в анализе крови их обозначают, как палочкоядерные и сегментоядерные лейкоциты. В норме нейтрофилов должно быть не менее 1500, то есть не меньше половины всех лейкоцитов, именно они отвечают за противостояние иммунитета воспалению и инфекции.

Снижение фракции лимфоцитов, представленных главными иммунными защитниками Т-лимфоцитами и клетками иммунной памяти В-лимфоцитами, после химиотерапии часто не явное и не столь разительное, как нейтрофилов. Выраженная лимфопения характерна для тяжелых нарушений иммунитета, ВИЧ/СПИД в том числе. После химиотерапии пациенты отмечают некоторое учащение заболеваемости вирусными респираторными инфекциями, но исследований по проблеме не проводилось, неизвестно насколько личное впечатление соответствует действительности. Предполагают, что при успешной химиотерапии злокачественной опухоли показатели иммунитета только улучшаются.
Трансаминазы крови — АЛТ и АСТ отражают не влияние противоопухолевых препаратов на клеточные фракции крови, а повреждающее действие цитостатиков и иммуноонкологических препаратов на печеночную ткань. Химиопрепараты приводят к токсическому гепатиту, а иммунные противоопухолевые лекарства — к аутоиммунному гепатиту. Гепатиты могут протекать бессимптомно и проявляться только изменением уровня трансаминаз, причём в зависимости от тяжести печеночного повреждения АЛТ может повышаться втрое и даже более чем в 20 раз превышать верхнюю границу нормы.

Как повысить лейкоциты после химиотерапии?
Лейкоциты, а именно нейтрофилы, после химиотерапии могут снизиться до критического уровня, что оборачивается тяжелыми инфекциями. Особенная форма генерализованной воспалительной реакции после химиотерапии — фебрильная нейтропения, когда ничего, кроме высокой температуры и тяжелого состояния у пациента не находят: нет объективных признаков сепсиса, пневмонии и воспалений других органов. В анализе крови не находят никакой патологической микрофлоры — всё стерильно, только нейтрофилов меньше нормы, причём процентное соотношение может сохраниться.
Нейтропения по степеням разделяется так:
- абсолютное число клеток от полутора тысяч до тысячи, что не исключает развития фебрильной нейтропении после химиотерапи, то есть однократного повышения температуры более 38,5℃ или дважды за одни сутки более 38℃
- средняя степень от тысячи до 500 клеток;
- тяжёлая нейтропения или агранулоцитоз, то есть отсутствие гранулоцитов — падение уровня нейтрофилов ниже 500.
Стимуляция лейкопоэза необходима только при фебрильной нейтропении, бессимптомное снижение фракции лейкоцитов требует коррекции только у ослабленных множественными хроническими болезнями пациентов.
Единственно эффективные препараты — колониестимулирующие факторы (КСФ), их несколько видов по преимущественной направленности на стимуляцию ростков белого кроветворения. Препараты активируют повышение рождаемости и скорость созревания нейтрофилов в костном мозге, при первичном использовании КСФ в анализе крови результат виден уже через несколько часов.
Никакие другие лекарства, кроме КСФ, не влияют на воспроизводство лейкоцитов, а только способствуют быстрому выведению депонированных лейкоцитов из костного мозга, истощая ресурсы кроветворение. На численности представителей белой крови не отражается питание пациента и какие-либо процедуры.
Использование стимуляторов кроветворения не только сопровождается неприятными побочными реакциями, но со временем тоже истощает резервы костного мозга, поэтому для КСФ определены строгие показания. КСФ никогда не совмещают с химиотерапией, препарат вводят на следующие сутки после цитостатика.
Как повысить гемоглобин после химиотерапии?
Как правило, анемия развивается после многократных курсов химиотерапии и в большинстве случаев не требует срочных мер в виде переливания эритроцитарной массы, как необходимо при обильном кровотечении.
По степени выраженности анемия бывает:
- легкой — гемоглобин на уровне 100-119 грамм на литр, как правило, на самочувствии почти не отражается, если у больного не очень распространенный раковый процесс;
- средняя степень при гемоглобине 80-99 г/л, недостаток переносимого в ткани кислорода проявляется снижением функциональных возможностей организма, возможна одышка при физической нагрузке и слабость с быстрой утомляемостью;
- тяжелой анемия становится при снижении уровня гемоглобина за 80 грамм на литр крови, главным образом, страдает самочувствие, но возможны и объективные нарушения со стороны органов сердечно-сосудистой системы.
Уровень гемоглобина повышают инъекциями эритропоэтинов, приступают к лечению при тяжелой степени. Повышение гемоглобина констатируют после нескольких месяцев лечения только у 60-70% пациентов, особенно эффективны эритропоэтины при анемии на фоне химиотерапии производными платины.

Лечение анемии длительное — несколько месяцев и часто на фоне инъекций препаратами железа. Нет однозначного понимания, меняют ли стимуляторы эритропоэза качество жизни в лучшую сторону, но использование эритропоэтина тоже сопряжено с побочными эффектами, особенно неприятное и опасное — повышение свертываемости крови с образованием тромбов. Из-за вероятности тромбозов стимулятор противопоказан пациентам с ограниченной двигательной активностью и историей тромбозов, не сочетается с КСФ и некоторыми цитостатиками.
Как часто нужно делать анализ крови?
Анализы крови — общий с лейкоцитарной формулой и тромбоцитами, а также развернутый биохимический, необходимо делать перед каждым циклом химиотерапии. При длительном цикле с еженедельными введениями препаратов уровень нейтрофилов должен проверяться накануне введения, потому что уровень лейкоцитов начинает снижаться на 7-10 дни после первой инъекции цитостатика.
Время выполнения контрольного анализа крови после химиотерапии ориентируется на исходное состояние и применяемую комбинацию цитостатиков, то есть всегда индивидуально, но не позже 5-7 дней после завершения химиотерапии. Дальнейший контроль зависит от глубины нейтропении, не исключается ежедневный мониторинг показателей. При нормализации уровня лейкоцитов следующий анализ планируется перед началом химиотерапии.
Как подготовиться к анализу крови после химиотерапии?
Для большей достоверности показателей любой анализ крови сдается натощак и лучше утром после 8-часового перерыва на еду. Перед анализом необходимо пару часов воздержаться от курения. Остальные ограничения определяются лечащим химиотерапевтом.
В анализе крови важны все показатели, отклонившиеся от нормы, потому что каждый отражает какие-то патологические изменения в организме. Ошибки в достоверности показателей возможны, но надо учитывать, что изменения в численности клеток крови не только ежедневные, но и ежечасные, костный мозг не имеет перерывов на обед и выходных, он каждую секунду трудится, рожая новые клеточки и выращивая их для выпуска в кровеносное русло.
Колебания биохимических показателей более стабильны, так как отражают состояние органов и целых систем органов, поэтому исследование делается ежемесячно, если нет повода смотреть чаще.

Противопоказания к химиотерапии
Противоопухолевое лечение токсичное по своей сути — химиотерапия убивает любые клетки, не все нормальные ткани способны противостоять цитостатикам.
В каждом клиническом случае время введения химиопрепарата и его доза определяется индивидуально, исходя из множества критериев. Формально химиотерапию нельзя начинать при уровне лейкоцитов ниже стандартной нормы, но при нейтрофилах выше 1500 не всегда есть необходимость в снижении разовой дозы химиопрепарата. И при меньшем уровне нейтрофилов возможно продолжение лечения, но при тщательном и регулярном мониторинге показателей и при наличии в резерве КСФ.
Нижняя граница начала химиотерапии для тромбоцитов — выше 100 тысяч, для гемоглобина — выше 90 г/л, в индивидуальном порядке эти пределы могут понижаться с изменением дозы вводимого цитостатика и интервалов между инъекциями. Конечно, средняя степень снижения, а тем более тяжелая —противопоказание для химиотерапии, но временное — до восстановления.
Конечно правдивость показателей, особенно в процессе противоопухолевого лечения, зависит от имеющегося лабораторного оборудования и качества реактивов, немаловажную роль играет скорость выполнения исследования. В нашей клинике любое исследование соответствует уровню экспертного заключения, иначе наши сотрудники просто не умеют работать.
Лечение после химиотерапии
Химиотерапия – один из безоперационных способов борьбы с раком. Лечение основано на введении в организм больного препаратов, которые содержат токсины и яды, сдерживающие или полностью прекращающие рост злокачественной опухоли. Химиотерапия наносит громадный урон человеческому организму. В результате воздействия ядов и токсинов повреждаются и гибнут не только атипичные клетки, но и здоровые, поражается печень, почки и другие системы. Поэтому после химиотерапии человеку необходимо лечение – комплексное, профессиональное, которое поможет справиться с побочными эффектами, пойти на поправку и полностью восстановиться.

Когда показана химиотерапия?
Решение о медикаментозном лечении онкологии принимает лечащий врач, основываясь на результатах анализов и аппаратных исследований. Как правило, к химиотерапии прибегают в следующих случаях:
- Тип рака. От разновидности злокачественной опухоли, её размеров и стадии развития зависит выбор оперативного или консервативного лечения. Химиотерапия всегда назначается после хирургического вмешательства для уничтожения оставшихся раковых клеток и возможных метастазов.
- Особенности организма пациента. Если больной раком находится в преклонном возрасте и, скорее всего, не переживёт операцию, либо по другим показаниям (опухоль локализована в недоступном для операции месте, плохое общее состояние, хронические болезни), ему назначают в качестве лечения химиотерапию. В этом случае упор делается на сдерживание роста раковых клеток и увеличение продолжительности жизни человека, больного раком.
Чаще всего медикаментозная терапия онкологии назначается для профилактики метастазирования ранее удалённых опухолей, а также лечения рака крови (лейкоз, гемобластоз) и других редких видов злокачественных новообразований (хориокарцинома, рабдомиосаркома). Также химиотерапия применяется для подготовки опухоли к операции – чтобы хирург мог её полностью удалить, не оставив ни единой раковой клетки.
Какие препараты химиотерапии для каких опухолей применяются

Это 2 группы средств консервативного лечения рака – цитостатики и цитотоксины. Первые проникают в атипичную клетку, нарушают её ДНК, запуская процесс самоуничтожения. Чаще всего для лечения используются следующие цитостатики: Гидроксимочевина, Фторурацил, Циклофосфан, препараты платины.
Цитотоксины уничтожают клетки – и раковые, и здоровые, вызывая тяжёлые побочные эффекты в организме у больных раком. Среди таких препаратов выделяют несколько групп:
- антрациклины (Дауномицин, Доксорубицин, Заведос, Фарморубицин);
- блеомицины – противоопухолевые антибиотики (Блеоцин, Бленоксан);
- митозаны (Митомицин – цитотоксический антибиотик);
- препараты таргетной терапии – лекарства направленного действия (например, Авастин блокирует рост кровеносных сосудов, которые питают злокачественную опухоль).
Больше всего побочных эффектов у цитостатиков и цитотоксинов. Поэтому лечение после химиотерапии – неотъемлемая часть процесса избавления от рака. Оно позволяет ускорить восстановление клеток организма, облегчить состояние больного и улучшить качество его жизни.
Побочные эффекты химиотерапии
Рак – тяжёлое заболевание, которое требует от пациента немалых физических и эмоциональных сил для лечения. Побочные эффекты, среди которых не только физиологические, но и психологические страдания, многих выбивают из колеи, заставляя замкнуться, отгородиться от внешнего мира. Это часто приводит к ухудшению общего состояния больных раком.
Наиболее частые побочные эффекты при лечении химиотерапией:
- тошнота, рвота, диарея/запор;
- головокружение, слабость, апатия;
- нарушение координации движений;
- алопеция (выпадение волос), повреждение ногтевых пластин;
- кожные заболевания;
- лейкопения, тромбоцитопения, эритропения;
- изменение вкусовых ощущений или полная потеря аппетита;
- заболевания ротовой полости (стоматит, мукозит);
- онемение конечностей;
- проблемы с мочеиспусканием;
- кровотечения;
- неврозы, стресс, депрессия.

Это лишь небольшая часть побочных эффектов при лечении рака химиопрепаратами. Реакция организма зависит не только от его индивидуальности, но и от применяемых средств. Если больному раком назначают для лечения лекарства таргетной терапии, то проблем с ЖКТ скорее всего не будет. У таких пациентов почти не бывает тошноты, рвоты, изжоги, поносов и запоров. Также большую роль играет предподготовка к лечению, которая позволяет провести реабилитацию большинства хронических заболеваний. Это помогает избежать их обострения после химиотерапии и быстрее восстановиться.
Лечение онкобольных после медикаментозной терапии рака
Применение лекарств для купирования злокачественного процесса имеет множество положительных моментов, за исключением одного – побочных эффектов. Однако с ними можно справиться, если своевременно начать лечение после химиотерапии рака.
Его назначает лечащий врач, опираясь на результаты последних анализов, аппаратных исследований и жалобы пациента. Лечение включает в себя:
- диету;
- иммуномодуляторы;
- симптоматические лекарства;
- психологическую помощь.
Диета в пост лечении рака
Одна из распространённых реакций организма на терапию препаратами, содержащими яды и токсины – тошнота и потеря аппетита. Отказываться от еды нельзя, потому что она даёт силы для восстановления, однако рацион пересмотреть придётся.

Основные рекомендации по питанию больных раком, которые восстанавливаются после лечения химиотерапией:
- Принимайте пищу небольшими порциями, но часто. Пригласите друзей, с ними перекусить гораздо приятнее, чем наедине.
- Включайте в рацион новые продукты (предварительно проконсультируйтесь с врачом).
- Если во рту ощущается металлический привкус, замените привычные столовые приборы пластиковыми.
Рекомендации по самому рациону касаются не только продуктов, но и приготовления различных блюд:
- Готовьте на пару или запекайте пищу в духовке. Так в ней сохранится больше полезных веществ.
- Употребляйте больше белков – индейку, куриную грудку без кожи, морскую рыбу (лучше красную), рыбью икру (любую).
- Добавьте молочные продукты – сметану, творог, ряженку, йогурт, цельное молоко.
- Готовьте салаты из зелени и овощей с использованием подсолнечного, льняного, оливкового масла.
- Введите в рацион сыр, сливочное масло, яйца, бобовые.
- В качестве перекуса используйте орехи, пророщенную пшеницу, фруктовые смузи.
- Для первых блюд готовьте крем-супы и супы-пюре, в том числе из чёрных бобов и чечевицы.
- Полезны свежевыжатые овощные, фруктовые, ягодные соки.
- В качестве гарнира употребляйте каши – гречневую, геркулес, ячневую, рисовую.
В день больному раком, который проходит лечение после воздействия химиопрепаратами, нужно выпивать около полутора литров жидкости. По этому вопросу рекомендуется проконсультироваться с врачом. Если наблюдается скопление жидкости в брюшине, лёгких или плевральной полости, её количество ограничивают.
Иммуномодуляторы в пост лечении рака
Химиотерапия для организма человека представляет сильнейший стресс. Больше всего повреждается костный мозг, отвечающий за кровь. После лечения её показатели значительно ухудшаются, показывая нехватку основных компонентов – лейкоцитов, эритроцитов и тромбоцитов, из-за чего возникают лейкопения, эритропения, тромбоцитопения.
Нехватка белых кровяных телец в организме сказывается на иммунитете – он становится настолько слабым, что больной может подхватить любую инфекцию или вирус, к которым ранее был невосприимчив. Для коррекции состояния больных раком лечение после химиотерапии всегда включает препараты-иммуномодуляторы, которые стимулируют гемопоэз (процесс кроветворения в костном мозге):
- Деринат;
- Граноцит;
- Лейкомакс;
- Глутоксим;
- Ликопид;
- Галавит;
- Нейпоген;
- Дезоксинат.

Иммуномодулирующие препараты применяются для улучшения качества жизни пациентов, больных раком. Их эффективность доказана более чем 30-летней практикой применения у онкологических больных во время химиотерапии и в период восстановления.
Симптоматическое лечение
На первом месте стоит устранение или ослабление болевого синдрома у больных раком. Для этих целей применяются анальгетики, нестероидные противовоспалительные препараты. Часто их сочетают с седативными средствами и транквилизаторами. Обезболивающие назначают по схеме от слабых до сильно действующих с постепенным нарастанием эффекта. Если боль сильная или болезнь запущена (неоперабельные стадии рака, сдерживаемые химиотерапией), врач назначает наркотические анальгетики. Однако к таким средствами прибегают только в крайнем случае и на короткий срок (до 3 суток).
Лечение расстройств ЖКТ
Первое, что делает врач – устанавливает причину состояния. Тошнота и рвота возникают не только от отравления организма больного раком при лечении токсическими противоопухолевыми препаратами. Часто это происходит в результате кишечной непроходимости – механической или динамической (отёк головного мозга, гиперкальциемия). Если ничего серьёзного не обнаружено, больному раком для лечения прописывают Церукал или Дексаметазон, если они действуют слабо, могут назначаться Зофран, Навобан, Осетрон.
Запор – один из побочных эффектов химиотерапии у особо тяжёлых больных. Здесь рекомендации врача исключительно индивидуальны. Если не стоит вопрос об оперативном лечении запора, проводят поэтапную терапию:
- Очистительная или масляная клизма (на ночь).
- Перорально касторовое или вазелиновое масло.
- Слабительное – Гутталакс, лист сенны, Бисакодил.
Диарея возникает либо как функциональное нарушение, либо как психоневрологическое осложнение после химиотерапии рака. Лечение включает в себя:
- диету;
- противодиарейные препараты (Лоперамид);
- солевые растворы для восполнения водно-солевого и электролитного баланса (Регидрон);
- лекарства, которые восстанавливают микрофлору кишечника (Линекс, Бифидумбактерин, Лактофильтрум – энтеросорбент, восстанавливающий кишечную мирофлору);
- Энтеросорбенты – активированный уголь, Диосмектит, Полифепан, Полисорб и другие.
Если анализы выявляют инфекционную природу диареи, для лечения состояния назначаются антибиотики.
Печень и почки

Оба органа участвуют в фильтрации, а потому сильнее остальных поражаются при лечении от рака. Для восстановления печени сначала нужно её очистить от скопившихся в ней вредных веществ. Для этой цели применяется Легалон – препарат на основе семян расторопши. После очищения основная задача – восстановить повреждённые химиотерапией клетки печени, чтобы орган снова заработал корректно и начал выполнять свою прямую функцию – очищать кровь от вредных веществ. Для лечения используют БАДы – Эссенциале Форте, Карсил, Флор Эссенс.
С почками несколько сложнее. Агрессивное воздействие токсических/ядовитых препаратов может вызвать мочекислую нефропатию, почечную недостаточность. Для восстановления правильной работы почек применяют:
- Нефрин, Канефрон, Хофитол, Нефрофит.
- Сборы из лекарственных трав (кукурузные рыльца, почечный чай, бурачник лекарственный и другие).
Если диагностируются воспалительные заболевания почек и мочевыводящих путей, для лечения назначаются антибактериальные препараты – Нитроксолин, Фурадонин.
Кровь
При лечении рака сильнодействующими токсичными препаратами в крови наблюдается сильная нехватка компонентов. Чтобы повысить уровень лейкоцитов, назначаются витаминные комплексы, содержащие витамины группы B, в частности B9 и 12.
Аскорбиновая и фолиевая (витамин B9) кислоты, кальций + витамин D3, магний и цинк ускорят выработку тромбоцитов. Эритроциты восстанавливаются самостоятельно. Повысить гемоглобин можно с помощью витаминов B12, B9, препаратов железа.
Психологическая помощь
Для пациентов, больных раком, свойственны стрессы и депрессия, которые загоняют человека в состояние безысходности и апатии. Это прямым образом сказывается на процессе лечения и выздоровления. Помощь психотерапевта в такой ситуации необходима. Важно найти своего врача, которому можно доверять и рассказывать о своих страхах и фобиях. Это поможет больному раком вернуться к полноценной жизни в социуме.
После каждого курса химиотерапии пациент нуждается в комплексном лечении. Выполняя все рекомендации лечащего врача, больной быстрее восстанавливается, что позволяет ему не выпадать надолго из нормальной жизни.
Клинический анализ крови: лейкопения и нейтропения после химиотерапии
Чем опасна лейкопения?
Побочные действия свойственны всем видам противоопухолевого лечения, даже если оно проводится по современным стандартам. Большая часть осложнений, в том числе и связанных с подавлением кроветворения, таких как лейко- и нейтропения, развивается отсрочено, когда пациент уже не находится в условиях стационара, а выписан под амбулаторное наблюдение.
Лейкопенией называется такое состояние, которое характеризуется снижением уровня лейкоцитов в крови.
Лейкоциты – это белые кровяные тельца. Одна из разновидностей форменных элементов крови наряду с эритроцитами и тромбоцитами.
Главная функция лейкоцитов — это защита организма от инфекций, чужеродных белков и инородных тел, способных нанести ему вред и нарушить баланс биохимических реакций.
Содержание лейкоцитов в крови не является постоянным, оно динамически изменяется в течение дня в зависимости от времени суток и функционального состояния организма. Например, уровень лейкоцитов повышается не только во время наличия какого-либо воспаления в организме, но и обычно несколько повышается к вечеру, после приёма пищи, а также после физического и эмоционального напряжения.
Но мы говорим о тех случаях, когда количество лейкоцитов снижается.
Этому всегда имеется какая-то причина, в том числе это закономерное осложнение противоопухолевого лечения.
Почему это состояние имеет для нас значение?
Лейкоциты отвечают за иммунитет и сопротивление различным неблагоприятным факторам, поэтому при снижении их уровня в крови в первую очередь страдает «оборона» организма.
В этом случае человек становится более уязвим для любой инфекции: бактериальной, вирусной или грибковой.
В большинстве случаев при развитии инфекционных осложнений специализированное противоопухолевое лечение должно быть отложено. Следовательно, помимо главной опасности для человека, которая заключается именно в инфекционном процессе, мы еще сталкиваемся и с тем, что приходится откладывать лечение онкологического заболевания на неопределенный срок до тех пор, пока мы не разберемся с инфекцией.
Почему важно знать о лейкоцитарной формуле?
Существует так называемая лейкоцитарная формула, которая формируется из подвидов лейкоцитов: моноцитов, эозинофилов, базофилов, лимфоцитов и нейтрофилов.
Каждый из видов выполняет собственную специфическую для него функцию, хотя в основе лежат именно иммунные процессы.
Когда мы получаем результаты клинического анализа крови, уровень лейкоцитов в нем может быть нормальным, но какую часть от этого общего показателя составляет тот или иной подвид, сказать навскидку невозможно. При этом для планирования системного лечения это очень важно. Именно поэтому онкологи требуют, чтобы в анализах крови было указано абсолютное число всех подвидов лейкоцитов. Обращать на это внимание должен и пациент, когда получает результаты анализов.
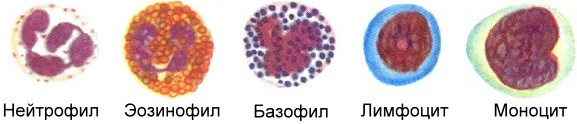
Наибольший интерес для химиотерапевтов представляют нейтрофилы. Этот подвид лейкоцитов играет очень важную роль в защите организма от бактериальных и грибковых инфекций и сравнительно меньшую — в защите от вирусных инфекций. В противоопухолевой или антигельминтной защите нейтрофилы практически не играют роли, в этих процессах участвуют другие клетки.
При проведении химиотерапии уровень нейтрофилов критично важный показатель. Если количество нейтрофилов падает ниже 0,5х10*9/л, то нормальная микрофлора, которая присутствует, например, во рту или кишечнике, может вызывать инфекции. Если количество снижается до Можно ли поднять уровень лейкоцитов и нейтрофилов?
Химиопрепараты – это токсичные вещества. К их применению существуют показания и противопоказания, потому что они могут как помочь пациенту, так и очень сильно навредить, если использовать их бездумно. Единственным подходящим и разумным методом повышения уровня лейкоцитов и нейтрофилов является ожидание.
Да, это действительно так.
Во-первых, потому что каждый организм имеет свои особенности и не всегда способен восстановиться к тому времени, которое предусмотрено рекомендациями.
Интервалы между циклами являются оптимальными, но при этом отклонение от сроков на 1-2 недели (иногда и больше, если потребуется) является допустимым, если имеются противопоказания к проведению химиотерапии.
Во-вторых, любые препараты, которые стимулируют повышение уровня лейкоцитов и нейтрофилов опасны тем, что после нескольких таких стимуляций резерв костного мозга может быть истощен, и после этого восстановление будет проходить намного дольше и будет сопряжено с возможными осложнениями.
Если лейко- и нейтропения постоянная, и организм не восстанавливается должным образом даже при увеличении интервалов между циклами, то назначаются специализированные препараты, которые должны применяться только под наблюдением врача в строго показанных ситуациях.

Любые так называемые иммуномодуляторы, стимуляторы иммунитета никакой пользы не принесут, эффекта от них не будет, потому что лейкоциты все равно будут снижаться на фоне химиотерапии, так и должно быть, но при этом такие препараты могут спровоцировать развитие нежелательных реакций.
Фебрильная нейтропения
Сочетание повышения температуры тела со снижением количества нейтрофилов носит термин фебрильной нейтропении. Это угрожающее жизни пациента состояние, внезапно и остро развивающееся у больных на фоне снижения числа циркулирующих в крови нейтрофилов ниже 0,5х10*9/л.
- количество нейтрофилов в периферической крови 9 /л;
- двукратное за сутки повышение температуры тела >38.0 0 С или однократное повышение температуры >38.3 0 С при измерении температуры во рту. Это значит, что при измерении температуры в подмышечной впадине вас и вашего врача должна начать беспокоить температура выше 37.5 0 С.
Основная проблема состоит в том, что врачам-онкологам очень трудно контролировать это осложнение и своевременно принимать необходимые меры, поскольку у большинства пациентов фебрильная нейтропения развивается в период, когда они уже не находятся в условиях стационара.
Поэтому пациент также должен быть внимателен к своему состоянию и своевременно принимать меры: связаться с врачом, как можно скорее сдать кровь и неукоснительно следовать тому, что рекомендует лечащий врач.
При повышении температуры тела выше 38.0 0 С необходимо как можно скорее сдать клинический анализ крови. Это важно! Без его результата невозможно сказать наверняка есть ли фебрильная нейтропения у пациента, нужны ли какие-либо срочные мероприятия.
Помните, что это осложнение может обернуться большой бедой, если его не распознать и не начать вовремя лечить.
Если имеет место сочетание обоих критериев (количество нейтрофилов в периферической крови 0 -38.3 0 С), необходимо как можно скорее связаться с лечащим врачом или обратиться в онкологическое учреждение по месту жительства.
В отсутствие своевременного лечения в течение 48 часов после развития фебрильной нейтропении летальный исход имеет место в 50% случаев! Даже при проведении антибактериальной терапии риск смертельного исхода сохраняется в 10% случаев.
Это говорит о том, что это очень опасное осложнение, нельзя относиться к нему легкомысленно.
Около 80 % фебрильных эпизодов на фоне сниженного уровня нейтрофилов в крови связаны с развитием инфекции, которая протекает с отсутствием классических симптомов (боль, гиперемия, отёк, жар), а основным критерием инфекционного процесса является высокая температура тела.

До последнего времени лихорадка, возникающая у больного с нейтропенией, являлась основанием для обязательной госпитализации и проведения лечения в стационаре. Однако в результате проведения клинических исследований была создана система оценки осложнений у больных с фебрильной нейтропенией. Врач согласно этой шкале считает баллы и может оценить существуют ли риски при проведении лечения амбулаторно.
Что рекомендуется делать пациентам, у которых развилось данное осложнение
1) При повышении температуры тела срочно сдать анализ крови. Сообщить лечащему врачу о результатах анализа.
При наличии критично низкого уровня лейкоцитов и нейтрофилов очередное введение химиопрепаратов будет отложено до момента полного восстановления.
2) Старайтесь придерживаться полноценного рациона, исключите сырые продукты (то есть мясо, рыбу, яйца, фрукты и овощи) – все продукты без исключения должны быть термически обработаны.
3) Соблюдайте режим работы и отдыха, не нагружайте себя, дайте возможность организму восполнить силы и энергию для скорейшего восстановления.
4) Тщательно соблюдайте личную гигиену, потому как любая инфекция может стать причиной ухудшения состояния.
5) Не посещайте места большого скопления людей без необходимости. Соблюдайте самоизоляцию. Это актуально не только во время нынешней пандемии, ведь риски присоединения инфекций во время фебрильной нейтропении колоссальные – даже ваши домочадцы могут представлять опасность, что уж говорить о большом количестве незнакомцев, например, в магазинах.
6) Если вы вынуждены посетить место с большим количеством людей, например, чтобы сдать анализ крови, то обязательно носите защитную маску. Старайтесь соблюдать дистанцию с окружающими.
К основным препаратам, которые используют при лечении фебрильной нетропении, относятся антибиотики, также используются специализированные препараты для стимуляции повышения уровня лейкоцитов и нейтрофилов – это колониестимулирующие факторы (Г-КСФ).
Эти препараты применяются для ускорения образования, созревания и выброса нейтрофилов из костного мозга в периферическую кровь, где они начинают выполнять свои функции и защищать организм.
Что следует знать пациентам о применении колониестимулирующих факторов
1) Применение Г-КСФ сразу после ХТ (в первые сутки) или на фоне ХТ строго запрещено, это может привести к развитию тяжелой лейко- и нейтропении. К сожалению, иногда такое происходит, поэтому пациенты тоже должны быть осведомлены, что так делать нельзя.
2) Применение этих препаратов должно быть прекращено как минимум за 48 часов до начала цикла химиотерапии.
3) Г-КСФ не применяются для лечения афебрильной нейтропении (то есть если уровень нейтрофилов низкий, но повышения температуры тела нет).
4) Не применяют их также при осложнениях и инфекциях, которые не связаны с нейтропенией (например, если развилась пневмония, но при этом уровень лейкоцитов и нейтрофилов в норме или повышен).
5) В некоторых случаях разрешается введение колониестимулирующих факторов с целью профилактики развития фебрильной нейтропении, если у пациента имеются факторы высокого риска развития этого осложнения. Наличие этих факторов должен перед каждым циклом химиотерапии оценивать лечащий врач.
Участие самого пациента в процессе лечения – это неоценимая помощь врачу в борьбе с онкологическим заболеванием. Когда пациент внимателен к себе, интересуется происходящим и стремится к командной работе с врачом, выполняя его рекомендации, то лечение проходит легче. И с осложнениями, которые, к сожалению, нередки, справляться тоже становится проще.
Источники литературы:
- Пристман Т. Практическая химиотерапия / Пер. с англ. Под. ред. А.М. Гарина. – М.: Практическая медицина, 2011. – 192 с.
- Корман Д. Б. Основы противоопухолевой терапии. – М.: Практическая медицина, 2006. – 512 с.
- Руководство по химиотерапии опухолевых заболеваний / Под. ред. Н. И. Переводчиковой, В. А. Горбуновой. – 4-е изд., расширенное и дополненное. – М.: Практическая медицина, 2017. – 688 с.
- Сакаева Д. Д., Орлова Р. В., Шабаева М. М. Практические рекомендации по лечению инфекционных осложнений фебрильной нейтропении и назначению колониестимулирующих факторов у онкологических больных. Злокачественные опухоли : Практические рекомендации RUSSCO #3s2, 2019 (том 9). С. 585–594.
- https://rosoncoweb.ru/calculators/febrile_neutropenia/
- (Общий алгоритм назначения Г-КСФ для профилактики фебрильной нейтропении (ФН) (на основании рекомендаций RUSSCO))
Как быстро поднять лейкоциты в крови после химиотерапии
Актуальный вопрос о повышении лейкоцитов после химиотерапии основан на их значимости для организма. Клетки крови напрямую связаны с иммунитетом, помогают защищаться от болезней. Химиотерапия неизбежно повлияет на состав крови, но исправить это представляется возможным.
Частота появления дефицита белых телец в крови распространена после курса химиотерапии, процедура способна понизить их. Возникает с вероятностью 59% у человека, проходящего лечение. Лейкопения угнетает иммунитет, растягивает терапию, увеличивает и без того высокие траты на излечение.
Влияние химиотерапии на состав крови
В норме лейкоциты содержатся в крови в составе от 4 до 9*109 на литр. Это белые кровяные тельца, отвечающие за иммунитет, уничтожают патогенных агентов. Поэтому их высокое содержание важно для организма. Если указанных клеток много в крови, говорят о хорошей сопротивляемости организма, о его быстрой способности восстановить утраты. Недостаток лейкоцитов в крови называют лейкопенией. Патология развивается от различных спортивных травм, вирусных инфекций, онкологии, других болезней. В этот период нужно всеми средствами повышать уровень лейкоцитов, от показателя зависит выздоровление.
При химиотерапии состав крови неизбежно меняется: подразумевают смещение между показателями количества всех составляющих крови (недостаток всех трёх компонентов называют панцитопения):
- недостаток лейкоцитов – лейкопения;
- эритроцитов – анемия;
- тромбоцитов – тромбоцитопения.
Падение элементов в крови не возникает немедленно. С начала курса терапии антираковым препаратом должно пройти минимум два дня. Тогда лейкоциты в крови постепенно снижаются, достигая пика на второй неделе.
Для чего нужны кровяные тельца
Кровь – жидкая подвижная субстанция, соединяющая системы органов. Циркулирует по круговой замкнутой схеме сосудов. Выполняет множество функций в организме человека. Является транспортным средством для питательных веществ. Осуществляет газообмен: переносит кислород к клеткам, удаляет углекислый газ. Кровь быстро регенерирует, так как органы кроветворения (у человека – костный мозг) создают новые элементы. В состав крови входят форменные кровяные тельца, плазма. У взрослого мужчины объём крови в среднем пять литров, у женщины – примерно четыре. Кровь на 40-50% состоит из форменных элементов, обладающих исключительными свойствами:
- Эритроциты – красные кровяные тельца. Демонстрируют зелёный цвет, только из-за присутствия в них гемоглобина окрашивают кровь в красный. Эти тельца переносят кислород от лёгких к тканям, забирая обратно углекислый газ.
- Тромбоциты – кровяные пластинки, основной задачей выступает остановка кровотечения при наличии внешнего ранения. Обеспечивают свёртываемость крови, предотвращают кровопотерю.
- Лейкоциты – белые клетки крови. Отвечают за иммунитет: распознают вирусы, борются с ними, защищают организм от чужеродных элементов. Этот процесс называют фагоцитоз. В нормальном соотношении их меньше, чем предыдущих элементов.
Лейкоциты делятся на две группы: гранулоциты (миелоциты), агранулоциты (нейтрофилы).
Химиотерапия влияет на кровь: цитостатические препараты, используемые в этом методе лечения, влияют на быстро делящиеся клетки. Они угнетают деление, за счёт этого представляется возможным уменьшить, остановить объём раковой опухоли либо полностью избавив пациента от нее, либо уменьшив до операбельного размера. Вместе с раковыми клетками под действие химиотерапевтических препаратов попадают здоровые клетки, предрасположенные к быстрому делению: волосяные фолликулы (отсюда облысение, как побочный эффект), клетки слизистой клетки кишечника, эпителий ротовой полости (появляются язвы, стоматит), кровяные клетки. Лейкопению нужно вылечить предельно быстро, так как лейкоциты через иммунитет борются с онкологией (к примеру, с РМЖ). Помимо этого, ввиду низкого иммунитета опасность представляет любое незначительное повреждение.

Последствия лейкопении
Из-за отсутствия иммунитета повышается риск:
- Организм в большей степени подвержен гепатиту, ВИЧ, туберкулёзу.
- Осложнения на верхние дыхательные пути (воспаление лёгких).
- Интоксикация организма из-за отсутствия вывода токсинов.
- Повышение вероятности гнойных процессов.
- Лейкоз (рак крови) – костным мозгом вырабатывается слишком большой объём лейкоцитов, которые не развились до рабочего состояния, это приводит к раку крови.
- Большая нагрузка на селезёнку.
Если не устранить проблему с лейкоцитами, она вызовет неприятные, непоправимые последствия.
Количество лейкоцитов в норме
Объём лейкоцитов варьируется с течением времени. Иногда они повышены. Общепринятая норма: 4-9 единиц на литр. Изменения, не вызванные болезнями, происходят в пределах нормы: при беременности уровень повышается от четырех до пятнадцати. Пожилые люди имеют несколько сниженный показатель: три с половиной – девять на литр.
- Лёгкая степень. Три с половиной – четыре единицы на литр. Выраженные симптомы отсутствуют.
- Средняя степень. Две – три с половиной единицы на литр. Защита организма теряется, опасность представляет каждый вирус, повреждение.
- Тяжёлая степень. Уровень лейкоцитов опустился ниже двух штук на литр (минимальное значение). Характерны тяжело текущие воспалительные процессы.
При химиотерапии лейкоциты падают в пять раз. Важно резко повышать их уровень для борьбы с внешними агрессорами. Для проведения диагностики нужно сдать общий анализ, говорящий о болезни, если результаты содержания лейкоцитов в моче, крови низкие.

Повышение лейкоцитов
Часть терапии после лечения антираковыми препаратами состоит в поднятии уровня иммунитета, который неизбежно нарушится. Неоспоримо, что запускание лейкопении приводит к необратимым последствиям. Человек умирает вследствие резвившегося сепсиса. Наиболее действенный способ – фармацевтический, с применением препаратов. Выработка белых кровяных телец допустима самостоятельно, потребуется придерживаться диеты. Известно множество народных способов повышения иммунитета.
Лекарства
Препараты для повышения уровня лейкоцитов подразделяют на две группы: основные, провоцирующие выработку лейкоцитов, быстро приводящие к результату после курса химиотерапии и вспомогательные. Последние защищают иммунитет, не вырабатывая лейкоциты. Побочные действия препаратов различны. Для назначения требуется помощь специалиста.
В основные препараты включают:
- Нейпоген. Стимулирует лейкоциты к выработке. Применяется как раствор для инъекций. Быстродействующий, выводится спустя сутки. Применяется: после химиотерапии; самостоятельно. Применение происходит исключительно под контролем врача, который фиксирует все изменения в лучшую, худшую сторону.
- Лейкоген. Увеличивает лейкоциты. Не слишком токсичен, выводится из организма полностью. Показания: низкий уровень белых тел в крови, как результат лучевой терапии. Противопоказан при образованиях в мозге. Назначение объёма, длительность курса подбираются врачом для пациента отдельно. В таблетированной форме. Купить возможно лишь по рецепту.
- Метилурацил. Выписывают после лечения онкологии. Характеризуется минимальным количеством побочных действий. Порождает рост, регенерацию тканей в организме. Применяется в различных состояниях, требующих усиления роста тканей. Форма выпуска различная (уколы, таблетки). Показания: гамма-терапия, антираковое лечение препаратами. Людям с лейкемией, злокачественными образованиями в области костного мозга противопоказан.
- Ленограстим. Действие направлено на костный мозг, чтобы стимулировать выработку нейтрофилов. Показания: после лечения злокачественной опухоли цитостатическими препаратами, вызывающими лейкопению. Противопоказаниями служат повышенная чувствительность к составу лекарства, миелолейкоз.
- Полиоксидоний. Форма: свечи (вагинальные, ректальные). Помогает выработке антител, повышает иммунитет, выводит токсины, соли. Противопоказан в период беременности, лактации, людям с почечной недостаточностью.
- Натрия Нуклеинат. В форме порошка, таблеток. Регулирует количество лимфоцитов. Противопоказан беременным, кормящим женщинам.
- Филграстим. Быстро стимулирует органы кроветворения. Показания: лейкоциты понижены. Используется для лучения острых инфекций. Побочные действия: мышечные спазмы, низкое артериальное давление, проблемы с выделительной системой. Проблемы у женщин, ждущих ребёнка. Не рекомендован людям с повышенной чувствительностью, с проблемами почек, печени, при лейкемии.
- Пентоксил. В виде таблеток. При лейкопении (всех степеней), некоторых других болезнях. К последствиям приёма относятся проблемы пищеварения. Нельзя при онкологии мозга.
- Пиридоксин. Препарат для обмена веществ. Участвует в образовании глутаминовой кислоты. Запрещено людям с личной непереносимостью компонентов.
- Батилол. Таблетки. Предупреждение лучевой болезни. Увеличивает эритроциты, лейкоциты. К побочным действиям относится несварение (диспепсия).
- Цефарансин. Таблетированная форма. Быстро действует, встраивается в мембраны клеток, стимулирует соединения.
- Популярны: циклофосфан, доксорубицин.
Вспомогательные лекарственные средства
К адъювантной терапии относят употребление препаратов, воюющих с опасностями самостоятельно, чтобы не тратить лейкоциты. Сюда относятся:

- антибиотики;
- противовирусные;
- жаропонижающие;
- витамины, вводимые инъекциями: B12.
Диета
К диетологическим способам увеличить лейкоциты в крови, если упали, относятся правильное сбалансированное питание, потребление продуктов, способствующих выработке. В меню обязательно входят продукты с витамином C, E, калием, Омега-3, цинком. Рекомендация: после химиотерапии нужно потреблять белок, иначе организму труднее справляться.
Продукты, повышающие уровень:
- Употреблять жидкость. Рекомендуемая норма для взрослого человека – два литра чистой воды на день. Нужно непременно кипятить её перед употреблением.
- Ягоды, фрукты, содержащие витамин C.
- Клетчатка, содержащаяся в овощах.
- Диетическое белое мясо.
- Яйца.
- Рыба, морепродукты.
- Растительные жиры: орехи.
- Злаки, крупы, бобовые культуры.
Советы: витамин A. Основной полезный витамин, необходимый выздоравливающему, его суть в увеличении лейкоцитов. Он находится в оранжевых фруктах, овощах, лососе. Витамин C для поддержания иммунитета – в цитрусовых.
К запрещенным продуктам относятся: жирная пища, копчёная, острая, консервированная. Исключение указанных блюд из организма облегчит процессы выздоровления.
Опасность при низких показателях иммунитета составляют недостаточно хорошо промытые фрукты, овощи, на которых содержатся яйца паразитов, инфекция, бактерии. Не прожаренное мясо тоже опасно. Ввиду пониженной сопротивляемости эти продукты повлекут за собой дополнительные болезни, осложнения. Поэтому важно соблюдать профилактические меры, тщательно мыть продукты, придавать их термической обработке. Следить за гигиеной рук.

Народная медицина
К традиционной медицине зачастую прибегают как к методу адъективной терапии. Именно комплексный подход поможет поднять лейкоциты после химиотерапии. Народные средства могут поспособствовать аллергии, необходима консультация дерматолога, прохождение анализов, если появляется нетипичная реакция: сыпь, аллергия, отёк. Плюсами такой медицины является отсутствие побочных эффектов, к примеру, у ребёнка, наполнение тела необходимыми для поддержания сил микроэлементами. Народными средствами это реально.
- Отвар шиповника, чтобы не падали показатели. Продукт содержит витамин C, отвар из ягод незаменим при лейкопении. Рецепт: две горсти сушёных плодов шиповника положить в термос, залить кипятком до предела. Дать настояться десять-двенадцать часов.
- Употребление за завтраком тёртой моркови, смешанной со сметаной. Полезно для поднятия элементов: повышает количество белых кровяных элементов.
- Крапива с мёдом поднимают: сто грамм высушенной травы измельчить, смешать с пятьюстами миллилитрами мёда. Пять миллилитров после пищи трижды в день.
- Быстро повысить лейкоциты в крови после химиотерапии в состоянии отвар из овса: 50 грамм неочищенного овса покрыть 400 миллилитрами воды. Дать закипеть, томить на пару четвёрть часа. Принимать по пятьдесят грамм три раза в день.
- Отвар из семян льна. Обладает свойствами повышения эритроцитов, выводит из тела токсины, оставшиеся от курса химиотерапии. Две ложки зёрен залить кипятком. Настоять, после чего употребить после полудня в объёме одного литра.
- Свёкла вызывает лейкоцитоз. Сок свёклы полезен при раковых заболеваниях. Из этого овоща готовят салаты, едят отварную, трут, пьют сок.
- Цикорий – не только заменяет кофеин, но и способствует выработке лейкоцитов.
- Чечевица. Употребление каш, супов на её основе поможет поддержать состав крови в норме в домашних условиях.
- Настойка из растения барбарис провоцируют поднятие. Приобретается в аптеке, пьют до еды в объёме чайной ложки, разбавленной водой.
- Настойка из родиолы розовой. Двадцать-тридцать капель настойки добавляют в полстакана воды, принимают перед едой трижды. Чтобы предотвратить снижение уровня лейкоцитов, рекомендуют производить лечение за несколько месяцев (идеально за три) до курса химиотерапии.

- Столовая ложка мёда. Нужно есть утром до завтрака. Повысит иммунитет, увеличит пониженные лейкоциты.
- Настой грецкого ореха. Сто граммов перемолотых плодов заливают двумястами граммами спирта. Настаивают четырнадцать дней. Процеживают, пьют раз в день по две чайные ложки, разбавленные водой.
- Настойка из донника. Шестьдесят грамм растолчённой травы заливают тремястами миллилитрами воды, дают настояться четыре часа. Курс: месяц потреблять по полстакана в день.
- Квас с использованием свёклы. Имеет противопоказания (подагра). Один овощ крупно нарезать, сложить во вместительную банку. Добавить шестьдесят граммов мёда, соли. Влить три литра тёплой воды. Оставить на трое суток в месте без света. Принимать один раз по пятьдесят граммов до еды.
- Пиво со сметаной. Внимание! Рецепт не показан ожидающим ребёнка, кормящим грудью матерям, несовершеннолетним. Стакан тёмного пива смешивают с тремя столовыми ложками сметаны, перемешивают. Напиток употреблять единожды в день.
- Отвар ячменя. В глубокую ёмкость объёмом два литра помещают полтора стакана промытого зерна овса. Кипячение происходит через полчаса. Настаивать шестьдесят минут, пить пол-литра в день.
- Разрешены витаминные напитки из фруктов, ягод, содержащих B12, С.
Указанные выше способы смогут вызвать повышение при регулярности приёма. Распространена комплексная терапия медикаментозно совместно с лекарственными препаратами основного, вспомогательного типа, диетологическим подходом. Этот путь терапии наиболее популярен и показывает хорошие результаты.
При лечении недостатка белых телец в крови перед химиотерапией следует соблюдать все предписания врача-онколога, употреблять полезную, содержащую витамины пищу. Достаточно вовремя начать лечиться, чтобы избежать осложнений, вызванных лейкопенией.
Способы повышения лейкоцитов после химиотерапии
После лечения цитостатиками значительно меняются характеристики лейкоцитов в крови: снижается их количество и скорость образования. Самым опасным осложнением химио- и радиотерапии является поражение костного мозга с угнетением ростка кроветворения. Под воздействием токсических препаратов кровяные клетки быстро разрушаются, а восстанавливаться так быстро не могут. После каждой дозы цитостатиков организму нужно время для восстановления уровня лейкоцитов.
Лейкоциты выполняют защитную функцию организма и борются с попавшими в него чужеродными микроорганизмами. Нормальным уровнем лейкоцитов для выполнения их функции считается 4000-8800 в микролитр крови.
Как наиболее эффективно повысить лейкоциты во время химиотерапии
Для начала стоит соблюдать диету, составленную специалистами:
1.Регулярное употребление грецких орехов. Можно ежедневно съедать по 5-7 штук либо приготовить настойку. Для ее приготовления очищенные грецкие орехи залейте водкой и настаивайте на свету около 2-ух недель, после этого уберите ее в темное место, употребляйте по 1 ст. л. 3 р/день длительно.
2.Важную роль играет поступление в организм легкоусвояемых белков, в большом количестве их содержат куриный бульон с мясом, говядина, тушеные рыба и овощи. Кроме этого, они содержат растительный и животный протеин, необходимый для организма.
3.Ежедневное употребление овощных соков. Наиболее полезными являются морковный и свекольный.
4.Положительно влияет на уровень лейкоцитов мед. Его необходимо употреблять по 1-2 ст. л. утром до первого приема пищи.
5.Каждый день в рацион должны входить фрукты и овощи красного цвета (перец, гранат, смородина, клубника, свекла).
6.Обязательно употребление рыбы красных сортов.
7.Употребление жидкости в больших объемах, не менее 2 литров.
Народная медицина, рецепты
Овес. Из него готовится отвар, способствующий повышению уровня лейкоцитов.Чтобы приготовить настой, потребуется овес, молоко, средняя кастрюля. Кастрюля до половины наполняется промятым овсом и заливается молоком. Далее все содержимое доводится до кипения и вариться на слабом огне 20 мин. После отвар охлаждается, процеживается и употребляется вместо воды. Важным условием для успешного лечения является употребление овсяного отвара непосредственно перед употреблением пищи. Нужно помнить, что каждый день следует готовить свежий отвар. После окончания курса лечения делают перерыв в течение месяца и проводят повторный курс.
Шиповник. Пять столовых ложек измельченных плодов шиповника заливается литром воды, кипятить на слабом огне 10 минут. После этого отвар укрывают покрывалом и оставляют на ночь. Утром его процеживают и пьют в течение чая.
Гречка. Промытую гречку на ночь заливают кефиром, а утром едят вместо завтрака.
Цикорий. Напиток из цикория пьют вместо чая.
Чечевица. Чечевица промывается и проращивается и употребляется по 1 столовой ложке 2 раза в течение суток.
Ячмень. Полтора стакана ячменя заливают 2 литрами воды, доводится до кипения и варится, пока количество воды не станет в два раза меньше. Употреблять с медом.
Фасоль. Увеличить содержание лейкоцитов помогут также зеленые зерна фасоли. В таком случае понадобится сок зерен, отжатый именно из недозрелых стручков. Принимать такое средство нужно 4-5 раз в день по 1-2 чайных ложек, перед употреблением разводить теплой водой. Первый в течение суток прием лучше выполнять на голодный желудок.
Хочется отметить, что после химиотерапии диета должна быть сбалансированной и разнообразной. В нее обязательно необходимо включать белковые продукты, крайне необходимые для восстановления сил и иммунной системы после курсов цитостатиков, а также овощи и фрукты всех оттенков красного. Желательно, чтобы в рационе присутствовали грецкие орехи, бобовые, гречка, овес и ячмень. Из них можно приготовить различные отвары по описанным выше рецептам. Для восстановления всех функций организма обязательно употребление жидкости в больших объемах. Обязательно употребление чая из цикория, шиповника, соков из фруктов и овощей.
Для подбора эффективного метода лечения вы можете обратиться за
– методы инновационной терапии;
– возможности участия в экспериментальной терапии;
– как получить квоту на бесплатное лечение в онкоцентр;
– организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Стимуляторы лейкопоэза (процесса образования лейкоцитов)
ЛЕЙКОГЕН (Leucogcnum)
Фармакологическое действие. Увеличивает число лейкоцитов (форменных элементов крови) в крови при лейкопении (снижении уровня лейкоцитов в крови). Малотоксичен, не обладает кумулятивными свойствами (не накапливается в организме).
Показания к применению. Лейкопения (снижение уровня лейкоцитов в крови) при лучевой и лекарственной терапии.
Способ применения и дозы. Внутрь по 0,02 г 3-4 раза в день до нормализации лейкоцитарной формулы (соотношения различных форм лейкоцитов – 5-7 дней; при стойкой лейкопении – 2-3 нед. и более.
Противопоказания. Лимфогранулематоз (злокачественное заболевание лимфоидной ткани), злокачественные новообразования костного мозга.
Форма выпуска. В таблетках по 0,02 г в упаковке – по 20 штук.
Условия хранения. Список Б. В защищенном от света месте.
ЛЕЙКОМАКС (Leukomax)
Синонимы: Молграмостин.
Фармакологическое действие. Лейкомакс представляет собой водорастворимый негликолизированный белок. Состоит из 127 аминокислот, имеет молекулярный вес 14 447 дальтон, содержит изолейцин в положении 100. Образуется штаммом Escherichia coli, несушим полученную с помощью генной инженерии плазмиду, содержащую ген гранулоцитарно-макрофагального колониестимулирующего фактора человека.
Лейкомакс обладает поливалентным (разнонаправленным) действием на различные ростки кроветворения: активирует зрелые миелоидные клетки (клетки костного мозга, из которых образуются форменные элементы крови – эритроциты и тромбоциты), стимулирует пролиферацию и дифференцировку (увеличение числа и специфичности) клетокпредшественников кроветворной системы, что приводит к образованию гранулоцитов, моноцитов и Т-лимфоцитов. Препарат значительно повышает содержание лейкоцитов в крови, главным образом, нейтрофилов, и, в меньшей степени, лимфоцитов и эозинофилов. После однократного парентерального (минуя желудочно-кишечный тракт) “введения лейкомакса это действие проявляется через 1-4 ч и достигает пика через 6-18 ч. Лейкемакс усиливает функциональную активность зрелых нейтрофилов в отношении бактерий и клеток злокачественных опухолей.
При подкожном введении максимальная концентрация препарата в сыворотке крови достигается через 3-4 ч. Препарат быстро метаболизируется (разрушается). Период полувыведения составляет 1-2 ч после внутривенного введения и 1-3 ч после подкожного введения.
Показания к применению. Профилактика и лечение нейтропении (уменьшения числа нейтрофилов в крови) у больных, получающих миелосупрессивную (подавляющую активность костного мозга) терапию (например, химиотерапевтические противоопухолевые средства); у больных с миелодиспластическими синдромами (общее название нарушений кроветворной функции костного мозга), апластической анемией (снижением содержания гемоглобина в крови, обусловленным угнетением кроветворной функции костного мозга); после трансплантации (пересадки) костного мозга.
Способ применения и дозы. Лейкомакс должен применяться под наблюдением врача, имеющего опыт лечения тех заболеваний, при которых препарат назначается. Первую дозу лейкомакса следует вводить, обеспечив тщательное медицинское наблюдение за больным. Дозы устанавливают с учетом показаний. Максимальная суточная доза – 10 мкг/кг.
Больным, получавшим миелосупрессивную терапию, назначают в суточной дозе 5-10 мкг/кг подкожно. Лечение начинают через 24 ч после последнего курса противоопухолевой химиотерапии и продолжают в течение 7-10 дней.
При миелодиспластических синдромах и апластической анемии по 3 мкг/кг один раз в день подкожно. Обычно для проявления лечебного действия препарата (повышения количества лейкоцитов в крови) требуется от 2 до 4 дней. В последующем суточную дозу подбирают так, чтобы содержание лейкоцитов в крови поддерживалось на желательном уровне (обычно не более 10 000/мм3).
Больным, которым проведена трансплантация (пересадка) костного мозга, лейкомакс вводят внутривенно капельно (в течение 4-6 ч) в суточной дозе 10 мкг/кг, начиная со дня трансплантации. Введение повторяют до тех пор, пока абсолютное число нейтрофилов в крови не достигнет 1000/мм3 и более. Максимальная продолжительность лечения составляет 30 дней.
Во время лечения лейкомаксом следует проводить анализы крови (включая определение количества лейкоцитов, их формулы; а также количества тромбоцитов) и следить за концентрацией альбумина в сыворотке.
Следует иметь в виду, что применение химиотерапевтических противоопухолевых препаратов в больших дозах (наряду с лейкомаксом) может повышать риск развития тромбоцитопении (уменьшения числа тромбоцитов в крови) и анемии. Рекомендуется регулярное определение содержания тромбоцитов в крови, а также гематокрита (отношения объема форменных элементов крови к объему плазмы).
По данным специальных исследований, после применения лейкомакса примерно у 1 % больных обнаруживаются антитела к лейкомаксу. Указаний на снижение лечебной активности препарата в этих случаях не получено.
Применение лейкомакса у пациентов пожилого возраста проводится в соответствии с обычными рекомендациями.
У больных, страдающих заболеваниями легких, при лечении лейкомаксом отмечается тенденция к снижению функции внешнего дыхания и развитию одышки; такие больные требуют внимательного наблюдения.
Раствор лейкомакса следует готовить непосредственно перед введением. Для приготовления раствора для подкожного введения добавить во флакон, содержащий лейкомакс, 1 мл бактериостатической воды для инъекций или стерильной воды для инъекций. Аккуратно перемешать до полного растворения порошка. Для приготовления раствора для внутривенного введения растворить в 1 мл стерильной воды для инъекций содержимое каждого из требуемого количества флаконов лиофилизированного (высушенного путем замораживания в вакууме) порошка. Полученный раствор препарата далее развести физиологическим раствором или 5% раствором глюкозы. Используется обычно 25, 50 или 100 мл раствора таким образом, чтобы окончательная концентрация лейкомакса в нем была не менее 7 мкг/мл. Данный раствор препарата пригоден к применению, по крайней мере, в течение 24 ч после приготовления (при хранении в холодильнике). Во избежание потери лейкомакса в результате адсорбции (поглощения) на компонентах инфузионной системы следует использовать следующие’ системы: набор для внутривенного вливания Травенол 2С0001, Интрафикс Эйр энд Инфузионгерэт R 87 Plus (Германия), Супли (Souplix, Франция), Травенол С0334 и Стерифлекс (Великобритания), Интравис Эйр Евроклапп-ISO и Солусет (Испания) и Линфосол (Италия). Не рекомендуется использование системы Порт-А-Кат (Фармация) из-за значительной адсорбции лейкомакса на ее компонентах. Рекомендуется применять в системе для внутривенного введения лейкомакса фильтр с низкой способностью к связыванию белка с диаметром пор от 0,2 до 0,22 мкм (например, Millipore Durapore). Следует визуально оце. кивать цвет и гомогенность (отсутствие частиц) раствора лейкомакса перед его внутривенным введением.
После растворения в бактериостатической воде для инъекций раствор лейкомакса можно использовать в течение недели, если он хранится при температуре +2-* +8 °С. Раствор лейкомакса можно заморозить, в таком , состоянии он устойчив в течение 28 дней. Замороженный препарат можно оттаивать, и повторно замораживать не более двух раз.
После растворения в стерильной воде для инъекций лейкомакс должен использоваться в течение 24 ч при условии хранения в холодильнике при температуре +2-+8 °С. Неиспользованный раствор лейкомакса следует вылить.
Побочное действие. Тошнота, рвота, анорексия (отсутствие аппетита), диарея (понос), возможны стоматит (воспаление слизистой оболочки полости рта), боли в животе; судороги, миалгии (мышечные боли), чувство усталости, астенические явления (слабость), возможны головные боли, головокружение, парезы (уменьшение силы и/или амплитуды движений); редко спутанность сознания, повышение внутричерепного давления, нарушения мозгового кровообращения; одышка, редко экссудативный плеврит (воспаление легочных оболочек, сопровождающееся выходом из ткани богатого белком отделяемого); редко артериальная гипотония (понижение артериального давления), обмороки, нарушения ритма сердца, сердечная .недостаточность, отек легких, повышенная капиллярная проницаемость, периферические отеки, экссудативный перикардит (воспаление околосердечной сумки, сопровождающееся выходом из ткани богатого белком отделяемого). При развитии плеврита и/или перикардита лейкомакс следует отменить. Возможны сыпь, зуд; болезненность в месте подкожного введения препарата. Со стороны лабораторных показателей наиболее часто отмечается снижение числа тромбоцитов, гемоглобина и уровня альбумина сыворотки крови. Также наблюдается повышение абсолютного и относительного содержания эозинофилов в крови. Редко проявляются аллергические реакции в виде бронхоспазма (резкого сужения просвета бронхов), ангионевротического отека, анафилактического шока. При появлении аллергических реакций лейкомакс следует немедленно отменить и в последующем не применять. Часто наблюдаются лихорадка (резкое повышение температуры тела), боли в костях. Возможны неспецифические боли в области грудной клетки, повышенное потоотделение.
При лечении лейкомаксом в отдельных случаях отмечалось развитие аутоиммунных заболеваний (заболеваний, в основе которых лежат аллергические реакции на собственные ткани или продукты жизнедеятельности организма) или их обострение. Это следует учитывать при назначении лейкомакса больным с аутоиммунными заболеваниями в анамнезе (истории болезни).
Такие побочные явления, появляющиеся в начале применения лейкомакса, как судороги, одышка, повышение температуры тела, тошнота, рвота, неспецифические боли в области грудной клетки, астенические явления, артериальная гипотония и ощущения прилива крови, в случае их небольшой выраженности, как правило, не требуют отмены препарата.
Противопоказания. Повышенная чувствительность к препарату.
Опыт применения лейкомакса при миелоидных лейкозах ограничен.
Безопасность применения лейкомакса у беременных женщин не установлена.
При необходимости назначения лейкомакса кормящимматерям кормление грудью не рекомендуется.
Безопасность применения лейкомакса была установлена лишь у ограниченного числа пациентов в возрасте” до 18 лет.
Исследования по определению влияния на репродуктивную функцию человека не проводилось.
Форма выпуска. Сухой лиофилизированный (высушенный путем замораживания в вакууме) порошок для инъекций во флаконах, содержащих 50 мкг (0,55×106 ед.); 150 мкг (1,67×106 ед.); 300 мкг (3,33×106 ед.); 400 мкг (4,44×106 ед.); 500 мкг (5,55×106 ед.) или 700 мкг (7,77×106 ед.).
Условия хранения. Список Б. Стерильный порошок лейкомакса в стеклянном флаконе типа 1 с пробкой из бутилированного или галобутилированного каучука и алюминиевым колпачком стабилен в течение 24 месяцев при температуре +2-+S °С, в условиях защиты от действия света.
ЛЕНОГРАСТИМ (Lenograstim)
Синонимы: Граноцит.
Фармакологическое действие. Ленограстим является рекомбинантным (полученным путем генной инженерии) человеческим гранулоцитарным колониестимулирующим фактором. Оказывает стимулирующее действие на клетки костного мозга и вызывает значительное увеличение в периферической крови числа лейкоцитов, главным образом нейтрофилов.
Показания к применению. Профилактика и лечение нейтропении (уменьшения числа нейтрофилов в крови) у больных, получающих химиотерапевтические противоопухолевые средства; после трансплантации (пересадки) костного мозга. Проведение периферической коллекции стволовых клеток костного мозга.
Способ применения и дозы. Препарат назначают из расчета 19,2 млн. ME (или 150 мкг) на м2 поверхности тела (0,64 млн. ME или 5 мкг на кг массы тела) в день. Максимальная доза препарата составляет 40 мкг на кг массы тела в день. Максимальная длительность непрерывного применения препарата не должна превышать 28 дней.
При проведении химиотерапии ленограстим применяют на следующий день после окончания курса лечения противоопухолевыми препаратами и вводят его подкожно (для чего разводят содержимое 1 флакона препарата прилагаемой водой для инъекций), ежедневно, до достижения стабильно нормального уровня нейтрофилов в периферической крови.
При трансплантации костного мозга препарат применяют на следующий день после проведения процедуры, вводят его внутривенно в течение 30 мин, ежедневно, до достижения стабильно нормального уровня нейтрофилов в периферической крови. Для внутривенной инфузии 1 флакон препарата растворяют сначала в прилагаемой воде для инъекций, затем полученный раствор дополнительно разводят 0,9% раствором натрия хлорида следующим образом: дозу 13,4 млн. ME -не более, чем в 50 мл; дозу 33,6 млн. ME -не более, чем в 100 мл; дозу 47,0 млн. ME – не более, чем в 140 мл.
В период терапии ленограстимом необходим систематический контроль картины периферической крови и обязательным подсчетом лейкоцитов и тромбоцитов.
Ленограстим уменьшает не все побочные эффекты. 1 противоопухолевой терапии, а только миелотоксический (повреждающее воздействие на костный мозг) эффект, поэтому не следует превышать рекомендуемые дозы препарата, в том числе и при увеличении дозы противоопухолевых химиотерапевтических средств.
Начинать лечение препаратом не рекомендуется непосредственно во время химиотерапии.
Побочное действие. Лейкоцитоз (увеличение содержания лейкоцитов в крови), тромбоцитопения (уменьшение числа тромбоцитов в крови). Боли в мышцах и костях. Боли в месте инъекции.
Противопоказания. Повышенная чувствительность к ленограстиму или к любому компоненту препарата; острый и хронический миелолейкоз (рак крови, при котором источником опухолевого процесса являются гранулоцитарные клетки /клетки костного мозга, из которых развиваются форменные элементы крови -лейкоциты/).
Следует соблюдать осторожность при назначении препарата больным миелодиспластическим синдромом (рефрактерной анемией /снижением уровня эритроцитов в крови/ различной этиологии /причины/) и при всех предопухолевых состояниях миелоидного (костномозгового) кроветворения.
Форма выпуска. Лиофилизированное (высушенное путем замораживания в вакууме) сухое вещество для инъекций во флаконах в комплекте с растворителем (1 флакон содержит 13,4 млн. ME, 33,6 млн. ME или 33,6 млн. ME, растворитель – вода для инъекций 1 мл в ампулах; 1 флакон содержит 47 млн. ME , растворитель – вода для инъекций 1,4 мл в ампулах).
Условия хранения. Список Б. В сухом, прохладном, защищенном от света месте.
ФИЛГРАСТИМ (Filgrastim)
Синонимы: Неупоген.
Фармакологическое действие. Филграстим является гемопоэтическим фактором роста (стимулятором кроветворения), который регулирует продукцию и высвобождение нейтрофилов из костного мозга в периферическую кровь. Имеет место дозозависимое увеличение количества нейтрофилов с нормальной или повышенной функциональной активностью. По окончании терапии филграстимом количество циркулирующих нейтрофилов снижается на 50% через 1-2 дня и возвращается к нормальному уровню в течение 2-7 дней. При подкожном и внутривенном введении препарата наблюдается линейная корреляция между введенной дозой и концентрацией его в сыворотке. Период полураспада составляет приблизительно 3,5 ч.
Показания к применению. Нейтропения (уменьшение числа нейтрофилов в крови) и нейтропеническая лихорадка (резкое повышение температуры тела) у больных, получающих цитостатическую (подавляющую деление клеток) химиотерапию.
Способ применения и дозы. Филграстим вводят в вену или подкожно из расчета 5 мг/кг массы тела 1 раз в день в 16,6 мл растворителя (5% раствор глюкозы), т.е. больному с массой тела в 60 кг требуется 300 мг филграстима. Максимальная суточная доза не должна превышать 70 мг/кг. Больным, леченным цитостатиками (средствами, подавляющими деление клеток) с аутотрансплантацией (пересадкой ткани в пределах одного организма) костного мозга, рекомендуется начальная доза филграстима из расчета 20 мг/день при подкожном введении или 30 мг/кг в день при внутривенном введении с 20-50 мл 5% раствора глюкозы. Интервал между приемом филграстима и цитостатика не должен быть менее 24 ч. Полная суточная доза филграстима вводится после установления критического уровня падения нейтрофилов и начинающегося его подъема. Продолжительность лечения – 14-18 дней. При изменении числа нейтрофилов доза препарата должна быть титрована по их количественному содержанию.
Если препарат разводится в концентрации 15 мг/мл, то следует добавлять 0,2% раствор альбумина до конечной концентрации 2 мг/мл. В процессе лечения должен осуществляться контроль за количеством лейкоцитов (при повышении более 50″! О9 л препарат отменяют) и за плотностью костного мозга у больных с остеопорозом (нарушением питания костной ткани, сопровождающимся увеличением ее ломкости).
Побочное действие. Могут отмечаться мышечные боли, преходящее падение артериального давления, реже – расстройство мочеиспускания, дозозависимое повышение содержания ферментов лактатдегидрогеназы, щелочной фосфатазы, гаммаглютаминтрансферазы и мочевой кислоты. Препарат не увеличивает риск развития побочных эффектов от химиотерапии, но не предупреждает развития тромбоцитопении (уменьшение числа тромбоцитов в крови) и анемии (снижение содержания гемоглобина в крови).
Противопоказания. Повышенная чувствительность к препарату. Следует с осторожностью назначать препарат больным с острой и хронической лейкемией (злокачественными опухолями крови), нарушенной функцией печени и почек. Не рекомендуется принимать филграстим при беременности и кормлении грудью.
Форма выпуска. Раствор для инъекций в ампулах по 1 мл (0,3 г филграстима) и 1,6 мл (0,48 г филграстима).
Условия хранения. Список Б. В защищенном от света месте. Раствор препарата готовится не ранее чем за 24 ч до введения и хранится при температуре +2-+8 °С.
Как быстро повысить лейкоциты в крови после химиотерапии в домашних условиях
Индуцированное химиотерапией снижение уровня лейкоцитов в крови, или лейкопения — один из наиболее часто встречаемых побочных эффектов, встречаемых в клинической онкологии. Лейкопенией называют снижение уровня лейкоцитов до 2 × 10 9 / л и ниже.
Недавние исследования показали, что частота возникновения лейкопении после химиотерапии составляет от 16% до 59%. Лечение лейкопении после химиотерапии является обязательным, поскольку данное состояние вызывает клинически значимые изменения иммунной системы. Это негативно влияет на качество жизни пациентов, увеличивая частоту инфекционных заболеваний и затрат на лечение.
- 1 Как химиотерапия влияет на состав крови
- 2 Почему важно поднять уровень лейкоцитов, эритроцитов и нейтрофилов
- 2.1 Зачем нужны клеточные элементы крови?
- 2.2 Что будет, если не повысится уровень лейкоцитов?
- 3 Основные методы влияния на состав крови после химиотерапии
- 3.1 Как быстро повысить лейкоциты в крови после химиотерапии в домашних условиях
- 3.2 Как повысить эритроциты в крови после химиотерапии в домашних условиях
- 3.3 Как поднять нейтрофилы после химиотерапии при помощи методов традиционной медицины
Как химиотерапия влияет на состав крови
Химиотерапевтические препараты уничтожают не только опухолевые клетки, но и здоровые клетки организма. Активно делящиеся юные клетки костного мозга наиболее чувствительны к воздействию химиотерапии, тогда как зрелые и высокодифференцированные клетки в периферической крови реагируют на неё меньше. Так как красный костный мозг является центральным органом гемопоэза, синтезируя клеточный компонент крови, его угнетение приводит к:
- уменьшению количества эритроцитов — анемии;
- уменьшению количества лейкоцитов — лейкопении;
- уменьшению количества тромбоцитов — тромбоцитопении.
Состояние, при котором наблюдается недостаток всех кровяных клеток называется панцитопенией.
Лейкоциты после химиотерапии реагируют не сразу. Как правило, количество лейкоцитов начинает снижаться через 2—3 дня после лечения и достигает пика между 7 и 14 днем.
Если наблюдается уменьшенное количество нейтрофилов, которые являются одним из вариантов лейкоцитов, наблюдается нейтропения. Нейтропения, ассоциированная с химиотерапией является одной из наиболее распространенных миелотоксических реакций, связанных с системным лечением рака, из-за цитотоксических эффектов по отношению к быстро делящимся нейтрофилам.
Зрелые гранулоциты, в том числе нейтрофилы, имеют продолжительность жизни от 1 до 3 дней, поэтому они имеют высокую митотическую активность и большую восприимчивость к цитотоксическому повреждению, чем другие клетки миелоидного ряда с более длительным периодом жизни. Начало и продолжительность нейтропении широко варьируют в зависимости от препарата, дозы, частоты сеансов химиотерапии и т.д.
Учитывая данные побочные эффекты большинства химиотерапевтических препаратов, пациентам назначается общий анализ крови в динамике, чтоб проследить за исходными данными показателей крови и их изменениями со временем.
Почему важно поднять уровень лейкоцитов, эритроцитов и нейтрофилов
Низкое количество разных форм лейкоцитов в гемограмме указывает на иммуносупрессию пациента. Угнетение иммунитета сопровождается увеличением восприимчивости организма к вирусным, грибковым и бактериальным заболеваниям. Снижение уровня лимфоцитов (в особенности NK-клеток) увеличивает риск рецидива опухоли, так как данные клетки отвечают за уничтожение атипичных (злокачественных) новообразований.
Также панцитопения сопровождается нарушением свертываемости крови, частыми спонтанными кровотечениями, лихорадкой, полилимфоаденопатией, анемиями, гипоксией и ишемией органов и тканей, увеличением риска генерализации инфекций и развития сепсиса.
Зачем нужны клеточные элементы крови?
Красные кровяные тельца, или эритроциты содержат железосодержащий пигмент гемоглобин, который является переносчиком кислорода. Эритроциты обеспечивают адекватную доставку кислорода тканям организма, поддерживая полноценный метаболизм и энергетический обмен в клетках. При нехватке эритроцитов наблюдаются изменения в тканях вследствие гипоксии — недостаточного поступления в них кислорода. Наблюдаются дистрофические и некротические процессы, нарушающие функционирование органов.
Тромбоциты отвечают за процессы коагуляции крови. Если у пациента количество тромбоцитов меньше 180х10 9 / л, у него наблюдается повышенная кровоточивость — геморрагический синдром.
Функция лейкоцитов состоит в защите организма от того, что является для него генетически чужеродным. Собственно, это и является ответом на вопрос о том, почему важно поднять уровень лейкоцитов — без лейкоцитов иммунная система пациентов не будет функционировать, что сделает доступным его организм для различных инфекций, а также опухолевых процессов.
Сами лейкоциты по микроскопическим характеристикам делятся на следующие группы:
- эозинофилы,
- нейтрофилы,
- базофилы;
Эозинофилы принимают непосредственное участие в противопаразитрном иммунитете, а также модулирует некоторые типы реакций гиперчувствительности. Эозинофильные гранулоциты могут, как способствовать развитию аллергической реакции, так и выступать её ингибиторами.
Функция нейтрофилов состоит в противогрибковой и антибактериальной защите. Гранулы, которые содержит в своей цитоплазме нейтрофил, содержат сильные протеолитические ферменты, высвобождение которых приводит к гибели патогенных микроорганизмов.
Базофилы принимают участие в воспалительном процессе и аллергических реакциях. В своей цитоплазме они содержат гранулы с медиатором гистамином. Гистамин приводит к расширению капилляров, снижению артериального давления, сокращению гладкой мускулатуры бронхов.
Лимфоциты разделяются на несколько видов. В-лимфоциты продуцируют иммуноглобулины, или антитела. Т-лимфоциты принимают участие в регуляции иммунного ответа: Т-киллеры обладают цитотоксическим действием по отношению к вирусным и опухолевым клеткам, Т-супрессоры препятствуют аутоиммунизации и подавляют иммунный ответ, Т-хелперы активируют и регулируют Т- и В-лимфоциты. Натуральные, или естественные киллеры способствуют уничтожению вирусных и атипичных клеток.
Моноциты являются предшественниками макрофагов, осуществляющих регуляторную и фагоцитарную функции.
Что будет, если не повысится уровень лейкоцитов?
Повышение лейкоцитов после химиотерапии необходимо для предотвращения последствий иммуносупрессии. Если у пациента наблюдается лейкопения, в частности, нейтропения, он будет восприимчив к инфекционным заболеваниям.
Клиническими проявлениями нейтропении может быть:
- субфебрильная лихорадка (температура в подмышечной впадине в пределах 37,1—38,0 °C);
- рецидивирующие гнойничковые высыпания, фурункулы, карбункулы, абсцессы;
- одинофагия — боль при глотании;
- отечность и боль десен;
- припухлость и болезненность языка;
- язвенный стоматит — образование поражения слизистой оболочки ротовой полости;
- рекуррентные синуситы и отиты — воспаления околоносовых пазух и среднего уха;
- симптомы пневмонии — кашель, одышка;
- периректальная болезненность, зуд;
- грибковые инфекции кожи и слизистых оболочек;
- постоянная слабость;
- нарушение сердечного ритма;
- боли в животе и за грудиной.
Чаще всего пациенты поступают с:
- внезапным недомоганием;
- внезапной лихорадкой;
- болезненным стоматитом или периодонтитом;
- фарингитом.
В тяжелых случаях развивается сепсис по типу септикопиемии или хрониосепсиса, что может привести к септическому шоку и летальному исходу.
Основные методы влияния на состав крови после химиотерапии
Идеальным вариантом была бы отмена того фактора, который приводит с лейкопении, однако зачастую отменить химиотерапию нельзя. Потому приходится использовать симптоматическую и патогенетическую терапию.
Как быстро повысить лейкоциты в крови после химиотерапии в домашних условиях
В домашних условиях можно откорректировать диету. Питание при низких лейкоцитах после химиотерапии должно быть сбалансированным и рациональным. Рекомендуется преобразовать пищевой рацион таким образом, чтоб увеличить в нем количество следующих компонентов:
- витамин Е,
- цинк,
- селен,
- зеленый чай,
- витамин С,
- каротиноиды,
- омега-3-жирные кислоты,
- витамин А,
- йогурт,
- чеснок,
- витамин В12,
- фолиевая кислота.
Выбор данных продуктов питания, повышающих уровень лейкоцитов в крови после химиотерапии, подходит для любого варианта умеренной иммуносупрессии, а также для профилактического использования. Он обоснован клиническими исследованиями по отношению к их иммуностимулирующему эффекту.
- Витамин Е, или токоферол содержится в большом количестве в подсолнечных семенах, миндальных и грецких орехах, сое. Он стимулирует продукцию натуральных киллеров (NK-клеток), которые обладают цитотоксическим эффектом по отношению к опухолевым и зараженным вирусом клеткам. Также токоферол участвует в продукции В-лимфоцитов, которые отвечают за гуморальный иммунитет — продукцию антител.
- Цинк увеличивает количество Т-киллеров и активирует В-лимфоциты. Он содержится в красном мясе, кальмарах, куриных яйцах.
- Был доказан иммуностимулирующий эффект селена в сочетании с цинком (по сравнению с плацебо) в исследовании Медицинской школы Мэрилендского университета. Исследовался в данном случае ответ на вакцину от гриппа. Селена много в фасоли, чечевице и горохе.
- Зеленый чай содержит большое количество антиоксидантов и факторов, способствующих стимуляции лимфоцитопоэза.
- Считается, что витамин С, которым насыщена черная смородина и цитрусы, стимулирует иммунную систему посредством влияния на синтез лейкоцитов, продукцию иммуноглобулинов и гамма-интерферона.
- Бета-каротин увеличивает количество натуральных киллеров, Т-лимфоцитов, а также препятствует перекисному окислению липидов свободными радикалами. Содержится в моркови. Кроме того, каротиноиды имеют определенный кардиопротекторный и вазопротекторный эффект.
- Большое количество омега-3-жирных кислот находится в морепродуктах и многих растительных маслах. Исследовался их иммуностимулирующий эффект по отношению к заболеваемости респираторными вирусными инфекциями — частота случаев болезни у людей, принимающих чайную ложку льняного масла в сутки, была уменьшена в сравнении с пациентами, которые его не употребляли.
- Витамин А, или ретинол содержится в абрикосах, моркови, тыкве. Он усиливает продукцию белых кровяных телец.
- Пробиотики, содержащиеся в йогурте, способствуют оптимизации жизнедеятельности исходной микрофлоры кишечника, а также увеличивает количество лейкоцитов. Немецкие исследователи провели исследование, которое было опубликовано в журнале «Clinical Nutrition». Оно показало, что 250 здоровых взрослых исследуемых, которые получали добавки йогурта 3 месяца подряд, демонстрировали симптомы простуды реже, чем те 250 из контрольной группы, которые не получали. Также у первой группы наблюдался более высокий уровень лейкоцитов.
- Чеснок обладает стимулирующим действием та лейкоциты, что обусловлено наличием серосодержащих компонентов (сульфиды, аллицин). Замечено, что в культурах, у которых чеснок является популярным пищевым продуктом, наблюдается низкая заболеваемость раком органов желудочно-кишечного тракта.
- Витамин В12 и фолиевую кислоту рекомендует Академия питания и диеты США в журнале «Oncology Nutrition». Специалисты указывают на использовании этих витаминов в синтезе белых кровяных телец.
Есть мнения, согласно которым можно поднять лейкоциты после химиотерапии народными средствами, однако этот вариант подходит исключительно для легких и бессимптомных форм — иначе можно запустить заболевание. Народная медицина в данном случае основывается на фитотерапии и рекомендует следующие варианты улучшения функции иммунной системы:
- отвар / настойка эхинацеи;
- классический имбирный чай (с тертым корнем имбиря, мёдом и лимоном);
- настойка прополиса (15—20 капель настойки на стакан молока);
- смесь сока алоэ, меда и кагора в соотношении 1:2:3;
- прочие травяные чаи: шиповниковый, яблочный, ромашковый.
Разумеется, поднять лейкоциты после химиотерапии за 3 дня одними продуктами питания, если их количество резко понижено, невозможно.
В случае, если уровень лейкоцитов не восстанавливается в срок, и тем более когда наблюдаются симптомы лейкопении обязательно использование рациональной медикаментозной терапии.
Как повысить эритроциты в крови после химиотерапии в домашних условиях
Для лечения анемии легкой степени дома следует употреблять в пищу продукты с железосодержащими соединениями или с веществами, улучшающими его усваивание, а также с фолиевой кислотой и витамином В12. К ним относится:
- красное мясо,
- цитрусы,
- красная смородина,
- гранаты,
- миндаль,
- грецкие орехи,
- капусту.
Народная медицина предлагает использовать для лечения легкой анемии следующие средства:
- травяной сбор из листьев земляники, ягод шиповника, корня кровохлебки и медуницы — по 100 мл дважды в день около 2 месяцев;
- свекольный сок с медом — столовая ложка трижды в день;
- изюм, чернослив, курага и мед в соотношении 1:1:1:1 — три кофейные ложки трижды в день до приема пищи.
Как поднять нейтрофилы после химиотерапии при помощи методов традиционной медицины
Для лечения нейтропении как угрожающего жизни пациента состояния используются следующие группы препаратов:
- антибиотики,
- противогрибковые средства,
- гемопоэтические факторы роста.
Первые две группы препаратов направлены на последствия нейтропении, а именно рецидивирующие бактериальные и гнойные инфекции.
К наиболее часто используемым антибиотикам при нейтропенических инфекциях относятся, например:
- имипенем ® ,
- меропенем ® ,
- цефтазидим ® ,
- ципрофлоксацин ® ,
- офлоксацин ® ,
- аугментин ® ,
- цефепим ® ,
- ванкомицин ® .
Из противогрибковых средств рекомендуется использовать вориконазол ® и каспофунгин ® .
К препаратам, непосредственно повышающим уровень лейкоцитов в крови, относятся факторы роста. Гемопоэтические факторы роста вводят для ускорения восстановления уровня нейтрофилов и сокращения продолжительности нейтропенической лихорадки. К рекомендуемым факторам роста относятся филграстим ® , сарграмостим ® , пегфилграстим ® .
- Филграстим ® (Neupogen ® ) является гранулоцитарным колониестимулирующим фактором (G-CSF), который активирует и стимулирует синтез, созревание, миграцию и цитотоксичность нейтрофилов. Был доказан его эффект относительно ускорения восстановления уровня нейтрофилов и сокращения продолжительности нейтропенической лихорадки. Тем не менее, согласно этим исследованиям, продолжительность лечения антибиотиками, продолжительность пребывания в больнице и смертность не изменились. Филграстим наиболее эффективен при тяжелой нейтропении и дигностированных инфекционных поражениях.
- Сарграмостим ® (Leukine ® ) является гранулоцитарно-макрофагальным колониестимулирующим фактором (GM-CSF), который способствует реабилитации нейтрофилов после химиотерапии и мобилизации клеток-предшественников периферической крови.
- Пегфилграстим ® (Neulasta ® ) является филграстимом длительного действия. Подобно филграстиму, он действует на гемопоэтические клетки путем связывания с определенными рецепторами клеточной поверхности, тем самым активируя и стимулируя синтез, созревание, миграцию и цитотоксичность нейтрофилов.
Все препараты подбираются лечащим врачом. Схемы лечения назначаются индивидуально, на основании результатов анализов. Все терапия проводится под строгим лабораторным контролем.


