Брадиаритмия плода в акушерской практике: диагностика, возможности терапевтических подходов, профилактика
ФГБУ «Научный медицинский исследовательский центр акушерства, гинекологии и перинатологии имени академика В.И. Кулакова» Минздрава России, Москва, Россия
Нарушения сердечного ритма плода до недавнего времени во многих случаях являлись причиной мертворождения, неонатальной и младенческой смертности, что послужило импульсом к развитию нового междисциплинарного направления в перинатологии – фетальной кардиологии-аритмологии. В отличие от фетальных тахиаритмий, которые активно поддаются лечению, даже своевременно предпринятая терапия брадикардии далеко не всегда обеспечивает благоприятный исход. В связи с чем предикция и профилактика развития фетальной атриовентрикулярной блокады до настоящего времени являются предметом активного изучения. В обзор включены научные публикации за последние 10 лет (преимущественно систематические обзоры и метаанализы) зарубежных и отечественных авторов, обнаруженные в базе данных Pubmed и в других доступных поисковых платформах: Cochrane, Web of Science, MEDLINE, Google Scholar. Приводятся современные представления о частоте встречаемости и патогенезе брадиаритмий плода, рассмотрены различные лечебно-профилактические подходы.
Заключение. Необходимо проведение дальнейших клинико-лабораторных исследований по разработке комплексного обследования и оптимальной тактики ведения беременных с различными видами фетальных брадиаритмий.
Нарушения сердечного ритма и проводимости у плода до недавнего времени во многих случаях являлись причиной мертворождения, неонатальной и младенческой смертности, что послужило импульсом к развитию нового междисциплинарного направления в перинатологии – фетальной кардиологии-аритмологии.
Фетальные нарушения ритма, по данным литературы, встречаются с частотой от 0,1% до 5% беременностей и подразделяются на тахиаритмии с частотой сердечных сокращений выше 160 в минуту и брадиаритмии с частотой сердечных сокращений ниже 110 в минуту [1]. Среди брадиаритмий ведущее место по тяжести последствий для проводящей системы плода занимает полная атриовентрикулярная (AV) блокада сердца, которая встречается с частотой 1 на 20 000–30 000 беременностей [1, 2]. Именно AV-блокада чаще других нарушений ритма приводит к развитию неиммунной водянки, в каждом втором случае ассоциируется с врожденными пороками развития сердца плода и до 25% – с хромосомными и синдромальными патологиями [3]. Неонатальная смертность от данного вида аритмии составляет 30%, особенно в ситуации ранней манифестации, и достигает 100% при сопутствующем эндокардиальном фиброэластозе и/или дилатационной кардиомиопатии [2, 4, 5].
В то время как фетальные тахиаритмии активно поддаются лечению, даже своевременно предпринятое лечение нарушений ритма сердца плода по типу брадикардии далеко не всегда обеспечивает благоприятный исход. В связи с чем предикция и профилактика развития фетальной AV-блокады до настоящего времени являются предметом активного изучения [1].
По данным литературы, в патогенезе брадиаритмии плода описаны две большие группы этиологических факторов: фетальные (врожденные аномалии развития сердца и генетические каналопатии), вызывающие блокады проведения импульса, и материнские [2].
Врожденные пороки развития сердца (дефект предсердно-желудочковой перегородки, тетрада Фалло, корригированная транспозиция магистральных сосудов) и генетически обусловленные каналопатии (синдром Бругада, синдром слабости синусового узла, синдром длинного Q–T, синдром Андерсена–Танила) нарушают электрофизиологическую преемственность между предсердиями и желудочками, составляют до 25% всех случаев брадиаритмии [2, 6].
Материнский фактор имеет место в 3 из 4 случаев всех брадиаритмий плода и обусловлен [2, 7]:
- заболеваниями обмена веществ у матери (фенилкетонурия, сахарный диабет 2 типа);
- инфильтративными заболеваниями миокарда, связанными с трансплацентарным переходом материнских Ro/La-аутоантител;
- вирусными инфекциями (цитомегаловирус, Коксаки, аденовирус);
- приемом лекарственных средств (антиконвульсанты, ретиноиды, селективные ингибиторы обратного захвата серотонина, препараты лития, препараты аденозинпревращающего фермента);
- ишемическими заболеваниями миокарда.
Патогенез
Наибольшую распространенность – от 50% до 80% всех случаев внутриутробной брадиаритмии, по данным различных авторов [2–5], имеет аутоиммуноопосредованная брадикардия плода (АОБП), которая связана с наличием у матери аутоиммунного заболевания (синдром Шегрена, системная красная волчанка, ревматоидный артрит, антифосфолипидный синдром, заболевания соединительной ткани, недифференцированная дисплазия соединительной ткани и т.д.) или бессимптомного носительства анти-Ro/La-антител.
Описанный в литературе симптомокомплекс преходящих кожных высыпаний и AV-блокады у новорожденных от матерей с аутоиммунным ревматологическим заболеванием называется неонатальной волчанкой (НВ). В то время как некардиальные проявления волчанки у новорожденных имеют преходящий характер и проходят по мере выведения материнских антител из кровотока новорожденного, болезнь проводящей системы, по существу, необратима. Важно отметить, что в подавляющем большинстве случаев нарушение ритма сердца плода является первым сигналом о подозрении заболевания у матери и служит основанием для ее обследования [7].
Наибольшее значение в развитии ревматологических заболеваний имеют пептид SSB/La 48 кДа и два пептида SSA/Ro 52 кДа и 60 кДа, являющиеся антинуклеарными антителами [7, 8].
Антинуклеарные антитела, специфичные для ряда аутоиммунных заболеваний матери и в норме отсутствующие в организме, вырабатываются к растворимым компонентам ядра клетки – рибонуклеопротеинам (RNP).
По данным ряда авторов [7, 9], анти-Ro-антитела (SSA) и анти-La-антитела (SSB), попав в кровоток плода, могут напрямую связываться с кальциевыми каналами L-типа кардиомиоцитов и обратимо подавлять их активность. Однако в ряде случаев, по неустановленным до настоящего времени причинам, длительное воздействие данных антител приводит к интернализации кальциевых каналов, нарушая метаболизм кальция в кардиомиоцитах плода, что служит причиной апоптоза клетки. Иммуногистохимическими исследованиями было показано, что поглощение макрофагами апоптотических клеток приводит к выработке провоспалительных цитокинов, экспрессия которых, наряду с компонентами комплемента, генерирует устойчивую воспалительную реакцию в .
Нарушения ритма сердца у беременных
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Статья посвящена вопросам нарушений ритма сердца у беременных
 Нарушение ритма сердца (НРС) – это изменение нормальной частоты, регулярности и источника возбуждения сердца, а также расстройства проведения импульса, нарушения связи и/или последовательности между активацией предсердий и желудочков [1]. Беременность – физиологическое состояние организма, нередко провоцирующее НРС, частота которых, по данным разных авторов, колеблется от 5 до 18% [2, 3], из них около половины (41,7%, по данным Т.В. Шабала) имеют функциональный генез [4].
Нарушение ритма сердца (НРС) – это изменение нормальной частоты, регулярности и источника возбуждения сердца, а также расстройства проведения импульса, нарушения связи и/или последовательности между активацией предсердий и желудочков [1]. Беременность – физиологическое состояние организма, нередко провоцирующее НРС, частота которых, по данным разных авторов, колеблется от 5 до 18% [2, 3], из них около половины (41,7%, по данным Т.В. Шабала) имеют функциональный генез [4].
Механизмы НРС при беременности изучены недостаточно. Развитие беременности не сопровождается возникновением специфических электрофизиологических изменений в структурах миокарда и проводящей системе сердца, которые способствовали бы формированию или модификации субстрата основных механизмов аритмогенеза (патологического повышенного автоматизма, повторного входа волны возбуждения – «re-entry», триггерной активности) и повышали бы риск НРС. Беременность сопровождают физиологические гемодинамические изменения (увеличение объема циркулирующей крови, ударного объема, сердечного выброса, частоты сердечных сокращений), вегетативные (увеличение плазменных концентраций катехоламинов, повышение чувствительности адренергических рецепторов) и гормональные сдвиги (увеличение синтеза эстрогенов, прогестерона, простагландинов, ренина, ангиотензиногена). Все это может способствовать изменению возбудимости, автоматизма и рефрактерности миокарда, приводить к развитию и/или увеличению его электрофизиологической негомогенности и, таким образом, провоцировать возникновение НРС. Кроме того, перечисленные физиологические процессы могут усугублять гемодинамические нарушения у женщин с заболеваниями сердца, возникшими до беременности, что, в свою очередь, будет способствовать возрастанию риска развития НРС [5, 6].
Б.А. Ребров и О.А. Реброва предложили структурировать все причины, приводящие к развитию НРС у беременных [7], следующим образом:
1. Функциональные факторы, связанные с дисбалансом вегетативной нервной системы:
– физические нагрузки;
– психоэмоциональные нагрузки;
– дисгормональная перестройка организма в связи с гестацией;
– употребление продуктов, вызывающих гиперкатехоламинемию (крепкий чай, кофе, никотин).
2. Органические поражения миокарда, сопровождающиеся его гипертрофией, ишемией, кардиосклерозом, дилатацией предсердий или желудочков, развившиеся вследствие:
– заболеваний сердечно-сосудистой системы (ишемическая болезнь сердца, миокардиты, перикардиты, врожденные и приобретенные пороки, кардиомиопатии, опухоли и травмы сердца);
– патологии органов дыхания с явлениями дыхательной недостаточности;
– системных заболеваний соединительной ткани (системная красная волчанка, системная склеродермия, дерматомиозит, ревматоидный артрит, системные васкулиты).
3. Заболевания центральной нервной системы (опухоли, нарушения мозгового кровообращения) и психогенные аритмии (неврозы, психопатии, стресс-гипокалиемии).
4. Заболевания органов пищеварения (язвенная болезнь, дискинезии пищеварительного канала и желчевыводящих путей, гепатиты).
5. Заболевания эндокринной системы (тиреотоксикоз, гиперпаратиреоз).
6. Наследственные заболевания и синдромы (болезнь Фабри, Кернса – Сейра, Ленегра, Лева, аритмогенная кардиомиопатия левого желудочка (ЛЖ), синдромы преждевременного возбуждения желудочка, синдром удлиненного интервала QT, синдром слабости синусового узла и др.).
7. Нарушения электролитного обмена (гипокалиемия, гипомагниемия, гиперкальциемия, гиперкалиемия).
8. Интоксикация (алкоголь, бытовая и промышленная химия, ксенобиотики, лекарственные препараты, в т. ч. антиаритмики).
НРС чаще прогрессируют и носят более стойкий характер (резистентный к медикаментозной терапии) в случае, если аритмии выявлялись еще до беременности, а также у беременных с органическим поражением сердца. Следует отметить, что даже при отсутствии органической патологии сердца у женщин с нарушениями ритма значительно чаще встречаются осложнения беременности (злокачественные гестозы, невынашивание, гипотрофия плода) [7].
Таким образом, основными направлениями в ведении беременных с нарушениями ритма сердца являются диагностика и лечение заболеваний сердечно-сосудистой системы, органов дыхания, дисфункции щитовидной железы, а также коррекция электролитных нарушений и других патологических состояний, способствующих развитию аритмий сердца. Кроме того, необходимо выявить и устранить факторы, которые могут провоцировать НРС: употребление алкоголя, кофеина, курение, психоэмоциональные перегрузки. Во многих случаях выполнения вышеперечисленных мер оказывается достаточно для профилактики или купирования ряда аритмий либо для существенного снижения выраженности их клинических проявлений [8]. В случае выявления НРС ведение беременной продолжается совместно с врачом-кардиологом.
Основные нарушения ритма и проводимости
1. Экстрасистолия.
Наджелудочковая и желудочковая экстрасистолия – наиболее часто встречающееся НРС у беременных. Часто она протекает бессимптомно и выявляется только при плановой регистрации ЭКГ или при длительном мониторировании ЭКГ по Холтеру.
Однако у части пациенток экстрасистолия может проявляться клинически (перебоями в работе сердца, дискомфортом в грудной клетке, тревогой и т. д.). Выявление патологических факторов, способствующих развитию нарушений ритма сердца, коррекция психоэмоционального статуса позволяют устранить или в значительной степени уменьшить субъективные ощущения, что часто снимает необходимость медикаментозной противоаритмической терапии [8].
За редким исключением наджелудочковая и желудочковая экстрасистолия не является противопоказанием к естественным родам и не требует медикаментозного лечения.
Назначение антиаритмических препаратов, в первую очередь кардиоселективных -адреноблокаторов, показано в редких случаях при плохой субъективной переносимости экстрасистолии, а также у беременных с желудочковой экстрасистолией (≥10 в час) и систолической дисфункцией ЛЖ (систолическая сердечная недостаточность и/или фракция выброса ЛЖ менее 40%) [8].
2. Наджелудочковые тахикардии.
Беременность может спровоцировать развитие наджелудочковой тахикардии (НЖТ) или привести к учащению уже имевшихся пароксизмов, таких как пароксизмальная атриовентрикулярная (АВ) узловая реципрокная тахикардия, АВ-реципрокная тахикардия при наличии дополнительных путей АВ-проведения – синдром Wolf – Parkinson – White, скрытые дополнительные пути. Реже регистрируются предсердные тахикардии, в основном при органическом поражении сердца.
Если пароксизм НЖТ протекает без нарушения гемодинамики, для купирования используют вагусные приемы (проба Вальсальвы, массаж каротидного синуса) (I, С). Если вагусные приемы неэффективны, вводят в/в антиаритмические препараты, назначаемые врачом-кардиологом (АТФ (I, С), -блокаторы (метопролол, пропранолол) (IIa, С), верапамил (IIb, С)).
В случае нестабильной гемодинамики на фоне пароксизма НЖТ (сердечная астма, отек легких, гипотензия) применяется электроимпульсная терапия (I, С).
3. Предсердные тахикардии.
Современные рекомендации предлагают автоматическую, триггерную и реципрокную предсердные тахикардии объединить термином «очаговая предсердная тахикардия», которая развивается преимущественно на фоне органических заболеваний сердца, электролитных нарушений, интоксикаций (дигиталисной, алкогольной). Прогноз для больных в этом случае определяется, как правило, основным заболеванием.
Больные с асимптомными, редкими, непродолжительными пароксизмами очаговой предсердной тахикардии не нуждаются в лечении. Их надо обследовать с целью определения причины НРС и попытаться устранить ее. Фармакотерапия или немедикаментозное лечение необходимы только больным с симптомными приступами аритмии, а также при ее хроническом течении [8].
Учитывая высокую эффективность и небольшое количество осложнений, в настоящее время в лечении больных с НЖТ, в т. ч. очаговой предсердной тахикардией, предпочтение отдают интервенционным вмешательствам (радиочастотная катетерная аблация), а не антиаритмическим препаратам (эффективность профилактической антиаритмической терапии составляет всего 50–60%) [8].
4. Фибрилляция предсердий (ФП).
Основными направлениями в лечении ФП являются:
– установление причины ФП и воздействие на модифицируемые факторы: лечение гипертиреоза, прекращение приема алкоголя, устранение передозировки сердечных гликозидов, симпатомиметиков, нормализация электролитного баланса и др.;
– контроль ЧСС, купирование и предупреждение рецидивов аритмии;
– профилактика тромбоэмболических осложнений.
Короткие, асимптоматические (малосимптомные) пароксизмы ФП не требуют антиаритмической терапии. Профилактическая антиаритмическая терапия может потребоваться при устойчивых, рецидивирующих, симптомных приступах аритмии. Независимо от тактики ведения пациентки и от выбора антиаритмической стратегии проведение антитромботической терапии обязательно [8]]!
5. Желудочковая тахикардия и фибрилляция желудочков (ФЖ).
ЖТ – редкое нарушение ритма при беременности. Она может быть представлена как эпизодами неустойчивой (длительность до 30 с без нарушения гемодинамики), так и устойчивой (длительность более 30 с или гемодинамическая нестабильность) вариантами, а по морфологии комплексов QRS – мономорфной или полиморфной формами.
Развитие ЖТ и/или ФЖ наблюдается в основном у беременных с органическими заболеваниями сердца, включая кардиомиопатии, врожденные и приобретенные пороки сердца, аритмогенную дисплазию (кардиомиопатию) правого желудочка. Перипортальная кардиомиопатия должна быть исключена, если впервые ЖТ развилась в течение последних 6 нед. беременности или в ранние сроки после родов. Желудочковые тахиаритмии могут быть следствием как врожденного удлинения, так и укорочения интервала QT, синдрома Бругада, возможно также развитие катехоламинергической полиморфной («двунаправленной») ЖТ (редкая наследственная аритмия). Вместе с тем ЖТ могут наблюдаться у беременных при отсутствии органического поражения сердца и генетически обусловленных ионных каналопатий. Наиболее часто среди них встречается идиопатическая ЖТ из выносящего тракта правого желудочка. Для предупреждения симптомных рецидивов данной тахикардии назначаются -адреноблокаторы или верапамил (I, С), при неэффективности фармакотерапии или тяжелом течении аритмии рекомендуется радиочастотная катетерная аблация (IIb, С).
Купирование гемодинамически нестабильной ЖТ, а также ФЖ практически не отличается от такового у небеременных и должно включать весь комплекс мероприятий по проведению электрической кардиоверсии, дефибрилляции (I, С) и кардиопульмональной реанимации, предусмотренных соответствующими рекомендациями. Электроимпульсная терапия является безопасной для плода в любом сроке беременности [8].
Исходя из риска внезапной сердечной смерти, всех беременных с ЖТ можно разделить на две группы: пациентки с потенциально злокачественными и злокачественными желудочковыми аритмиями. К потенциально злокачественным аритмиям относятся желудочковая экстрасистолия (≥10 в час) и эпизоды неустойчивой ЖТ при наличии дисфункции ЛЖ (систолическая сердечная недостаточность и/или фракция выброса ЛЖ менее 40%). У пациенток с этими НРС еще не было эпизодов устойчивой ЖТ или ФЖ, но вероятность их развития высока. Целью лечения данной категории пациенток является снижение риска смерти – первичная профилактика (назначение -адреноблокаторов (I, С), а в случае их непереносимости или неэффективности и при отсутствии альтернативного решения – амиодарона (может оказывать отрицательное воздействие на плод, включая гипотиреоидизм, умственное недоразвитие и др.)).
Группу лиц со злокачественными желудочковыми аритмиями составляют беременные с выраженным структурным поражением миокарда и пароксизмами устойчивой ЖТ и/или успешно реанимированные по поводу ФЖ. Прогноз жизни у этих больных крайне неблагоприятен, а лечение должно быть направлено не только на устранение тяжелой аритмии, но и на продление жизни, т. е. на вторичную профилактику внезапной сердечной смерти. Для этого возможно использование амиодарона и соталола, а также комбинации -адреноблокаторов и амиодарона (с учетом вышеизложенного отрицательного влияния его на состояние плода) (IIа, С). Имплантация кардиовертера-дефибриллятора (наиболее эффективный метод вторичной профилактики внезапной сердечной смерти) может быть проведена как до беременности, так и, при необходимости, в любом сроке беременности (желательно не ранее 8-ми нед.) с использованием средств максимальной защиты плода и под контролем эхокардиографии (IIa, С) [8].
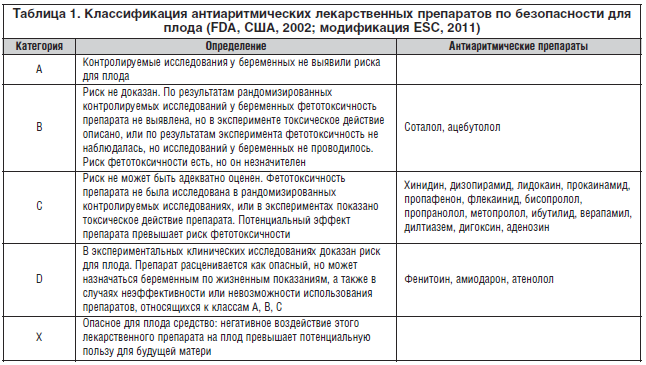
На сегодняшний день безопасных для плода противоаритмических препаратов не существует, поэтому их применяют только по строгим клиническим показаниям – при гемодинамически значимых или жизнеугрожающих НРС (табл. 1). В то же время нельзя забывать об антиаритмическом эффекте препаратов магния, которые широко назначаются беременным акушерами-гинекологами. Их применение приводит к уменьшению частоты возникновения аритмий (в т. ч. желудочковых) и обеспечивает их профилактику [9].
6. Нарушение проводимости сердца.
Нарушения проводимости (блокады) сердца возникают при замедлении или полном прекращении проведения электрического импульса из синусового узла по проводящей системе сердца. Выделяют следующие виды блокад:
– синоатриальную;
– внутрипредсердную;
– атриовентрикулярные: I, II (Мобитц I, Мобитц II) и III степени;
– блокады ветвей пучка Гиса.
Причинами возникновения синоатриальной и внутрипредсердной блокад могут быть воспалительные, склеротические, дегенеративные изменения миокарда предсердий, передозировка лекарственных препаратов (-адреноблокаторов, сердечных гликозидов и др.), электролитные нарушения. Эти виды блокад наблюдаются и у практически здоровых лиц при ваготонии.
Синоатриальные блокады в подавляющем случае бессимптомны и не требуют специального лечения. Синоатриальные блокады с симптомной брадикардией (пресинкопе, синкопе) являются показанием для имплантации искусственного водителя ритма.
АВ-блокады характеризуются нарушением проведения импульса от предсердий к желудочкам. При беременности чаще всего встречаются АВ-блокады, которые в большинстве случаев носят врожденный характер. Они, как правило, протекают бессимптомно и не осложняют течение беременности и родов. Вероятным этиологическим фактором является первичное генетически детерминированное заболевание проводящей системы сердца (во многих случаях прослеживается семейный характер заболевания).
Другими причинами поражения проводящей системы сердца являются болезнь Ленегра, болезнь Лева, синдром Кернса – Сейра, болезнь Фабри. Причинами развития блокад у пациенток, кроме того, являются: врожденные и приобретенные пороки сердца, кардиомиопатии, операции на открытом сердце. У практически здоровых лиц может быть блокада правой ножки пучка Гиса.
У беременных с симптомами, связанными с синдромом слабости синусового узла, нарушениями АВ-проводимости II–III степени (пресинкопе и синкопальные состояния) требуется выполнение временной или постоянной эндокардиальной стимуляции сердца [8].
Таким образом, НРС, нередко сопровождающие беременность, требуют своевременной диагностики и устранения провоцирующих их факторов. Сбалансированное питание, нормализация режима сна и бодрствования, коррекция психоэмоционального статуса – всего этого, как правило, оказывается достаточно для уменьшения частоты возникновения НРС, улучшения их переносимости, а также в целях профилактики.
Кардиотокография (КТГ) в диагностике состояния плода. Лекция для врачей
Лекция для врачей “Кардиотокография в диагностике состояния плода”. Лекцию для врачей проводит заведующая родильным отделением, МУЗ «Городская клиническая больница СМП г. Ставрополя», врач высшей категории, к.м.н Гюсан О. А.
На лекции рассмотрены следующие вопросы:
- Диагностика состояния плода во время беременности
- Контроль за двигательной активностью плода
- Кардиотокография
- Допплерометрия кровотока в системе мать – плацента – плод
- Амниоскопия
- Амниоцентез
- Кардиотокография
- КТГ выполняется в норме 1 раз в 7-10 дней
- При нарушении МППК (маточно-плацентарного кровотока) 1 раз в 2-3 дня
- Необходимо 3-4 последовательных исследования для точной постановки диагноза
- Ведение тренда (вариабельность ритма, STV, базальный ритм)
- Выполняется с 32 недель беременности. Технически выполнимо с 28 недель
- Допплерометрия
- Достоверность повышается при наличии СЗРП (синдром задержки развития плода)
- Достоверность в III триместре беременности 2%
- Совпадение результатов КТГ и допплерометрии практически в 100% случаев свидетельствует о наличии здорового плода или нарушении его состояния
- При расхождении данных предпочтение следует отдавать автоматизированной кардиотокографии
- Кардиотокография
- Запись проводится не менее 40 мин. При необходимости запись продолжается до 1 часа
- При соблюдении критериев Доуза-Редмана, нормальном STV, отсутствии патологических ритмов, положительном нестрессовом тесте запись можно сократить до 10-20 мин
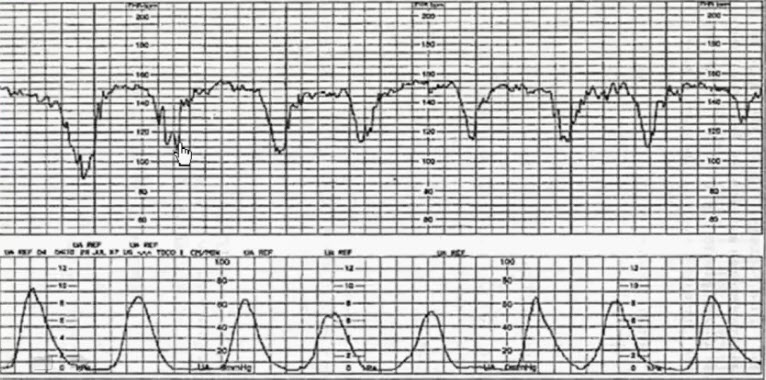
- Оценивается: базальная частота, амплитуда и частота осцилляции, наличие и амплитуда акселераций, наличие и выраженность акселераций, двигательная активность плода
- Базальный ритм – средняя частота СС, сохраняющуюся неизменной за период равный 10 мин и более
- КТГ во время беременности (норма)
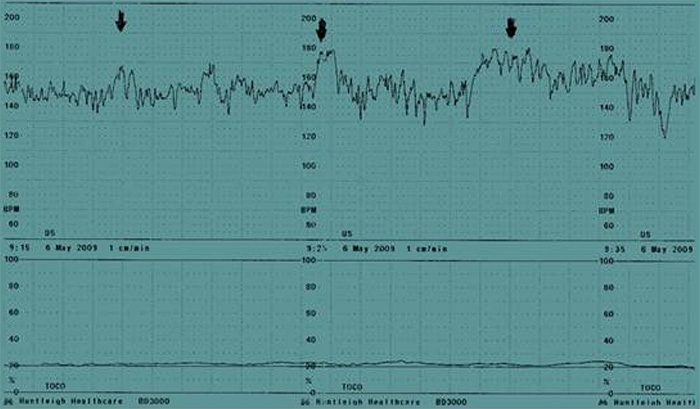
- Базальный ритм
- Норма – 120 – 160 ударов в минуту
- Может быть в границах 110-120, 160-170, если остальные характеристики ритма отвечают нормативным требованиям
- Ритм должен иметь стабильную базальную частоту
- Повышению базального ритма способствует повышение температуры, прием гинипрала, тахикардия у матери. В родах тахикардия плода может быть признаком хорионамнионита
- Плавающий базальный ритм – прогностически неблагоприятный признак
- Диагноз: беременность 39 нед. Гестоз легкой степени. ХФПН. Околоплодные воды светлые. Через 2 часа роды, масса 2940 г, 7/8 баллов
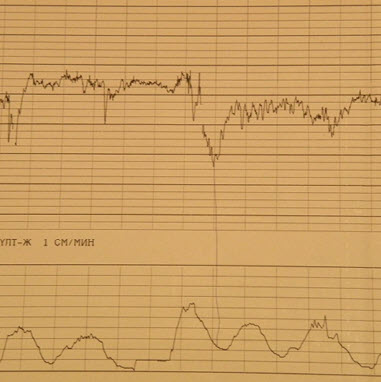
- Высокий базальный ритм
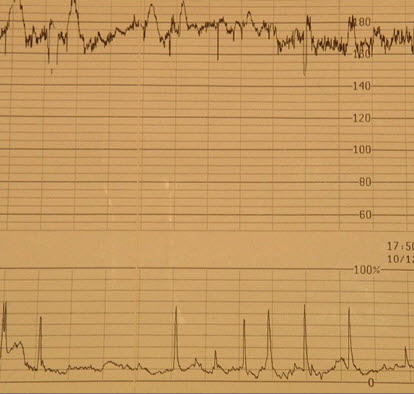
- Низкий базальный ритм
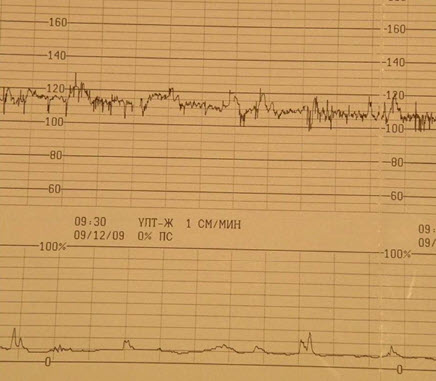
- Вариабельность сердечного ритма – амплитуда – частота
- Вариабельность
- Амплитуда
- Низкоамплитудные (3 – 6 уд/мин)
- Среднеамплитудные (6 -15 уд/мин)
- Высокоамплитудные
- Частота
- Низкочастотные (0-4)
- Среднечастотные (4 – 8)
- Высокочастотные (более 8)
- Амплитуда
- Вариабельность сердечного ритма
- Наличие высоких осцилляций свидетельствует об удовлетворительном состоянии плода
- Физиологическому ритму присущ среднеамплитудный, но высокочастотный осцилляторный ритм
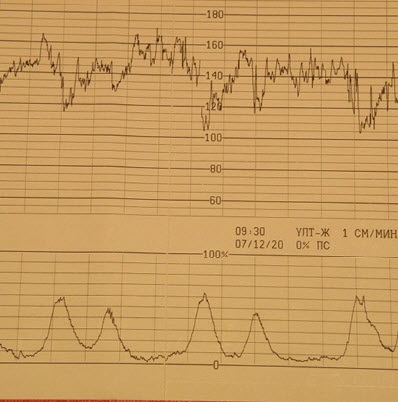
- Высокоамплитудный ритм
- Диагноз: беременность 38 нед. Роды, срочные. Околоплодные воды светлые. Через 1 ч. роды, масса 3540 г, 8/8 баллов
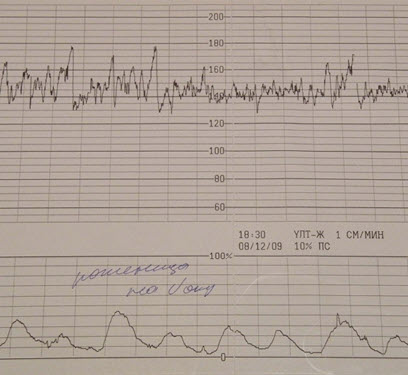
- Среднеамплитудный ритм
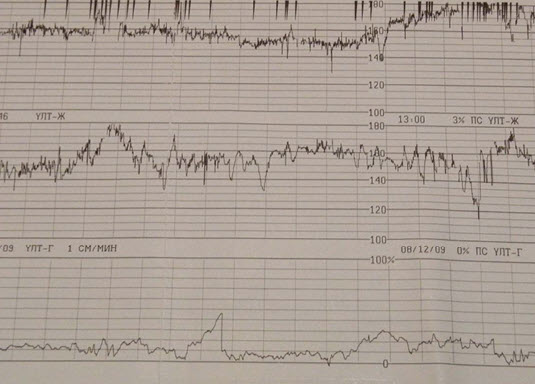
- Акселерации-увеличение ЧСС на 15 и более уд./мин и продолжительностью более 15 сек по сравнению с базальным ритмом
- Спорадические (вариабельные)
- Тревожные признаки
- Периодические (униформные) – совпадают с маточными сокращениями. При сочетании с тахикардией-начальные признаки гипоксии – повторное КТГ
- Пролонгированные – повторное КТГ
- Тревожные признаки
- Спорадические (вариабельные)
- Пролонгированные акселерации
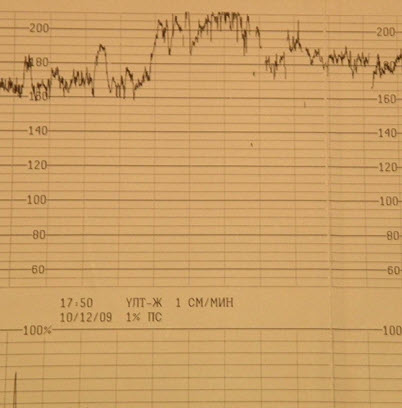
- Децелерации – замедление ЧСС на 15 уд./мин и более и продолжительностью 15 сек и более
- DIP 0 – пикообразные, кратковременные
- Тревожные признаки
- DIP I- возникновение с началом схватки (часто при компрессии пуповины). При сочетании с условно- патологическими ритмами свидетельствует о наличии дистресс-синдрома
- DIP III вариабельная децелерация
- Патологические признаки
- DIP II -поздняя децелерация
- DIP I
- Диагноз: беременность 37 нед. Роды 2, срочные.
ХФПН. Многоводие. Околоплодные воды светлые. Через 1 ч роды , масса 3500 г, 8/8 баллов
- Диагноз: беременность 37 нед. Роды 2, срочные.
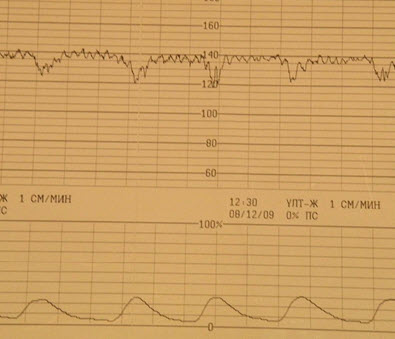
- DIP I
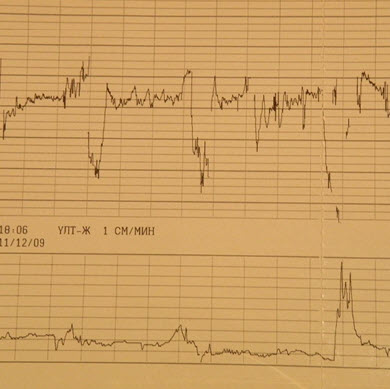
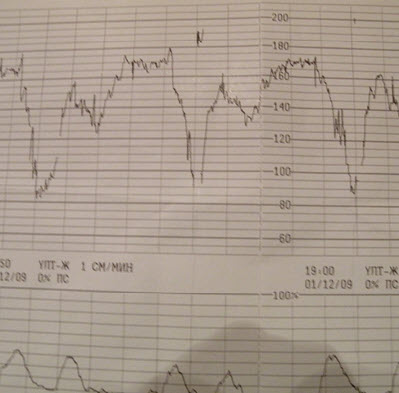
- DIP II -поздняя децелерация
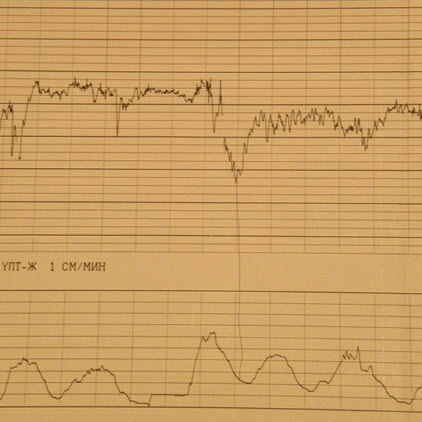
- DIP 0 – пикообразные, кратковременные
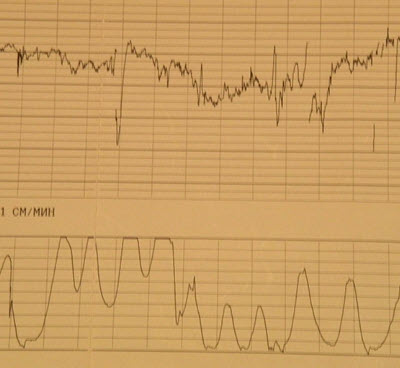
- Патологические ритмы
- Линейный (с-м сдавления н/полой вены порок развития ЦНС, выраженная ХФПН)
- Синусоидальный (терминальное состояние плода, гемолитическая болезнь)
- Проваливающийся (сочетание линейного ритма с периодическим колебанием базальной частоты). Часто наблюдается при недоношенных беременностях
- Линейный
- КТГ во время беременности: монотонный ритм, отсутствие акцелераций (начальные признаки гипоксии плода)
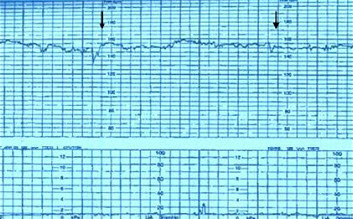
- Линейный
- Диагноз: беременность 39 нед. Роды 1, срочные. ХФПН, декомпенсация. Околоплодные воды светлые. ОКС в экстренном порядке, масса 3100г, 6/7 баллов. Тугое обвитие пуповины в/г шеи
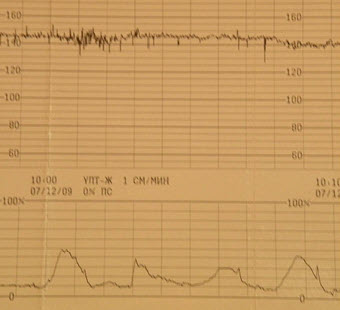
- Синусоидальный
- КТГ во время беременности – синусоидальный ритм (выраженная гипоксия плода)
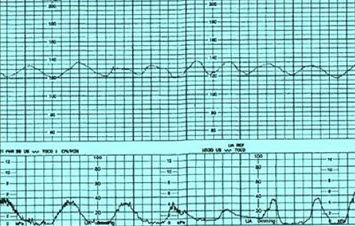
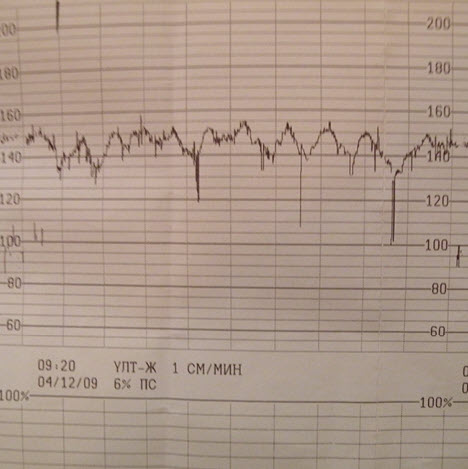
- Тревожные (условно-патологические ритмы)
- Низкоосцилляторный (гипоксия, седация)
- Высокоосцилляторный – данный ритм указывает. Что имеется какое-то неблагополучие, а с другой стороны свидетельствует о том, что резервы плода пока еще достаточны.
- Высокоосцилляторный с плавающей базальной частотой
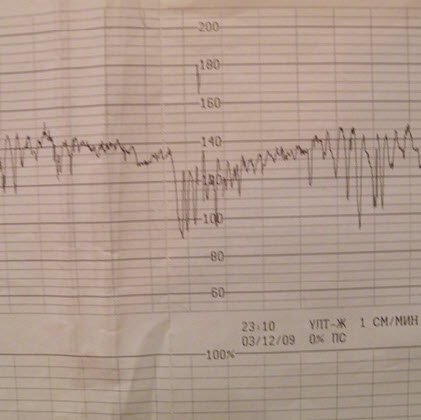
- Низкоосцилляторный
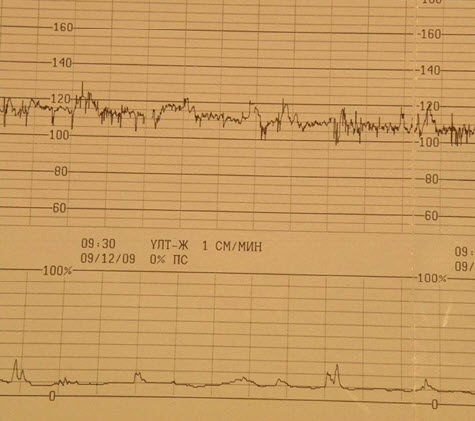
- Низкоосцилляторный
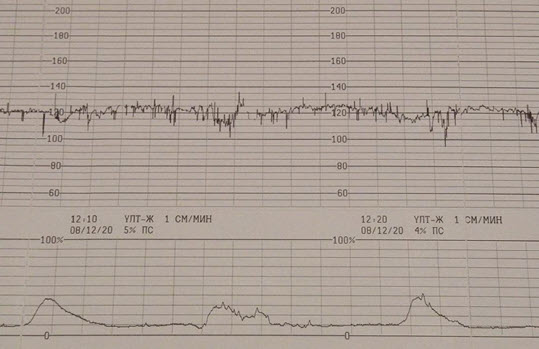
- Тревожные (условно-патологические ритмы)
- Дыхательный ритм – зрительно представляет собой ровную или волнообразную изогнутую ленту, выполненную отметками о сердечных ударах, в которых невозможно выделить какие бы то ни было упорядоченные комплексы. Для уточнения состояния плода необходимо было выполнить биофизический профиль плода, допплерометрию. Если ритм при повторных исследованиях повторяется, то с высокой степенью вероятности можно ожидать рождение ребенка с аспирацией, врожденной пневмонией
- Дыхательный ритм
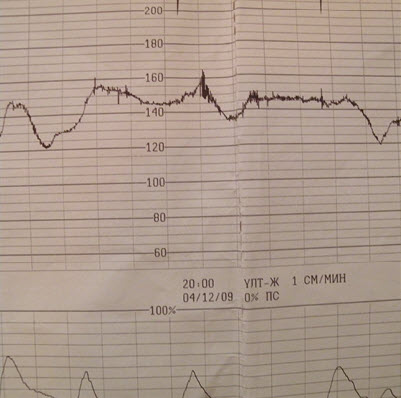
- Тревожные (условно- патологические ритмы)
- Экстрасистолический – записывается как две или три параллельные тахограммы, по типу бигеминии или тригемении. Выполняется биофизический профиль плода, УЗИ с целью исключения пороков сердца, допплерометрия
- Тревожные (условно-патологические ритмы)
- Гармоничный характеризуется теми же параметрами, что и осцилляторный, за исключением присутствия в нем тождественных друг другу медленных осцилляций. Каждая последующая по своим параметрам напоминает предыдущую. При наблюдении в динамике нередко отмечается снижение амплитуды и частоты осцилляций
- Гармоничный тип
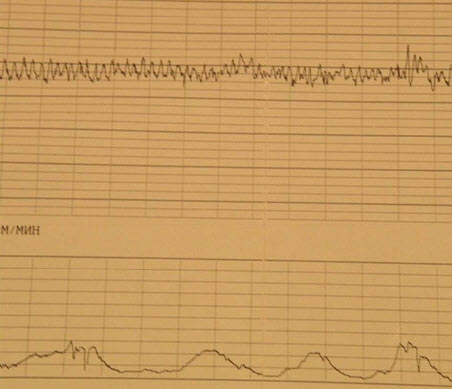
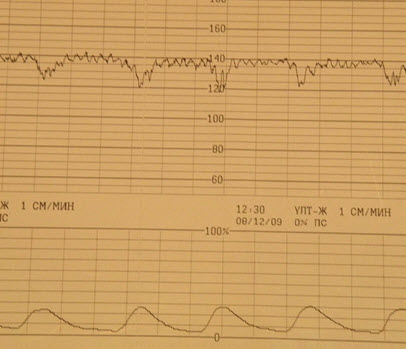
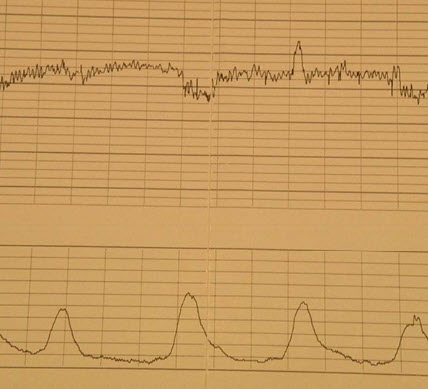
- Согласно критериям ВОЗ (1985): нормальная кардиотокография
- базальный ритм в пределах 110-150 уд./мин
- амплитуда вариабельности сердечного ритма – 5-25 уд./мин
- децелерации отсутствуют или выявляются спорадические, неглубокие и очень короткие
- регистрируются 2 и более акцелерации на протяжении 10 мин. записи. Если такой тип КТГ обнаруживается за короткий период исследования, запись можно не продолжать
- Критерии Доуза-Редмана
- отсутствие децелераций
- наличие минимум одного шевеления плода или трех акцелераций
- отсутствие признаков синусоидального ритма STV 3 мсек, или более
- наличие либо акцелерации, либо эпизода высокой вариабельности
- отсутствие децелераций или ошибок в конце записи
- «Подозрительная» кардиотокограмма
- базальный ритм в пределах от 110 до 100 или от 150 до 1/0 уд./мин
- амплитуда вариабельности базального ритма – между 5 и 10 уд./мин. более чем за 40 мин. исследования или более 25 уд/мин
- отсутствие акцелераций более чем за 40 мин. записи
- спорадические децелераций любого типа, кроме тяжелых. При обнаружении таких признаков на кардиотокограмме должен быть проведен любой из стрессовых тестов
- Патологический тип
- базальный ритм менее 100 или более 170 уд./мин
- вариабельность базального ритма менее 5 уд./мин, наблюдаемая на протяжении более чем 40 мин. записи
- повторяющиеся выраженные ранние децелераций или вариабельные децелераций
- поздние децелераций любой конфигурации
- синусоидальный тип кривой, характеристиками которого является наличие частоты менее чем 6 осцилляций в мин., амплитудой менее 10 уд./мин и продолжительностью 20 мин и более
- STV (short-term variation, т.е. «короткая вариабельность»)
- STV менее 5 мсек, необходимо интерпретировать как признак низкой вариабельности
- STV более 10 мсек. – аналогичен регистрации сальтаторного типа вариабельности
- Если критерии Доуза-Редмана не соблюдены, но STV более 4,5 – признаков гипоксии нет
- Норма STV – 4 и более
- STV 3-3,5 – признаки тканевой и метаболической гипоксии
- При STV 2,5 – экстренное родоразрешение путем операции кесарево сечение
- Бальные системы оценок КТГ (эффективность 75 %)
- Для оценки состояния плода при беременности
- Фишер (1976г)
- Кребс (1978г)
- Лионе (1979г)
- Готье (1982г)
- Отт (1989)
- Макаров (1997)
- Для оценки состояния плода в родах
- Соломатина (1980)
- Савельевой (1981)
- Для оценки состояния плода при беременности
- Функциональные пробы
- нестрессовый тест (положительный, отрицательный, сомнительный)
- окситоциновый контрактильный тест
- маммарный стрессовый тест
- степ-тест
- тест со звуковой стимуляцией
- Выводы:
- Кардиотокография, при всей своей высокоинформативности, неприменима для прогнозирования перинатальных исходов
- Данные, свидетельствующие об отсутствии гипоксического состояния плода на момент исследования, не говорят о том, что это состояние не возникнет в родах
- Благоприятные результаты КТГ сохраняют свою актуальность в течение недели
- При признаках умеренной гипоксии – КТГ необходимо повторять каждые сутки
- Данные КТГ используются только в совокупности с данными других методов исследования
Дополнительный материал
Лекция для врачей “Кардиотокография (монитор плода)”. Лекцию для врачей проводит гинеколог Жушман Владимир Владимирович
На лекции рассмотрены следующие вопросы:
- КТГ метод регистрации сердечной деятельности плода, наиболее точно характеризующий функциональное состояние плода в анте- и интранатальном периодах
- Современные кардиомониторы регистрируют: сердечную деятельность плода, сокращение матки, движение плода
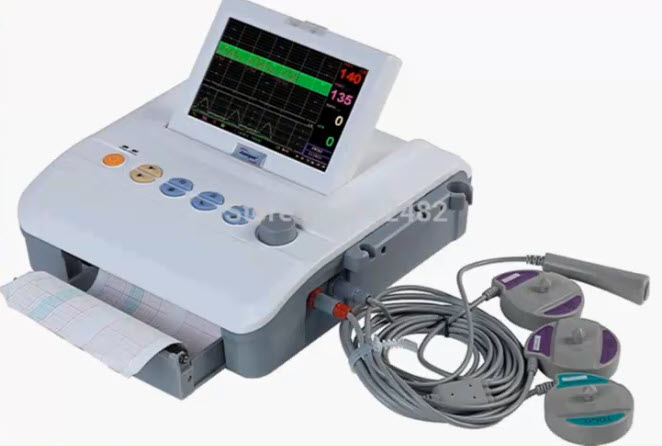
- Датчик записи сердечной деятельности: основан на принципе допплера (ультразвуковой датчик)

- Датчик записи сократительной деятельности матки

- Запись
- Положение пациентки: полусидя или на бок (сдавление нижней полой вены лежа)
- Ультразвуковой датчик устанавливают на переднюю брюшную стенку в зоне наибольшей слышимости сердечных тонов плода
- ТОКО датчик устанавливают в области дна матки
- Датчик движения плода помещается в руку (пациентка самостоятельно отмечает шевеление)
- Оценка КТГ (нестрессовый тест)
- Базальный ритм (120-160 в мин.) Средняя величина
- Тахикардия >160
- Брадикардия 15 ударов в течении >15 сек.
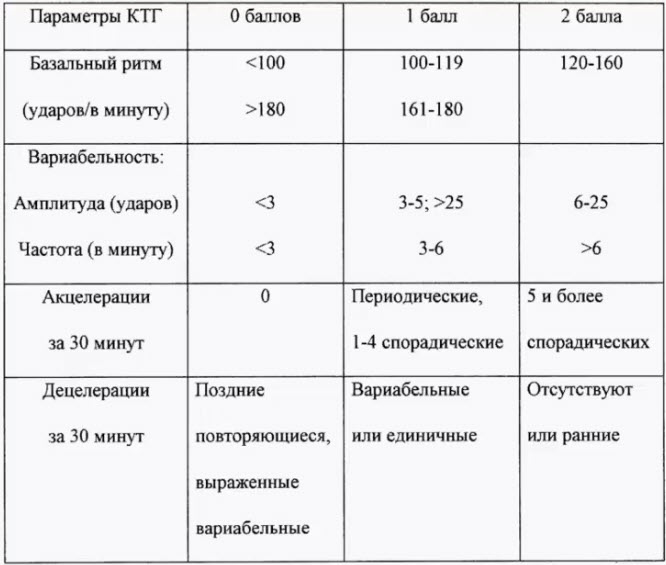
- Шкала Фишера

- Стрессовый тест (окситоциновый тест): реакция сердечной деятельности в ответ на сокращение матки. Скорость введения окситоцина 0.01 ЕД в мин в физ. растворе. Противопоказания: предлежание плаценты, излитие околоплодных вод, рубец на матке, отслойка плаценты
- За 10 мин. 3 схватки – позитивный стрессовый тест в случае наличия поздних децелераций. Это плохо.

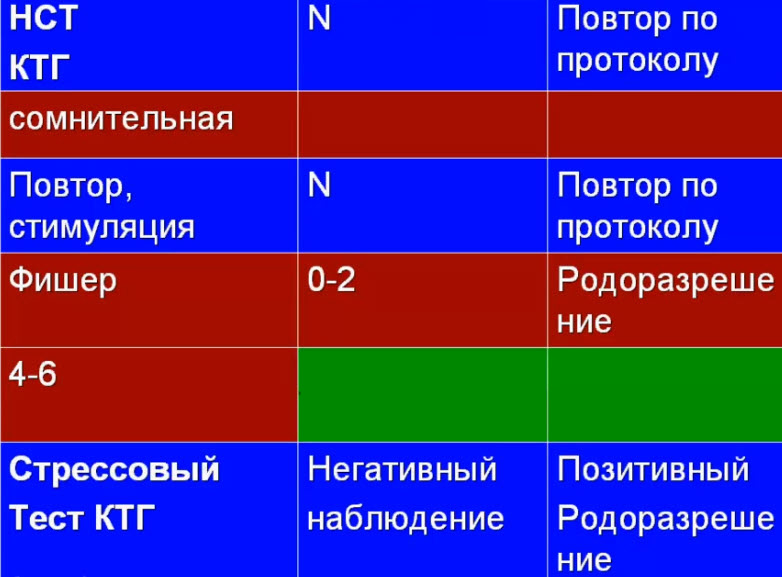
- Алгоритм ведения пациенток после КТГ

Брадикардия плода при беременности: насколько опасна и что делать?

Многие женщины сталкиваются с таким опасным явлением, как брадикардия плода при беременности. Это аномальное снижение частоты сердцебиения, которое провоцирует недостаточное насыщение мозга и других органов будущего ребенка кислородом. Потенциально это способно привести к смерти эмбриона или необратимым изменениям в его мозгу. Насколько опасна брадикардия плода, какие факторы способствуют ее появлению и можно ли снизить риск? На эти вопросы попробуем ответить в данной статье, также охарактеризовав пути решения этой проблемы.
Брадикардия плода: причины и симптомы

Не всякое снижение пульса у человека является аномалией или патологией. Например, оно наблюдается во время сна или при снижении температуры окружающей среды – в такие моменты организм экономит энергию, обмен веществ замедляется. Также подобное явление наблюдается у спортсменов, а у некоторых людей оно имеется с рождения, но не имеет характера патологии. В таких случаях говорят о физиологической брадикардии. Важным ее отличие от аномальной является отсутствие патологических симптомов.
Аномальная брадикардия – это такое снижение частоты сердечного ритма, при котором возникают различные болезненные состояния организма: головокружение, холодная потливость, потеря сознания и т. д. Как правило, они проявляются при сильном сокращении сердцебиения. Если оно незначительно, то субъективных ощущений у человека может не возникать.
Чтобы судить о наличии брадикардии сердца у плода, необходимо иметь представление о физиологической норме частоты сердцебиения. У взрослого человека она составляет 60-80 ударов в минуту, у эмбриона же изменяется в ходе его развития:
- На 3-5 неделе – 75-80;
- На 5-6 неделе – 80-100;
- На 6-7 неделе – 100-120;
- На 7-9 неделе – 140-190;
- На 10-12 неделе – 160-180;
- На 4 месяце – 140-160;
- К 9 месяцу – 130-140.
Указанные значения не являются точными, так как физиологическая норма у каждого ребенка может незначительно различаться. Примерно до 21 дня беременности сердцебиение у эмбриона не прослушивается вообще – на этом этапе у него его собственное сердце еще не начало формироваться, а обмен веществ полностью обеспечивается кровотоком матери.
Однозначно диагностировать патологическую брадикардию у матери и плода можно только во 2 триместре (после 20 недель вынашивания), так как на этом этапе его собственная система кровоснабжения в целом уже сформировалась, поэтому пульс должен стабилизироваться. Врач ставит диагноз в том случае, если в данный период частота сердцебиения составляет менее 110-120 ударов в минуту.
Брадикардия может быть «материнским» заболеванием или наблюдаться только у плода. В первом случае замедление сердцебиения у самой женщины также сказывается на состоянии будущего ребенка, во втором патология эмбриона не сказывается на здоровье матери. Причинами заболевания со стороны матери являются:
- заболевания сердечно-сосудистой системы – атеросклероз, нестабильное артериальное давление, ишемическая болезнь сердца, кардиосклероз, дистрофия или воспаление миокарда (сердечной мышцы);
- общие заболевания организма – нарушение кроветворной функции костного мозга, опухоли, анемия, инфекционные патологии, почечная недостаточность и т. д.
Со стороны плода причинами брадикардии выступают следующие патологии:
- материнская анемия, высокая токсичность окружающей среды, психический стресс у женщины;
- пороки развития собственной сердечно-сосудистой системы плода;
- нарушения репродуктивной системы матери – ранее старение плаценты, аномальное накопление околоплодных вод и т. д.;
- резус-конфликт – несовместимость материнской и эмбриональной крови по резус-фактору;
- интоксикация материнского организма из-за курения, употребления алкоголя или наркотиков, некоторых видов лекарств.
Симптомами брадикардии у матери являются типичные признаки кислородного голодания – головокружение, слабость, головная боль, шум в ушах, боль в груди, пониженное давление, одышка. Если патология наблюдается только у плода, о ней будут свидетельствовать снижение или прекращение его двигательной активности, а также судороги. Особенности эмбриональной формы заболевания в том, что выявить ее по состоянию матери невозможно – только непосредственно наблюдением за самим ребенком с помощью современных средств диагностики.
Беременность у пациенток с брадикардией характеризуется высоким риском гипоксии плода. Продолжительное кислородное голодание способно привести к замершей беременности, выкидышу или необратимым нарушениям в организме будущего ребенка. Особенно сильно от этого страдает его мозг, так как нервные клетки наиболее чувствительны к недостатку кислорода.
Виды брадикардии у плода

По характеру и интенсивности снижения частоты сердечных сокращений у плода различаются следующие разновидности патологии:
- Базальная – диагностируется при снижении ЧСС эмбриона до менее 120 раз в минуту, при своевременной помощи вреда для ребенка и самой матери можно избежать;
- Децелерантная – такая брадикардия ставится, если частота эмбрионального сердцебиения не более 72 ударов в минуту, при этом женщине назначается лечение в стационаре с постельным режимом;
- Синусовая – при ней пульс плода снижается до 70-90 ударов в минуту, такое состояние является наиболее опасным, поэтому женщине требуется срочная госпитализация и интенсивное лечение вплоть до самых родов.
Определение точного вида и причины брадикардии имеет большое значение, так как от этого зависит, насколько велика опасность для ребенка и матери, какую стратегии терапии следует выбрать для лечения заболевания или хотя бы снижения рисков.
Диагностика брадикардии у плода
Если с выявлением нарушений сердечного ритма у самой матери проблем не возникает, то в случае эмбриональной брадикардии ситуация сложнее. Обнаружить патологию можно только путем наблюдения за самим плодом. Для этого применяются следующие методы:
- Аускультация. Это прослушивание сердцебиения плода с помощью стетоскопа. Оно проводится снаружи через брюшную стенку матери. Это самый простой, но и наименее надежный способ диагностики, так как на показания влияет наличие у женщины жировой прослойки, а также двигательная активность плода.
- УЗИ. Ультразвуковое исследование позволяет не только услышать сердцебиение плода, но и визуализировать сам эмбрион. УЗИ может проводиться абдоминально (через брюшину) или трансвагинально (с введением датчика во влагалище). При этом врач получает данные о характере и интенсивности двигательной активности плода, частоте его дыхания и сокращений сердца.
- КТГ (кардиотокография). Это один из самых точных способов диагностировать брадикардию у плода на поздних сроках. Он заключается в записи пульса эмбриона и его сопоставлении с частотой сокращений матки матери. Оценка происходит по 10-бальной шкале: при 8-10 баллах патологии не выявляется, при 6-8 – диагностируется легкая аномалия, а при менее 6 баллах – тяжелая форма. Преимуществом КТГ является возможность использования этого метода при наличии у матери эндокринных и сердечно-сосудистых нарушений.
- ЭКГ (электрокардиография). Данный метод заключается в регистрации электрических импульсов сердца плода, часто в сочетании с записью сердечных шумов (фонокардиографией). Полученные данные в реальном времени отображаются в виде кардиограммы – линейных графиков на бумажной ленте. На брадикардию указывает наличии в них Р-зубца и увеличенных интервалов Т-Р и Т-Q.
В зависимости от степени выраженности заболевания проводятся некоторые из этих тестов или они применяются комплексно. Направление на их прохождение дает врач, ориентируясь на состояние матери, ее возраст, наличие у нее подобных проблем при прошлых беременностях и т. д.
Профилактика и лечение брадикардии плода

К брадикардии склонны женщины с хроническими заболеваниями сердечно-сосудистой, эндокринной, пищеварительной систем, ожирением, психическими расстройствами. Факторами риска также являются:
- Постоянный эмоциональный стресс – например, из-за напряженной работы, нездоровой обстановки в семье (в том числе физического и сексуального насилия);
- Физический дискомфорт – в частности, регулярное поднятие тяжестей, занятия спортом, работа или проживание в высокотоксичной среде, нарушения питания;
Лечение этого заболевания зависит от его интенсивности, риска для здоровья матери и плода, причин появления. Основная цель терапии заключается в устранении провоцирующего фактора, снижении опасности для женщины и будущего ребенка:
- При легкой брадикардии врач назначает профилактические меры – прогулки на свежем воздухе, малоинтенсивные физические упражнения, прием минерально-витаминных комплексов, диетическое питание и т. д. В этом случае будущая мать не остается на лечении в стационаре, лишь проходит регулярные обследования.
- Тяжелая брадикардия может привести к потере беременности, поэтому пациентка помещается на сохранение в больничный стационар. Врач назначает лечение основного заболевания матери, вызывающего патологию, параллельно стимулирует плацентарный кровоток, чтобы уменьшить или исключить гипоксию плода. Однако, даже если эти проблемы решены, женщина остается под наблюдением до конца беременности. Обычно в таких случаях назначается кесарево сечение, так как естественные роды ребенок может просто не пережить.
Выявление брадикардии плода на ранних сроках – залог успешного лечения этого заболевания. Поэтому всем беременным женщинам, даже если они не входят в группу риска и не имеют видимых симптомов патологии, рекомендуется регулярно посещать акушера-гинеколога и проходить медицинские обследования.
Сердцебиение плода: норма
Главный показатель, на основании которого можно оценить жизнеспособность и динамику состояния будущего ребенка – сердцебиение плода. Норма сердечных сокращений существует для каждого срока беременности, начиная с 5 недели, и любое отклонение в состоянии плода может свидетельствовать о развитии неблагоприятной ситуации. Особенно важным моментом является контроль за сердечной деятельностью малыша во время родов, так как на основании данных о частоте и характере сердцебиения плода принимается решение о необходимости вмешательства в процесс родоразрешения.
Причины нарушения сердечного ритма
Тахикардия (учащенное сердцебиение с частотой более 200 уд/мин) может быть вызвано: нервными переживаниями матери, значительными физическими нагрузками, анемией, нахождением в душном помещении. Чаще всего причины нарушения сердечного ритма – развитие кислородной недостаточности у плода. Небольшое учащение сердцебиения плода во время схваток считается нормальным.
Серьезный сигнал – диагностика приглушенного сердцебиения плода. Данная патология может свидетельствовать о плацентарной недостаточности, неправильном предлежании малыша или расположении плаценты, гипоксии, избытке или недостатке околоплодных вод либо чрезмерной двигательной активности малыша. Если беременная женщина имеет избыточный вес, причиной приглушенного сердцебиения может быть ожирение матери.
Еще одно возможное отклонение – слабое сердцебиение. В этом случае во II и III триместрах вероятна гибель плода ввиду развития хронической гипоксии. Если слабое сердцебиение отмечается в первом триместре беременности, причина может быть в неправильном определении ее срока.
Если у эмбриона размером от 5 мм сердцебиение не прослушивается, наиболее распространенная причина – неразвивающаяся беременность или внутриутробная гибель плода. При постановке такого диагноза необходимо проведение УЗИ исследований, и на основании их результатов принимается решение о выскабливании матки, осуществлении искусственных родов либо проведении операции по разрушению плода.
Методы измерения сердцебиения и нормы
Когда измеряется сердцебиение плода, норма определяется с учетом срока беременности, определенного врачом. Для 6-8 недель нормой считается 110-130 ударов в минуту, для срока в 9-10 недель – 170-190 ударов, а с 11 до 42-й недель – от 140 до 160 уд/мин. На разных этапах развития плода динамика сердечных сокращений меняется в результате совершенствования вегетативной нервной системы ребенка и усложнения структуры сердца.
Чтобы диагностировать состояние плода и ход течения беременности или родов, используются следующие методы измерения сердцебиения и нормы. Каждый метод дает абсолютно достоверную информацию, однако выбор наиболее подходящего способа диагностики зависит от срока беременности.
Применение УЗИ аппарата – лучший способ контролировать частоту сердцебиений ребенка в самом начале беременности. Применение трансвагинального датчика позволяет зафиксировать динамику сердечных сокращений эмбриона уже с 5 недель беременности, а использование классического трансабдоминального УЗИ аппарата показывает первые результаты с 6-7 недель.
Аускультация
Выслушивание частоты сердцебиений плода с использованием специальной трубочки – стетоскопа является наиболее простым способом диагностики состояния плода. Акушерская трубка размещается на животе у беременной со стороны широкой воронки. К другой стороне трубки врач прикладывает свое ухо. Услышать сердечную активность плода с помощью стетоскопа можно уже с 18-й недели беременности. В процессе схваток акушер прибегает к аускультации 3-4 раза в час, чтобы контролировать состояние ребенка.
Кардиотокография
Уже с 32-й недели беременности допускается проведение кардиотокографии, которая позволяет одновременно регистрировать и сердечные сокращения плода, и динамику активности матки. Некоторые кардиомониторы позволяют одновременно с этими исследованиями регистрировать двигательную активность ребенка. Кардиотокография может проводиться до родов и в процессе схваток при наличии некоторых патологий в состоянии матери или плода.
Эхокардиография
Надежный способ диагностики сердечной активности плода при сроке беременности от 18 до 28 недель. Эхокардиография проводится комплексно и предусматривает несколько режимов функционирования сканера УЗИ аппарата: М-режим и режим Допплера. В результате удается дополнительно проанализировать структуру сердца и крупных сосудов. Эхокардиография проводится только при наличии у беременной соответствующих показаний.
Нарушения ритма сердца и проводимости у беременных. Клиническое наблюдение
М.М. МАНГУШЕВА, Т.В. РУДНЕВА, С.П. ЯКУПОВА, Н.Г.ШАМСУТДИНОВА, Л.С. ШАМЕЕВА
Казанский государственный медицинский университет
Республиканская клиническая больница МЗ РТ, Казань
Шамсутдинова Наиля Гумеровна —
кандидат медицинских наук, ассистент кафедры госпитальной терапии КГМУ
420049, г. Казань, ул. Бутлерова, д. 49, тел. 7 (904) 7638372, e-mail: nailya@e-diva.ru
Нарушения ритма при беременности представляют особую медицинскую проблему, поскольку могут вызвать нарушения жизнедеятельности плода. В статье описываются актуальные вопросы диагностики нарушения ритма сердца при беременности, возможности медикаментозной и немедикаментозной коррекции. Приведена демонстрация клинического наблюдения.
Ключевые слова: нарушения ритма сердца, беременность.
M.M. MANGUSHEVA, T.V. RUDNEVA, S.P. YAKUPOVA, N.G. SHAMSUTDINOVA, L.S. SHAMEEVA
Republican Clinical Hospital of the Ministry of Health of the Republic of Tatarstan, Kazan
Disturbances of a heart rhythm and conductibility of pregnant. Clinical study
Rhythm disturbances during pregnancy are the special medical problem as they may cause fetus life activity disturbances. The article describes the current problems of heart rhythm disturbances of pregnant, possibilities of drug and non-drug correction. Is demonstrated a clinical study.
Key words: heart rhythm disturbances, pregnancy.
Нарушение ритма сердца (НРС) — это изменение основных электрофизиологических свойств сердца (автоматизма, возбудимости, проводимости), ведущее к нарушению координированного сокращения всего сердца или его отделов и проявляющееся изменением частоты, регулярности ритма и проведения возбуждения по проводящей системе сердца. Довольно часто (от 5,1% до 38,7%) у практически здоровых беременных могут возникать разнообразные нарушения ритма. Они представляют собой серьезную медицинскую проблему, что обусловлено рядом причин. Во-первых, сами аритмии способны создавать угрозу здоровью и жизни беременной женщины и плода. Во-вторых, частота аритмий во время беременности увеличивается, что обусловлено значительными физиологическими изменениями в организме матери. Беременность самостоятельно может выступать в качестве проаритмогенного фактора [1].
Механизмы развития нарушений ритма у беременных связаны с функциональными, гормональными и гемодинамическими изменениями, которые происходят во время беременности. У беременных в несколько раз повышается уровень эстрогена и хорионического гонадотропина. Кроме того, высокое содержание катехоламинов в плазме крови и рост чувствительности адренорецепторов приводит к чрезмерной активации симпатической нервной системы. Все эти изменения у беременных создают благоприятные условия для развития аритмий.
Диагностика нарушений ритма сердца и динамическое наблюдение при беременности существенно не отличаются от таковых у небеременных. Беременные с жалобами на сердцебиение, «перебои» в работе сердца, а также здоровые беременные с бессимптомными аритмиями, обнаруженными на электрокардиограмме, должны проходить тщательное обследование, включающее холтеровский суточный мониторинг ЭКГ и при необходимости электрофизиологическое исследование (чреспищеводное с целью диагностики, уточнения механизма тахикардии, возможно и оказания купирующей терапии).
Холтеровский мониторинг желательно проводить в динамике (на 28-30-й неделе, перед родами и через 2 месяца после родов). При выявлении нарушений ритма у здоровых беременных требуется более детальное обследование для исключения, прежде всего, органической патологии сердца. Нарушения ритма сердца чаще всего сопутствуют порокам сердца, кроме того патологии бронхолегочной системы, дисфункции щитовидной железы, электролитным нарушениям и другим патологическим состояниям.
Безусловно, имеет значение анализ течения предшествующих беременностей. Для диагностики нарушений ритма сердца, а также причин, их вызывающих, в первую половину беременности пациентки должны направляться на обследование в кардиологическое отделение терапевтического стационара, а во вторую половину беременности — в отделение патологии беременных родильных домов. Беременные с имеющимися в анамнезе аритмиями, а также пациентки, у которых нарушения ритма выявлялись в предыдущие беременности, должны находиться под диспансерным наблюдением у терапевтов женских консультаций.
НРС обнаруживаются почти у 20% беременных, причем наиболее часто, по данным различных авторов, выявляются наджелудочковые экстрасистолии (НЖЭС) (в 28—67% случаев) и желудочковые экстрасистолии (ЖЭС) (в 16—59% случаев). НРС клинически протекают чаще бессимптомно и определяются только при плановой регистрации ЭКГ или холтер-мониторинге ЭКГ [2]. В подавляющем большинстве случаев экстрасистолическое нарушение ритма сердца не является противопоказанием к естественным родам и не требует медикаментозного лечения.
Назначение антиаритмических препаратов, в первую очередь кардиоселективных β-блокаторов, показано при плохой субъективной переносимости экстрасистолии и у беременных с экстрасистолией высоких градаций, прогностически неблагоприятных.
Реципрокная суправентрикулярная тахикардия — наиболее частый вид тахикардий, встречающийся у женщин детородного возраста. Данный вид нарушений ритма сердца часто встречается у молодых женщин, носит циклический характер и часто связан с предменструальными изменениями в организме. У данных женщин СВТ, вероятно, обусловлена имеющимся периодом низкого содержания эстрогенов в крови.
Относительно заболеваемости СВТ во время беременности данные противоречивы. По данным литературы, риск первичного возникновения СВТ во время беременности возрастает на 34%, а риск развития рецидивов СВТ — на 29%. С другой стороны, у женщин с дополнительными путями проведения эпизоды тахикардии встречаются значительно чаще, по сравнению с АВ-реципрокной тахикардией [3].
Тактика ведения беременных пациенток с пароксизмом АВ-тахикардии такая же, как и у небеременных пациенток. Первоначально должны быть использованы вагусные пробы. При успешном купировании пароксизма с помощью вагусных проб никакой дополнительной антиаримической терапии не требуется. В том случае, если тахикардия продолжается, по рекомендациям Американской ассоциации кардиологов, методом выбора является внутривенное введение АТФ. Ретроспективный анализ показал безопасность и эффективность данного препарата во втором и третьем триместре беременности. Эффективность и безопасность АТФ в первом триместре не изучена.
С целью своевременного выявления брадикардии рекомендуется кардиомониторинг плода. Нецелесообразно введение АТФ беременным с синдромом WPW (возможно развитие фибрилляции предсердий с высокой частотой желудочковых возбуждений). В случае неэффективности АТФ может быть использовано внутривенное введение пропранолола и метопролола. Назначения верапамила следует избегать из-за длительного гипотензивного эффекта.
В том случае, если пароксизм не удается купировать медикаментозно, или у пациентки наблюдается гемодинамическая нестабильность, методом выбора является синхронизирующая электроимпульсная терапия. Для купирования антидромной WPW-тахикардии (с широкими QRS-комплексами) предпочтительнее использовать антиаритмические препараты, способные ухудшать проведение через дополнительные проводящие пути (пропафенон, новокаинамид).
Для лечения эпизодов СВТ во время беременности показано проведение радиочастотной абляции. Радиочастотная абляция также является методом выбора у пациенток с СВТ, устойчивых к медикаментозной терапии. Операцию рекомендуется проводить во втором триместре беременности.
Фибрилляция и трепетание предсердий редко наблюдаются во время беременности при отсутствии органического поражения сердца или каких-либо эндокринных нарушений. Если у женщины развивается фибрилляция или трепетание предсердий во время беременности и у нее не было данных эпизодов в анамнезе, следует исключить у нее возможный врожденный порок сердца, ревматическую болезнь сердца или гипертиреоз.
В настоящее время растет число беременных с врожденными пороками сердца. Следует обратить внимание, что у женщин с врожденными пороками сердца в несколько раз чаще возникают эпизоды ФП. В большинстве случаев пароксизмов ФП в анамнезе у женщин имелись оперативные вмешательства с вовлечением предсердий.
Фибрилляция предсердий часто встречается у пациенток с дефектом межпредсердной перегородки и рубцовыми изменениями предсердий вследствие хирургических вмешательств. Управление эпизодом ФП должно быть направлено на урежение ЧСС β-блокаторами или дигоксином. Во многих случаях восстановление синусового ритма происходит спонтанно. Если спонтанное восстановление ритма не произошло быстро, электрическая кардиоверсия должна быть проведена в течение 48 часов. По истечении данного срока следует решить вопрос о назначении антикоагулянтной терапии.
ЭИТ также показана пациенткам с нестабильной гемодинамикой. Мониторинг плода следует проводить во время и непосредственно после ЭИТ. Антиаритмическая терапия препаратами IА- (дизопирамид), IС- (пропафенон), III- (соталол) классов показана пациенткам с рецидивирующей фибрилляцией и трепетанием предсердий для профилактики рецидивов ФП, а также пациенткам с гемодинамическими нарушениями.
Кроме того, пациенткам с хронической формой ФП с целью профилактики кардиоэмболических осложнений должна назначаться антикоагулянтная терапия. Однако доказан тератогенный эффект варфарина в течение первого триместра беременности. В отличие от варфарина, гепарин не проникает через плаценту и является препаратом выбора у таких пациенток.
При трепетании предсердий медикаментозная терапия менее эффективна, а для восстановления синусового ритма чаще требуется проведение чреспищеводной электрокардиостимуляции (ЧПКЭС) или ЭИТ. При тяжелых, рефрактерных к медикаментозному лечению пароксизмах ФП и ТП возможно применение РЧА, которая наиболее эффективна при типичном трепетании предсердий.
Желудочковая тахикардия (ЖТ) редко встречается при беременности. Наиболее часто — это впервые возникшие пароксизмы.
ЖТ из выносящего тракта правого желудочка встречается у пациентов без структурных поражений сердца и носит доброкачественный характер. Большинство эпизодов тахикардии возникают на фоне воздействия стрессовых факторов и хорошо отвечают на терапию β-блокаторами. Возникновение эпизодов ЖТ или групповых желудочковых экстрасистол не зависит от сроков беременности. Чаще желудочковая тахикардия носит мономорфный характер, и 73% случаев исходят из выносящего тракта.
Число пароксизмов желудочковой тахикардии значительно снижается в послеродовом периоде у большинства женщин. Предполагают, что гемодинамические и нейрогормональные изменения во время беременности играют большую роль в возникновении ЖТ.
Более серьезный прогноз у пациенток, у которых желудочковая тахикардия возникает на фоне органического поражения сердца, синдрома удлиненного QT-интервала, синдрома Бругада.
Купирование гемодинамически нестабильной ЖТ должно включать весь комплекс мероприятий по проведению электрической кардиоверсии. У пациенток с эпизодами ЖТ, не сопровождающейся гемодинамической нестабильностью, можно использовать лидокаин, новокаинамид.
Препаратами выбора для катехоламин чувствительных тахикардий являются β-блокаторы. У пациенток с синдромом удлиненного QT имеется высокий риск возникновения жизнеугрожающего нарушения ритма сердца — пируэт-тахикардии. Как и оговаривалось ранее, таким пациенткам показано назначение β-блокаторов в течение беременности и в послеродовом периоде. В некоторых случаях, особенно в целях профилактики внезапной сердечной смерти, может потребоваться установка кардиовертера-дефибриллятора (ИКВД). ИКВД может быть осуществлена как до беременности, так и на любом сроке беременности с использованием средств максимальной защиты плода [1].
Авторы наблюдали суправентрикулярную тахикардию у беременной женщины на сроке 30 недель.
Пациентка М., 27 лет, доставлена 30.12.11 г. по линии санавиации в кардиологическое отделение РКБ на сроке беременности 30 недель с жалобами на ощущение учащенного сердцебиения. Данная беременность вторая. Первая беременность и роды протекали без осложнений. Ранее на учете у кардиолога не состояла. По данным предыдущих ЭКГ у пациентки наблюдалась синусовая аритмия, нерезко выраженная тахикардия.
Чувство выраженного сердцебиения появилось за два дня до поступления. На приеме в женской консультации зафиксирована наджелудочковая тахикардия. Инъекцией АТФ ритм не восстановлен. Пациентка госпитализирована в кардиологическое отделение БСМП г. Наб Челнов. Проводилась консервативная терапия: верапамил 80 мг 3 раза в день, поляризующая смесь. На фоне проводимой терапии ритм не восстановлен, в связи с чем пациентка переведена в РКБ.
При поступлении у пациентки на ЭКГ наблюдалась суправентрикулярная тахикардия с частотой сердечных сокращений 180 уд. в мин. Гемодинамика была стабильная. После осмотра и обследования выставлен диагноз: «Нарушение ритма сердца: Пароксизмальная форма левопредсердной тахикардии с ортоградной блокадой с коэффициентом проведения 1:1, 3:1». По данным Эхо-КС органической патологии сердца не выявлено.
30.12.11, в связи с неэффективностью медикаментозной терапии, проведена операция радиочастотной абляции. После проведенного оперативного лечения восстановился синусовый ритм.
3.01.12 у пациентки произошел рецидив тахикардии, частота сердечных сокращений в пределах 120—140—180 уд в мин. Далее пациентка находилась под наблюдением в кардиологическом отделении, регулярно осматривалась акушерами-гинекологами. Приступы тахикардии с частотой 180 в минуту сопровождались одышкой, купировались инфузиями калиево-магниевой смеси.
На сроке беременности 37—38 недель пациентка переведена в отделение патологии беременных для родоразрешения путем операции кесарево сечения. На вторые сутки после родоразрешения синусовый ритм восстановился, рецидива пароксизмов тахикардии не наблюдалось.
Нарушения проводимости (замедление или полное прекращение проведения возбуждения из синусового узла по проводящей системе сердца) при беременности обычно не представляют опасности. Даже при полной атриовентрикулярной блокаде, особенно если она обусловлена врожденным или приобретенным в детстве пороком сердца, беременность и роды могут протекать нормально. Противопоказанием к беременности следует считать полную атриовентрикулярную блокаду с частотой сокращений желудочков менее 40 в минуту, а также наличие синдрома Морганьи-Адамса-Стокса.
Особую проблему представляет решение вопроса о возможности беременности и родов у женщин с имплантированным искусственным водителем ритма (ИВР). ИВР с постоянной частотой стимуляции не позволяет сердцу гибко реагировать на меняющиеся во время беременности гемодинамические условия, что в некоторых условиях усложняет положение. Имплантация ИВР с регулируемой частотой стимуляции позволяет сохранить беременность при условии частого контроля за работой ИВР.
1. Оганов Р. Г., Мамедов М. Н Национальные клинические рекомендации по кардиологии. — М., 2009. — 392 с.
2. Аксельрод А. С., Чомахидзе П. Ш., Сыркин А. Л. Холтеровское мониторирование ЭКГ. Возможности, трудности, ошибки / под ред. А. Л. Сыркина. — М.: ООО «Медицинское информационное агентство», 2007. — 192 с.
3. Tak T., Berkseth L., Malzer R. A case of supraventricular tachycardia associated with Wolff-Parkinson-White syndrome and pregnancy. — Wisconsin Medical Journal. — 2012. — V. 111 (5). — P. 228—232.
Неразвивающаяся беременность — причины, симптомы, диагностика, лечение и профилактика

Неразвивающаяся беременность представляет собой патологию, характеризующуюся гибелью плода, аномалиями в инертности миометрия и сбоями во внутреннем балансе организма.
По-другому эта патология называется замершей беременностью. Данное аномальное развитие беременности является вариантом невынашивания. Выделяют два варианта замирания беременности:
- гибель плода или эмбриона (в зависимости от этапа гестации);
- анэмбриония.
Плод сначала развивается нормально в матке, а затем гибнет под воздействием некоторых факторов. Морфологические характеристики плода могут быть нормальными, но жизнедеятельность отсутствует. Выброса эмбриона и продуктов гестации из матки при этом не происходит. Зачастую такая ситуация не характеризуется стандартными признаками угрозы невынашивания.
При анэмбрионии внутри плодного яйца отсутствует эмбрион. Обычно это связывают с тем, что он не развился вообще, или его онтогенез прервался в самом начале. Если при УЗИ в плодном яйце не просматривается эмбрион, то это может быть вызвано анэмбрионией или ранним этапом гестации. Эмбрион может оставаться внутри матки по причине патологических изменений в тканях плодного яйца и аномального функционирования миометрия. Замирание беременности наблюдается примерно в 10% случаях гестации. Неразвивающаяся беременность на ранних сроках гестации встречается наиболее часто.
Причины неразвивающейся беременности
Причины неразвивающейся беременности весьма разнообразны. В основном они совпадают с факторами, ответственными за различные виды выкидышей. К сожалению, порой не представляется возможным прояснить, какой именно фактор вызвал замершую беременность. К механизмам, обуславливающим эту патологию, относят:
- отклонения в геноме эмбриона;
- неадекватную реакцию иммунитета матери на эмбрион;
- патологическую морфологию гениталий;
- аномальное функционирование эндометрия, влекущее сбои при гестации;
- отклонения в свертываемости крови;
- инфекции;
- гормональные нарушения;
- дополнительные факторы.
Следует различать причины неразвивающейся беременности и факторы, приводящие к пребыванию погибшего плода в матке. К последним можно отнести сильное закрепление развивающейся плаценты в результате глубокого проникновения хориона. Отчасти это может быть вызвано аномалиями эндометрия в районе прикрепления плодного яйца. Недостаточные сократительные характеристики миометрия тоже могут вызывать проблемы с выведением эмбриона. К этому могут приводить аномалии белкового обмена веществ и хронические патологические явления в матке.
Патологическая морфология гениталий
Аномалии матки могут быть приобретенными или же врожденными. Врожденные аномалии этого органа обычно приводят к невынашиванию на более поздних стадиях. Патологии в строении матки в ряде случаев сопутствуют аномалиям в мочевыводящей системе. Ненормальное развитие матки зачастую взаимосвязано со сбоями в прикреплении плодного яйца, функциональной патологией эндометрия, гормональными сбоями и другими проблемами при гестации.
Отклонения в геноме эмбриона
Отклонения в геноме эмбриона являются одной из основных причин невынашивания. Неразвивающаяся беременность на ранних этапах гестации обычно вызвана именно ими.
Ввиду этого в случае первой в анамнезе угрозы невынашивания в ранние сроки беременности более предпочтительным является выжидательный подход, а не сохраняющий. Организм зачастую избавляется от сбойного эмбриона посредством невынашивания на ранних стадиях. Наличие существенных генетических аномалий в геноме эмбриона делает нелогичными попытки его сохранения. К сбоям в геноме эмбриона могут приводить нарушения мейоза, отклонения в ходе оплодотворения, ненормальное дробление яйцеклетки и другие факторы.
Аномальное функционирование эндометрия, влекущее сбои при гестации
Аномальное функционирование эндометрия, влекущее сбои при гестации, может быть вызвано разнообразными причинами. К ним относятся отклонения в работе эндокринной и иммунной систем, а также воздействие различных инфекционных факторов. Большое значение в установлении причины невынашивания имеет гистологический анализ плаценты.
Хронический эндометрит является одним из наиболее частых проявлений патологии эндометрия, приводящим к замиранию беременности. Это заболевание вызвано совокупностью патологических явлений, включая нарушение трансформации тканей эндометрия. В ряде случаев наблюдается фиброз стромы и присутствие в ней плазматических клеток.
Отклонение в свертываемости крови
Тромбофилические отклонения вносят существенный вклад в риски невынашивания, включая неразвивающуюся беременность. Природа этой патологии может носить как аутоиммунный, так и аллоиммунный характер. При замершей беременности зачастую наблюдается такое аутоиммунное нарушение, как антифосфолипидный синдром. Он обладает не только аутоиммунными свойствами, но и тромбофилическими. Женщины с замершей беременностью характеризуются повышенным присутствием антифосфолипидных антител в организме. Механизм этого явления до конца не изучен и нуждается в дальнейшем уточнении.
При наличии полиморфизма некоторых генов гемостаза повышаются тромботические риски, которые могут привести к невынашиванию беременности. Полиморфизм этих генов также может приводить к ухудшению метаболизма фолатов в организме женщины. Это ведет к протеканию эмбриогенеза по патологическому сценарию и нарушениям в развитии плаценты. Следствием этого становятся различные проблемы в развитии плода, вплоть до замершей беременности.
Далеко не во всех случаях причины, вызывающие неразвивающуюся беременность, поддаются выявлению. Возможно, что к этиологическим факторам, приводящим к этой патологии, также относятся ненормальная деятельность NK-клеток и присутствие антител аллоиммунного характера.
Факторы риска
Согласно медицинским исследованиям невынашивание на ранних сроках наиболее часто обусловлено возрастом женщины и высоким количеством предшествовавших выкидышей. Репродуктивный потенциал женщин снижается под действием различных заболеваний хронического характера:
- поликистоза яичников;
- сахарного диабеат;
- патологических состояний соединительной ткани;
- заболеваний почек;
- гипотериоза;
- тяжелых форм артериальной гипертонии.
К факторам риска относятся и сбои в репродуктивном здоровье супруга. Не исключено также негативное влияние на протекание гестации различных мутагенов и тератогенных причин, однако степень их воздействия требует уточнения и проведения исследований. К этим факторам мутагенного и тератогенного свойства можно отнести:
- употребление кофеина в большом количестве;
- принятие наркотиков;
- употребление табачной продукции;
- принятие алкоголя.
Диагностика

Неразвивающаяся беременность характеризуется совокупностью специфических признаков. На протяжении начальных 12 недель обычно отмечается прекращение рвоты и тошноты, а также повышенной секреции слюнных желез. В случаях, когда мертвый эмбрион находится внутри матки свыше 1 месяца, у некоторых женщин появляется общий упадок сил, повышение температуры и головокружение. Проводимые одновременно инструментальные виды обследования выявляют отсутствие моторики плода на больших сроках (на раннем сроке движения плода не отмечаются даже в норме). В пределах 1 недели после смерти плода пропадает болезненность молочных желез. Спустя 0,5–1,5 месяца после отмирания эмбриона возникают болевые ощущения и из половых путей вытекают кровянистые выделения.
Мероприятия для постановки диагноза
При смерти эмбриона до 20 недели размеры матки характеризуются уменьшенными параметрами по сравнению с нормой. При этом на ранних этапах гестации это происходит по причине рассасывания плодного яйца, а на более поздних сроках за счет поглощения околоплодных вод и мацерирования эмбриона.
Канал шейки раскрывается на 1–3 см и более в случае задержки мертвого эмбриона на 3–4 месяце вынашивания. Если эмбрион погиб в возрасте старше 14 недель и находится в матке более месяца, то из шейки матки начинает выделяться плотная слизистая жидкость, а внутри плодного пузыря присутствует темная жидкость. Изменение степени плотности маточных стенок не является качественным диагностическим симптомом замершей беременности.
Инструментальная диагностика неразвивающейся беременности
УЗИ является наиболее качественным и точным способом инструментальной диагностики неразвивающейся беременности. Использование этого метода способствует ранней и точной постановке диагноза. Начиная с 7 недели гестации, УЗИ позволяет выявить отсутствие эмбриона в полости плодного яйца, а также диагностировать исчезновение сердцебиения.
Несмотря на точность УЗИ при начальных сроках гестации и долгом присутствии мертвого эмбриона в матке, не всегда представляется возможным его обнаружить. Этот метод инструментального обследования показывает отставание размерных характеристик матки от нормы, а также аномалии морфологических характеристик плодного яйца. Для изографической дифференциации замершей беременности от различных патологий сердца плода (например, преходящей брадикардии) необходимо уделять проведению УЗИ как минимум несколько минут.
Само по себе отсутствие сердцебиения у эмбриона не является императивным признаком замершей беременности, так как оно отсутствует в норме на ранних сроках. УЗИ позволяет визуализировать локализацию плаценты, ее размерные характеристики, наличие отслойки и ряд внешних изменений в структуре.
В целях оперативного обнаружения неразвивающейся беременности на ранних сроках проводится трансвагинальное УЗИ. Такой подход информативен начиная с 2,5 недель гестации. Параллельно обследование позволяет исключить риски внематочной беременности. В ходе проведения УЗИ специалист уделяет внимания ряду признаков, служащих критерием этой патологии. К их числу относятся:
- патологические изменения в контурах и костях черепа;
- избыточный кифоз;
- искажение нормальной формы позвоночника;
- деформация клетки;
- размывание скелетных контуров.
Лабораторная диагностика
Различные виды иммуноферментного анализа позволяют выявить какие-либо отклонения в гормональном статусе женщины. Уровень ряда гормонов имеет важное диагностическое значение для выявления замирания беременности. Например, концентрация β-ХГЧ при этой патологии обычно снижается вплоть до 9 раз. Для белка АФП характерно достижение пиковых уровней спустя примерно 4 дня после смерти эмбриона. Концентрация плацентарного лактогена при замершей беременности может снижаться в 2,7 раза. Несмотря на то что прогестерон при этой патологии может оставаться на значительном уровне, концентрация эстрадиола уменьшается.
Опорожнение матки
Для опорожнения матки в период от зачатия до 6 недель используются медикаментозный метод, а до наступления 12 недели применяется вакуумная аспирация. При медикаментозном лечении неразвивающейся беременности применяется оральный прием лекарств или введение их во влагалище. В ходе такого лечения необходим постоянный мониторинг состояния женщины до выхода плода. При недостаточной эффективности медикаментозного подхода используется хирургический метод.
На данный момент в России основным подходом для устранения последствий замершей беременности является хирургический метод. Это приводит к снижению функциональных характеристик эндометрия в области прикрепления эмбриона. Ряд хирургических подходов к лечению неразвивающейся беременности влечет развитие хронического эндометрита, что нежелательно для репродуктивного здоровья женщины. Из всех методов хирургического устранения последствий замирания беременности вакуумная аспирация характеризуется наименьшими последствиями. Специфика этой процедуры позволяет проводить ее в условиях амбулаторного лечения.
Не ранее чем через две недели после вывода плодного яйца требуется проведение контрольного УЗИ. Альтернативой УЗИ может быть тест на уровень β-ХГЧ. Иногда для минимизации опасности инфекционных проблем, обусловленных наличием в матке некротизирующихся элементов, может быть принято решение об использовании антимикробных препаратов.
Дополнительное обследование после замирания беременности
После нескольких неразвивающихся беременностей и развития привычного невынашивания обычно проводят некоторые виды обследования, перечисленные ниже:
- генетический анализ материалов плодного яйца;
- анализ данных анамнеза;
- инструментальное обследование на предмет патологии анатомии женской репродуктивной системы;
- анализ гормонального фона;
- иммунограмма;
- анализ на инфекции;
- анализы, характеризующие общее состояние здоровья (общий анализ крови и мочи, биохимия крови);
- анализы на свертываемость крови;
- консультация супругов у генетика.
Лечение
Замершая беременность вне зависимости от своего генеза практически во всех случаях сопровождается хроническим эндометритом. По этой причине после выведения соответствующих тканей из матки требуется оперативное применение комплекса лечебных мероприятий:
- функциональное восстановление свойств эндометрия;
- подготовительное лечение для облегчения протекания последующей гестации.
Отмирание эмбриона внутри матки требует оперативного и длительного лечения эндометрита (не позднее трех месяцев после невынашивания). Задержка с применением лечения снижает действенность реабилитационных мер и понижает вероятность благополучного протекания последующей гестации. К сожалению, менее 7 % женщин России используют реабилитационное лечение после очищения матки по завершении неразвивающейся беременности.
Зачастую специалисты предостерегают от прописывания антибиотиков всем женщинам с этой патологией. Необходимость применения противомикробных препаратов желательно основывать на данных бактериологического посева из канала шейки. Употребление антибиотиков в малосимптомных случаях представляется необоснованным. Данные препараты при слабом асептическом процессе способны усугубить сниженный иммунный статус и проблемы в репродуктивной системе женщины.
В случае высокого риска острого эндометрита или усугубления хронической формы этого заболевания допустимо применение бактериальных средств. Гистологическое исследование способно подтвердить нормализацию состояния эндометрия при адекватном лечении. Среди прочего основанием для этого могут быть риски развития острых инфекций, диагностика абсцесса, наличие тошноты, рвоты и высокой температуры.
Восстановление эндометрия
При хронической форме эндометрита у женщин, переживших замершую беременность, требуется применение комплекса восстановительных мер. К ним относятся принятие разнообразных противовоспалительных средств, нормализация иммунных сбоев, улучшение метаболизма, иногда применяется физиотерапия. Главные задачи при восстановлении эндометрия:
- устранение результатов повреждающего воздействия неразвивающейся беременности;
- возвращение в норму функционального состояния тканей эндометрия;
- корректировка сбоев обмена веществ;
- нормализация гемодинамических характеристик.
Гормональное лечение
Гормональные средства комбинированного действия оказывают положительное влияние на состояние эндометрия у женщин, перенесших замершую беременность. К положительным изменениям относятся удлинение шейки матки, уменьшение кровопотерь при менструации и повышенную вязкость цервикальной слизи. Использование оральных контрацептивов комбинированного действия помогает женщинам после замирания беременности тем, что страхует от нежелательного зачатия на протяжении нескольких менструальных циклов и помогает более качественно подготовиться к новой гестации. Для минимизации рисков повторения неразвивающейся беременности специалисты обычно рекомендуют возобновление попытки зачать нового ребенка не ранее, чем через 3–6 месяцев. Этот период необходим для восстановления и оздоровления организма будущей матери.
Подготовка к зачатию
После перенесенной замершей беременности пристальное внимание необходимо уделять вопросу временного предохранения от зачатия. Контрацепция важна для восстановления организма женщины до нужного состояния, в котором она будет готова к новой гестации. Женщины, перенесшие замершую беременность, зачастую нуждаются в помощи квалифицированного психолога, а также психологической поддержке близких родственников.
При подготовке к новому зачатию женщинам, перенесшим замершую беременность, необходимо пройти через комплекс мероприятий для предотвращения повторного невынашивания. Необходимо обеспечение нужного уровня информированности женщины, ее психологической поддержки и мотивации перед выходом на новую гестацию. Многое зависит от врача, который должен правильно информировать и мотивировать будущую мать. Совокупность мер по подготовке к предстоящей гестации включает:
- анализ и оптимизацию состояния микрофлоры влагалища;
- устранение запоров и недостаточной перистальтики;
- развитие правильного пищевого поведения;
- избавление от вредных привычек при их наличии;
- принятие комплекса витаминов, имеющих особое значение для подготовки к гестации (например, фолиевой кислоты и витаминов группы B), а также значимых минералов (например, железа, йода).
Заключение
Предотвращение неразвивающейся беременности основывается на совокупности элементов, ключевым среди которых является адекватное восприятие будущими родителями своей ответственности перед планируемыми детьми. Благодаря психологической помощи со стороны специалистов и родственников, корректировке образа жизни, комплексу восстановительных мер и качественной диагностике женщина даже после перенесенной замершей беременности будет готова к новому зачатию и успешному вынашиванию. Важным элементом успеха при выходе на новую беременность является своевременная и адекватная контрацепция. Важно понимать, что у женщин после замирания беременности возникают неизбежные проблемы с эндометрием, и организму требуется время и лечение, чтобы подготовиться к следующей беременности.
- Базальный ритм (120-160 в мин.) Средняя величина