Методы эндоваскулярной хирургии аневризмы артерий головного мозга
а) Методы эндоваскулярного лечения аневризмы сосуда головного мозга. Попытки окклюзии аневризмы при помощи отделяемого баллона в 1980-х годах сопровождались высокими рисками и не предотвращали повторное кровоизлияние. Введение Guglielmi отделяемых спиралей (GDC) в 1990 г. оказалось намного более безопасной и более эффективной альтернативой. Платиновые спирали вводятся через катетер в дно аневризмы и отделяются электролитически. «Плотная упаковка» аневризмы несколькими спиралями занимает менее одной трети фактического объема, но этого достаточно, чтобы предотвратить повторное кровотечение у большинства пациентов.
Примерно в одной трети случаев радиологи специально оставляют заполнение шейки аневризмы в связи с риском окклюзии спиралью проксимального сосуда, в этом случае риск повторного кровоизлияния выше.
Приблизительно в 5% случаев эмболизация аневризмы не удается. Аневризмы подходят для эмболизации если соотношение дно/ширина шейки больше чем 2:1. Радиологи могут выбирать спирали разного диаметра и ЗЭ-формы. Как правило, требуется от четырех до пяти спиралей, но возможное количество варьируется от одной спирали для 3 мм аневризмы до 20 спиралей для гигантских аневризм.
1. Коррекция с помощью баллона. Этот метод, разработанный Moret, позволяет эмболизировать аневризмы с широкой шейкой. Периодическое раздувание баллона на отдельном катетере в несущем сосуде предотвратцает выпадение спиралей в просвет сосуда. По окончании процедуры спирали сохраняют форму, приданную им баллоном. Некоторые центры используют эту технику в 30-40% случаев эндоваскулярной хирургии.
2. Биоабсорбирующие полимеры. Новые разработки включают в себя использование биоабсорбирующего полимерного покрытия вокруг спирали (Matrix) или в спирали (Cerecyte). Экспериментальные работы на животных показали, что эти полимеры стимулируют регенерацию клеток, способствуют организации тромба в аневризме и стимулируют образование новой интимы. Будут ли эти спирали улучшать общие результаты, остается неопределенным, эта информация будет получена в ходе исследований.
3. Гидрогелевые и волокнистые спирали. Гидрогелевые спирали покрыты гидрофильным полимером, расширяющимся при контакте с кровью, что помогает заполнить просвет аневризмы. Кроме того, спирали с волокнами дакрона или нейлона вызывают более тромбогенную реакцию, чем платина, однако все эти новые технологии ждут дальнейших исследований.
4. Интракраниальные стенты. Введение в практику стентов подходящего размера и достаточной гибкости для прохождения через внутричерепные сосуды предоставило другую альтернативу для аневризм, имеющих широкую шейку, гигантских или веретенообразных аневризм, особенно развивающихся из внутренней сонной артерии или развилки основной артерии. После установки стента микрокатетером можно пройти через стент в полость аневризмы, чтобы разместить в ней спираль без риска окклюзии просвета сосуда. Для предотвращения тромбоза стента назначается пожизненная антитромбоцитарная терапия.
5. Оникс. Оникс — жидкий полимер, который затвердевает при контакте с кровью, может быть введен в аневризму, если ее шейка защищена баллоном или стентом. Теоретически метод весьма привлекателен, но первые исследования показали высокий уровень сложности выполнения, что ограничивает его более широкое применение.
6. Отдаленные результаты эндоваскулярной хирургии. При любых вмешательствах необходимо проведение контрольной ангиографии, как правило, через шесть месяцев после лечения. Реканализация аневризмы за счет уплотнения или миграции спиралей требует повторного вмешательства примерно у 10% пациентов.
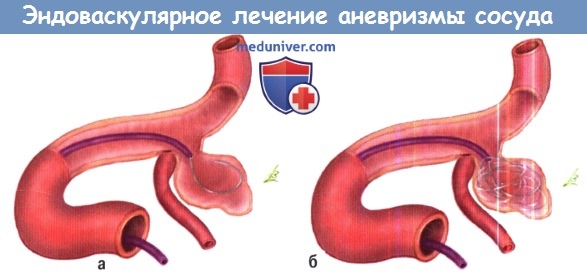 А. Эмболизация спиралями — введение первой спирали через катетер.
А. Эмболизация спиралями — введение первой спирали через катетер.
Б. Введение последующих спиралей.
б) Выбор эндоваскулярного метода лечения аневризмы сосуда головного мозга. Изначально, в 1990-х годах эндоваскулярное лечение предназначалось для неоперабельных аневризм. Данная методика лечения чаще используется для тех аневризм, которые трудно лечить открытым путем, в частности, аневризм заднего обращения, несмотря на все убедительные доказательства большей радикальности. Международное исследование аневризматического САК (ISAT)—клипирование против койлинга, началось в 1994 г. Комитет по мониторингу данных остановил сбор информации в 2001 г. после того, как центры изучили данные 2143 пациентов.
Исследование показало, что через один год после эндоваскулярной эмболизации абсолютный риск смерти снизился на 7% (относительный риск снижался на 23%) по сравнению с пациентами, перенесшими клипирование. Значительно больше повторных кровоизлияний и более высокая смертность от повторного кровоизлияния имели место в течение первого года в группе койлинга, однако исследователи по-прежнему выступают за данную методику. Несмотря на отсутствие долгосрочных результатов и то, что пациенты выбранной группы почти всегда имели хороший соматический и неврологический статус, а также небольшую аневризму переднего отдела вилизиева круга, в Великобритании резко сменилась тактика лечения в пользу эмболизации; доля операций внутрисосудистым методом увеличилась с 37 до 54%. Во многих центрах этот показатель в настоящее время превышает 80%.
Последующее семимилетнее наблюдение за пациентами ISAT показало, что выживаемость за это время выше, несмотря на повышенный риск позднего повторного кровоизлияния в эндоваскулярной группе.
Лечение аневризм проводится бригадой специалистов, состоящей из интервенционных радиологов и нейрохирургов. Даже если бы не было разницы в результатах между этими двумя методами лечения, большинство пациентов выбрали бы наименее инвазивный подход. Результаты ISAT подтверждают использование эмболизации в качестве метода первой линии. Тем не менее, не все аневризмы подходят для эндоваскулярного лечения. Следующие факторы делают эмболизацию более трудной или невозможной:
– Аневризма средней мозговой артерии
– Аневризмы с широкой шейкой и соотношением тело/ширина шейки менее чем 2:1
– Аневризмы 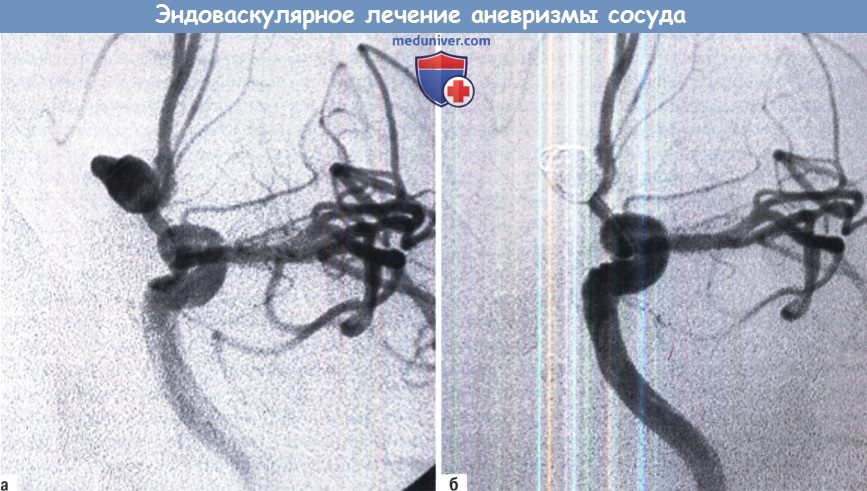 А. Цифровая ангиограмма, показывающая аневризму передней соединительной артерии.
А. Цифровая ангиограмма, показывающая аневризму передней соединительной артерии.
Б. Завершающая стадия эмболизации спиралями, показывающая дно, заполненное спиралями.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Эмболизация аневризмы
 Эмболизация аневризм – современный метод высокотехнологичного лечения патологического выпячивания сосудов. Аневризмы – это мешковидное или веретенообразное расширение сосуда с истончением его стенки. Тонкая сосудистая стенка может разорваться и вызвать большое кровотечение, которое без помощи хирургов, вероятно убьёт пациента. Аневризму можно вырезать, отключить или закрыть. Преднамеренная окклюзия (закрытие) просвета кровеносного сосуда с помощью специально введённого в лечебных целях вещества (эмбола) , называется эмболизацией.
Эмболизация аневризм – современный метод высокотехнологичного лечения патологического выпячивания сосудов. Аневризмы – это мешковидное или веретенообразное расширение сосуда с истончением его стенки. Тонкая сосудистая стенка может разорваться и вызвать большое кровотечение, которое без помощи хирургов, вероятно убьёт пациента. Аневризму можно вырезать, отключить или закрыть. Преднамеренная окклюзия (закрытие) просвета кровеносного сосуда с помощью специально введённого в лечебных целях вещества (эмбола) , называется эмболизацией.
Эмболизация — это малоинвазивная процедура, являющаяся альтернативой хирургии. Она показана в случаях, когда выполнение открытого оперативного вмешательства очень травматично или чревато осложнениями. В нейрохирургии эндоваскулярная эмболизация аневризмы головного мозга всё больше вытесняет операции с трепанацией черепа.
Цель эмболизации аневризмы заключается в предотвращении кровотока в аневризматическом мешке путём заполнения его полости специальными спиралями. Это должно предотвратить разрыв и кровотечение. Эндоваскулярная эмболизация аневризмы головного мозга не восстанавливает области уже повреждённого мозга.
Материалами для окклюзии служат спирали, специальные губки или гистоакрил. Для лечения аневризмы обычно используются спирали, либо эмболизирующее вещество.
Спирали бывают разной конфигурации, длины и диаметра. Структурные спирали изготавливают из платины, которая при введении в сосуд сворачивается в трёхмерную фигуру для заполнения полости аневризмы.
Могут потребоваться дополнительные устройства, такие как стент, чтобы помочь удержать спирали внутри аневризмы. Вмешательство с помощью стента подразумевает постоянное размещение его в сосуде, прилегающем к аневризме, для обеспечения поддержки, которая удерживает спирали внутри мешка. Самыми сложными технологиями пользуются для эмболизации аневризм сосудов головного мозга, потому что риски заболевания очень высоки, а доступ к ним, открытым методом очень затруднён.
Подготовка к лечению
- Не ешьте твёрдой пищи после полуночи в день операции. Питьё воды допускается утром в день процедуры, если не указано иное.
- Вы должны прекратить приём антикоагулянтов за 5 дней до процедуры. Эти препараты включают аспирин, плавикс и Варфарин.
- Если вы находитесь на инсулине, спросите своего врача о любых корректировках, которые могут потребоваться.
 Как проходит лечение
Как проходит лечение
После местной анестезии врач вставляет полую пластиковую трубку (катетер) в в бедренную артерию и продвигает его, используя ангиографию, до места аневризмы.
Используя направляющий катетер,спирали платиновой проволоки или маленькие латексные шарики проводят через катетер и вводят их в аневризму. Они заполняют аневризматический мешок, выключая его из кровообращения, вызывая образование сгустка крови (тромба), который полностью пломбирует полость аневризмы. Мягкость платины позволяет спирали соответствовать причудливой форме мешка. Для полного его заполнения требуется в среднем 5-6 спиралей.
Средняя продолжительность процедуры составляет 1-2 часа.
Когда шейка аневризмы слишком широка иногда требуется установить стент в основной сосуд, чтобы удерживать спирали внутри мешка. Поскольку стент действует как барьер между аневризмой и материнским сосудом, очень маловероятно, что из неё будут выступать катушки.
Возможные осложнения
Эмболизация как метод лечения имеет небольшой риск. Возможные осложнения включают в себя такие симптомы, как слабость в одной руке или ноге, онемение, покалывание, нарушения речи и проблемы со зрением. При эмболизации аневризм церебральных артерий может быть непродолжительная головная боль.
Серьёзные осложнения, такие как инсульт или смерть, встречаются редко. Курение, ожирение и высокое артериальное давление увеличивают шанс получения осложнений после процедуры.
Прогноз
Эффективны как открытая хирургия, так и эндоваскулярные методы. Выбор лечения зависит от ряда факторов: есть ли риск разрыва аневризмы, её размер, форма и местоположение. Как и все медицинские решения, наилучший вариант лечения следует обсудить с вашим врачом.
Процедуру иногда требуется выполнить несколько раз в течение жизни пациента.
АНЕВРИЗМЫ СОСУДОВ ГОЛОВНОГО МОЗГА
 Частая причина геморрагического инсульта. Аневризмы представляют собой выпячивания сосудистой стенки и располагаются обычно в местах деления сосудов. Под действием различных факторов (гипертоническая болезнь, курение, наследственная предрасположенность) происходит рост аневризмы и истончение ее стенки. Указанные процессы в итоге приводят к разрыву аневризмы и кровоизлиянию в мозг и окружающие его пространства. Более половины больных не переносят кровоизлияние и погибают не смотря на интенсивную терапию даже в самых лучших клиниках. Именно поэтому практически во всех случаях рекомендуется профилактическая операция, имеющая целью выключение аневризмы из кровотока.
Частая причина геморрагического инсульта. Аневризмы представляют собой выпячивания сосудистой стенки и располагаются обычно в местах деления сосудов. Под действием различных факторов (гипертоническая болезнь, курение, наследственная предрасположенность) происходит рост аневризмы и истончение ее стенки. Указанные процессы в итоге приводят к разрыву аневризмы и кровоизлиянию в мозг и окружающие его пространства. Более половины больных не переносят кровоизлияние и погибают не смотря на интенсивную терапию даже в самых лучших клиниках. Именно поэтому практически во всех случаях рекомендуется профилактическая операция, имеющая целью выключение аневризмы из кровотока.
Общая информация. Диагностика
Хирургическое лечение артериальных аневризм церебральных сосудов на протяжении нескольких десятилетий является одним из основных и наиболее важных направлений работы сосудистого отделения института. Это связано с тем, что методов консервативного лечения данной патологии не существует, а оперативные вмешательства на аневризмах остаются в ряду наиболее сложных нейрохирургических операций. Несмотря на многочисленные исследования, направленные на разработку методов профилактики разрыва аневризм и лечение осложнений аневризматических кровоизлияний, артериальные аневризмы церебральных сосудов по-прежнему являются заболеванием с высокой вероятностью летального исхода или стойкой инвалидизации: при отсутствии хирургической помощи до 70% больных погибают в первый год от начала болезни, 25% выживших остаются инвалидами. Распространенность артериальных аневризм в популяции довольно высока — не менее 0,6% (около 600 человек на 100 000 населения). Частота САК вследствие разрыва аневризм составляет 10–15 случаев на 100 000 населения в год. Таким образом, в России ежегодно в госпитализации нуждается около 18 000 больных с аневризматическим САК. Появление новых диагностических возможностей привело к учащению выявления бессимптомных аневризм, что еще более увеличило количество больных, обращающихся за медицинской помощью.
КТ в режиме ангиографии
За более чем 40-летний период в институте выполнено около 5000 прямых хирургических вмешательств и более 700 эндоваскулярных операций по поводу артериальных аневризм. Число больных, ежегодно поступающих для оперативного вмешательства, возросло со 100 больных в 70-е–80-е годы до 300 и более к настоящему времени. Постоянный анализ этого клинического материала в диссертационных работах, детализация принципов лечения в зависимости от сроков после кровоизлияния, размеров, расположения, анатомических особенностей аневризм, их количества у одного человека, возраста больных, привели к созданию отдельных направлений в хирургии церебральных аневризм. Важнейшую роль в хирургическом лечении аневризм играют методы диагностики заболевания. В настоящее время диагностика аневризм может быть выполнена методами прямой ангиографии, МРТ- и СКТ-ангиографии. Результаты этих трех методов могут быть представлены в объемном изображении (3D-реконструкция). СКТ-АГ в настоящее время может считаться методом выбора в выявлении причины САК.
Особую роль в обследовании больного в остром периоде САК играют методы диагностики ангиоспазма. Транскраниальная ультразвуковая допплерография (ТК УЗДГ), уступая нейровизуализационным методам в чувствительности и специфичности, позволяет оценить динамику ангиоспазма, так как неинвазивность метода дает возможность проводить многократные исследования. КТ и МРТ в различных режимах у больных с аневризмами незаменимы в диагностике и динамическом контроле таких осложнений САК и операции, как внутримозговые гематомы, внутрижелудочковые кровоизлияния, отек и ишемия головного мозга, острая и отсроченная гидроцефалия.
Оставаясь неизменной в основополагающих принципах, хирургия церебральных аневризм постоянно совершенствуется. Современный этап лечения артериальных аневризм в институте можно характеризовать как этап строго дифференцированного и индивидуализированного лечения, выполняемого с учетом всех особенностей течения болезни, морфо-функциональной характеристики аневризм, состояния больного и других факторов. Основой идеологии хирургии аневризм является интеграция и взаимодополнение микрохирургических и эндоваскулярных методов. При микрохирургическом лечении аневризм основной операцией является клипирование шейки аневризмы самозажимающимся клипсом. В зависимости от анатомо-топографических особенностей аневризмы, используются клипсы различного размера и конфигурации. За последние годы в институте разработан и внедрен ряд хирургических и диагностических методов, позволивших улучшить качество выключения более сложных аневризм: внутрисосудистая аспирация крови, интраоперационная ультразвуковая допплерография, флоуметрия, флюоресцентная ангиография.
Основными преимуществами эндоваскулярного метода лечения аневризм являются возможность полного выключения аневризмы из кровотока при отсутствии хирургической травмы мозга и возможность выключения аневризм, труднодоступных или недоступных для прямого хирургического вмешательства. Эти преимущества в первую очередь важны у больных в остром периоде кровоизлияния, при аневризмах параклиноидного отдела ВСА и вертебро-базилярного бассейна. Предпочтительным методом эндоваскулярного выключения аневризм следует считать реконструктивные операции — окклюзию полости аневризмы с сохранением просвета несущего сосуда. Для выключения аневризм в настоящее время используется методика окклюзии аневризмы отделяемыми микроспиралями.
Выбор метода выключения аневризмы
Окклюзия аневризмы
со стент-ассистенцией
Преимущества эндовазального лечения в первую очередь важны у больных в остром периоде кровоизлияния, при аневризмах параклиноидного отдела ВСА и вертебро-базилярного бассейна. Основным фактором, определяющим возможность окклюзии аневризмы эндоваскулярным методом до недавнего времени считалось соотношение размера тела аневризмы и ее шейки. Установлено, что чем больше размер аневризмы и шире ее шейка, тем больше вероятность отдаленной реканализации после первоначально тотально выполненной окклюзии. Для решения этой проблемы разработаны стент-ассистирующие методики. Суть стент-ассистирующей методики при лечении аневризм заключается в предотвращении смещения витков спиралей в просвет несущего сосуда. Это достигается следующим образом: первым этапом сосуд на уровне шейки аневризмы устанавливается стент, а затем через ячейку стента проводится микрокатетер, через который доставляются микроспирали. В последние годы появилась новая категория внутричерепных стентов, так называемые потоконаправляющие стенты (flow divert), которые позволяют уменьшать кровоток в аневризме, направляя основной поток крови по несущему сосуду. Тромбирование аневризмы после установки такого стента в среднем наступает в период от 4 до 6 месяцев после операции. Эта методика наиболее эффективна для лечения аневризм крупных и гигантских размеров. В настоящее время в НИИ нейрохирургии ежегодно выполняется около 250 микро-хирургических и 150 эндоваскулярных операций на аневризмах в «холодном» периоде после САК (21 день и более). Выбор метода операции зависит, прежде всего, от анатомических особенностей аневризмы. Эндоваскулярный метод предпочтителен при аневризмах ВСА параклиноидного и инфраклиноидного расположения. При аневризмах развилки СМА и аневризмах ПМА-ПСА чаще проводятся прямые вмешательства, так как особенности строения этих аневризм (преимущественно широкая шейка, близость устьев артерий второго порядка, варианты строения ПСА и др.) и невозможность применения стентов ограничивают использование эндоваскулярного метода. На решение вопроса о методе операции влияет возраст больного — у молодых больных предпочтительны прямые операции, имеющие более высокую радикальность. Ограничением для эндоваскулярного метода являются патологические изгибы и выраженный атеросклероз брахиоцефальных артерий. При необходимости операции со стент-ассистенцией следует учитывать наличие кровотечений различной этиологии в анамнезе, так как установка стента требует в длительного приема антикоагулянтов в послеоперационном периоде. В некоторых случаях микрохирургические операции выполняют вторым этапом в случаях, когда в ходе эндоваскулярного вмешательства достигнута лишь частичная окклюзия аневризмы. Возможны и обратные ситуации — эндоваскулярное вмешательство после паллиативной прямой операции (укрепление аневризмы марлей, неполное клипирование). Результаты микрохирургического лечения аневризм в холодном периоде после САК на протяжении многих лет остаются достаточно хорошими. Риск возникновения нового неврологического дефицита несколько выше при микрохирургическом выключении аневризмы, риск летального исхода выше при эндовазальном лечении.
Лечение больных в остром периоде заболевания
Сравнение внешнего вида мозга
в остром и холодном периоде после САК
Лечение больных в остром периоде после САК – сложная задача, требующая привлечения различных специалистов. Обоснованием операций в остром периоде является, прежде всего, возможность повторных кровоизлияний, которые сопровождаются крайне высокой летальностью. После выключения аневризмы также возможно начало проведения интенсивной сосудистой терапии, направленной на устранение последствий кровоизлияния. На основании анализа результатов хирургического лечения более чем 600 больных в остром периоде САК в институте было показано, что прогностически значимыми критериями оценки исхода операции являются массивность кровоизлияния, состояние больного по шкале Нunt-Нess или WFNS, срок операции после САК. C учетом этих факторов разработаны основные принципы лечения больных. Показания к операции в острой стадии САК должны быть строго индивидуализированы. Для решения вопроса о тактике ведения больного необходимым минимумом является оценка состояния больного по шкале Нunt-Нess или WFNS, КТ, ангиография, ТК УЗДГ с определением выраженности ангиоспазма. Особое внимание следует обращать на срок после кровоизлияния. Операция показана больным в I–II стадии по Нunt–Нess, независимо от срока после САК; в III–IV стадии по Нunt–Нess в сроки от 14 суток после САК. У больных III–IV стадии при операции на 0–3 сутки после САК необходима установка датчиков для послеоперационного контроля ВЧД, так как для этих больных характерно развитие ангиоспазма и отека мозга в раннем послеоперационном периоде . У больных III–IV стадии на 4–7 сутки после САК при наличии умеренного или выраженного ангиоспазма от операции следует воздержаться. Длительность отсрочки операции при ангиоспазме зависит от показателей ТК УЗДГ: операция может быть выполнена при снижении скорости кровотока до соответствующей легкому спазму, либо при стабилизации на уровне умеренного спазма в течение нескольких дней, но не ранее 7-х суток после САК. В V стадии операция показана только при наличии больших внутримозговых гематом. В этих случаях операция наиболее эффективна при максимально ранних вмешательствах. В остром периоде САК методом выбора, особенно у тяжелых больных, следует считать эндоваскулярное выключение аневризмы. В ряде случаев при невозможности полной окклюзии аневризмы можно ограничиться частичным выключением, с последующей повторной операцией после улучшения состояния. Помимо анатомических особенностей, ограничением для проведения эндоваскулярной операции в остром периоде служит выраженный ангиоспазм, препятствующий проведению катетера. При выполнении прямого вмешательства необходимо учитывать, что мозг больного в остром периоде САК значительно более чувствителен к хирургической травме, в связи с этим необходимо использовать максимально щадящие способы доступа к аневризме с ограничением тракции мозга, использованием методов релаксации (осмодиурез, выведение ликвора) и защиты мозга от ишемии.
На протяжении всего периода лечения больных в острой стадии САК ведущей задачей является предотвращение и лечение типичных для кровоизлияния из аневризмы осложнений, в первую очередь, ангиоспазма, отека мозга и острой или отсроченной гидроцефалии. В настоящее время для борьбы с этими осложнениями используется методика внутрисосудистого введения спазмолитиков под контролем ТК УЗДГ, 3Н-терапия в условиях мультимодального мониторинга, декомпрессивная трепанация черепа. За последние 10 лет послеоперационная летальность при прямых операциях в остром периоде составила в среднем 7,3%, а общая смертность — 12,4%. Среди выживших больных 80% полностью независимы в повседневной жизни, около 40% вернулись к работе и учебе. Полученные данные использованы при создании рекомендательного протокола по ведению больных в остром периоде САК совместно с ведущими нейрохирургами России. Опыт института позволил принять участие в нескольких в международных исследованиях, посвященных лечению больных в острой стадии САК.
Лечение крупных и гигантских аневризм
Выключение гигантской аневризмы ВСА
с использованием методики ВАК
Хирургическое лечение крупных и гигантских аневризм — один из самых сложных вопросов сосудистой нейрохирургии. В 70-е годы оперативное пособие у таких больных ограничивалось перевязкой внутренней сонной артерии на шее, при этом послеоперационная летальность составляла 15,2%. С появлением эндовазальной техники стало возможным проведение баллон-окклюзионного теста под контролем ЭЭГ с последующей стационарной окклюзией ВСА. В отдельных случаях данный способ лечения комбинировали с наложением ЭИКМА, однако, послеоперационная летальность в группе гигантских аневризм оставалась высокой. С 1995 года в институте разработана и используется методика внутрисосудистой аспирации крови из аневризмы. Методика ВАК показала себя весьма эффективной в хирургии крупных и гигантских аневризм ВСА, позволила в 4 раза уменьшить послеоперационную летальность и значительно сократить группу больных, которым отказано в хирургическом лечении. В настоящее время отделение располагает самым большим опытом в мире по применению методики ВАК.
Выключение крупной аневризмы с помощью
установки потоко-направляющего стента
Наряду с прямыми вмешательствами, на протяжении многих лет для лечения крупных и гигантских аневризм в институте использовались и эндоваскулярные методы. До появления стент-ассистенции и потоконаправляющих стентов, добиться полного выключения таких аневризм спиралями удавалось редко. Появление стентов существенно изменило возможности эндоваскулярного лечения крупных и гигантских аневризм. С момента использования потоконаправляющих стентов произошло существенное снижение доли деконструктивных операций. Несомненно, что эта технология имеет большие перспективы и в ближайшем будущем существенно изменит структуру эндоваскулярных вмешательств при лечении аневризм в целом.
Микрохирургическое лечение бессимптомных аневризм
До недавнего времени бессимптомные аневризмы выявляли крайне редко. В последние годы широкое распространение и доступность неинвазивных методов нейровизуализации привели к значительному увеличению числа пациентов со случайно выявленными аневризмами. За последние 10 лет в институте оперировано около 400 пациентов с бессимптомными аневризмами. Результаты хирургического лечения в этой категории больных следует признать удовлетворительными. С учетом этих данных, а также крайне высокой вероятностью неблагоприятного исхода при разрыве аневризмы, можно утверждать, что неразорвавшиеся бессимптомные аневризмы в большинстве случаев необходимо оперировать. Следует отметить, что больной должен быть полностью информирован о характере болезни, предстоящей операции и возможных осложнениях.
Множественные аневризмы
К настоящему времени доля больных с множественными аневризмами составляет 20–25% от всех оперируемых в институте больных с аневризмами. В подавляющем большинстве случаев у больного с множественными аневризмами обнаруживают не более двух аневризм, однако встречаются больные с тремя и более аневризмами. Сочетания аневризм по локализации, размерам, количеству, клиническим проявлениям достаточно разнообразны. Первоочередной задачей на этапе диагностики является определение аневризмы, послужившей источником кровоизлияния. Основным принципом лечения МА является первоначальное выключение из кровотока разорвавшейся аневризмы с применением микрохирургической или эндоваскулярной техники в зависимости от анатомических особенностей аневризмы. Операции могут быть выполнены в один и несколько этапов. При лечении множественных аневризм различных сосудистых бассейнов, особенно в остром периоде САК, а также при сложных аневризмах, предпочтительны двухэтапные или многоэтапные вмешательства.
Лечение аневризм у больных детского возраста
Аневризмы головного мозга у детей встречаются редко и могут сочетаться с различной патологией соединительной ткани (с-м Марфана, с-м Элерса-Данлоса) и различными аномалиями развития вилизиева круга. У детей в три раза чаще, чем у взрослых, выявляются аневризмы со сложными анатомическими характеристиками. Псевдотуморозный и ишемический типы течения при «детских» аневризмах встречаются в несколько раз чаще, чем у взрослых. Случайно обнаруженные аневризмы у детей редки. Принципы хирургического лечения аневризм у детей в целом те же, что и у взрослых. Следует отметить, что компенсаторные возможности ребенка при развитии каких-либо осложнений больше, чем у взрослых, поэтому дети легче переносят выключение несущих аневризму артерий. В этой связи деконструктивные операции можно рассматривать как метод выбора в случаях сложных аневризм при невозможности выключения аневризмы с сохранением проходимости артерии.
Методы эндоваскулярной хирургии аневризмы артерий головного мозга
Чудновец Л.Г., Селезнев Е.В., Сайфуллина Э.И., Мустафин М.С.,
Камалов А.Р., Мустафакулов У.С., Халимов Э.Р.
Региональный сосудистый центр, Республика Башкортостан, г. Уфа,
Актуальность. Нетравматическое субарахноидальное кровоизлияние (САК) является одним из наиболее частых и тяжелых форм нарушения мозгового кровообращения, частота заболевания составляет 6-16 на 100 тыс. в год. Причинами САК в 70-85% случаев является разрыв артериальных аневризм сосудов головного мозга. Летальность до оказания медицинской помощи составляет 12%, в первые 30 дней после заболевания – более 40%. Хирургический метод лечения САК в случае разрыва интракраниальных аневризм является основным. Причинами летальности и инвалидизации при нетравматических САК является повторный разрыв аневризмы и развитие некупируемого вазоспазма.
Материалы и методы. За период с июня 2009 года по июнь 2011 года в нашем центре эндоваскулярные оперативные вмешательства проведены 65 пациентам, средний возраст которых составил 48,43±13,34 лет (женщины – 36 (55,4%), мужчины – 29 (44,6%). Большинство пациентов поступило с подозрением на геморрагический инсульт. Каждый пациент был обследован в соответствии с приказом Минздравсоцразвития России №389н от 06.07.2009 “Об утверждении порядка оказания медицинской помощи больным с острыми нарушениями мозгового кровообращения”
Тактика лечения определялась совместно с нейрохирургами после проведения селективной церебральной ангиографии. Учитывались локализация, анатомические особенности аневризмы, возможность эндоваскулярного доступа, характер внутримозгового кровоизлияния, возраст, тяжесть состояния пациента.
Эмболизация артериальной аневризмы проведена 64 пациентам. Тотальная эмболизация (тип А) достигнута у 19 пациентов (29,2%), парциальная (тип В) – у 41 пациентов (63,1%), (тип С) – у 5 (7,7%) пациентов. Эмболизация с использованием баллон-ассистенции проведена у 5 пациентов (7,7%), стент-ассистенции (в “холодном периоде”) – у 3 пациентов (4,6%). 1 пациентке с гигантской аневризмой ВСА установлен “отводящий поток” стент.
Характер распределения пациентов по локализации аневризмы был следующим: ВСА – 31 (47,7%), ПСоА – 13 (20%), ПМА – 2 (3,1%), СМА – 15 (23,1%), артерий ВББ – 4 (6,2%). Множественные аневризмы выявлены у 22 пациентов (33,8%).
Распределение оперированных пациентов с САК по тяжести состояния при поступлении по шкале Hunt-Hess: I степени – 19 пациентов (29,2%), II степени – 21 (32,3%), III и IV степени – 25 (38,5%). Степень субарахноидального кровоизлияния оценивалась по КТ-шкале C.M. Fischer: 1 балл – 5 пациентов (10,4%), 2 балла – 16 пациентов (33,3%), 3 балла – 2 пациента (4,2%), 4 балла – 25 пациента (52,1%). Интравентрикулярное кровоизлияние наблюдалось у 22 пациентов (33,8%).
В острейшем периоде кровоизлияния (1-3 сутки) оперировано 20 пациентов (30,8%), остром (4-30 сутки) – 29 (44,6%). Плановые оперативные вмешательства (в “холодном” периоде (свыше 30 суток) кровоизлияния и асимптомные аневризмы) проведены у 16 пациентов (24,6%). У 17 пациентов (26,2%) эмболизация аневризм проводилась как первый этап комбинированного оперативного вмешательства перед трепанацией черепа с удалением внутримозговой гематомы или наружным дренированием желудочковой системы.
При проведении эндоваскулярной эмболизации мы столкнулись со следующими осложнениями. Интраоперационный разрыв аневризмы произошел у 2 пациентов (3,1%), проводилась дальнейшая имплантация спиралей до прекращения кровотечения и прикрытие шейки аневризмы комплайнсным баллонным катетером (в одном случае потребовалось открытое оперативное вмешательство с удалением гематомы). Острый тромбоз артерии развился у 2 пациентов (3,1%), проводился селективный церебральный тромболизис и пластика области шейки аневризмы баллонным катетером. Самопроизвольное отделение спирали наблюдалось в 1 случае (1,5%) – был произведен захват и перерастяжение свободного конца спирали с низведением ее в нисходящий отдел аорты. Летальных исходов в результате интраоперационных осложнений не наблюдалось.
Результаты лечения. Благоприятный исход (полное восстановление без неврологического дефицита) достигнут у 44 пациентов (67,7%), удовлетворительный (умеренный и выраженный неврологический дефицит) – у 13 пациентов (20%).
Летальность составила 12,3% (8 случаев). В 1 случае причиной летальности был повторный разрыв аневризмы после проведенной частичной эмболизации аневризмы.
Была оценена эффективность эндоваскулярного лечения аневризм в зависимости от локализации, тяжести состояния пациентов, сроков операции с момента САК, эпизодов повторного САК за период госпитализации.
Выявлено, что результаты лечения зависели от тяжести состояния пациента по шкале Hunt-Hess на момент операции: в группе пациентов с II степенью тяжести летальный исход наблюдался у 1 пациента (4,8%) – связан с дальнейшим развитием некупируемого декомпенсированного вазоспазма, III степенью – у 15%, IV степенью – у 80% (p Информация о материале Просмотров: 6169
Лечение и операция по удалению аневризмы сосудов головного мозга: риски и последствия
Аневризмой называют патологическое образование в виде местного расширения кровеносной артерии головного мозга из-за слабой, неэластичной, истонченной сосудистой стенки. Заболевание серьезное, способное привести к смертельному исходу. Оно опасно разрывом сосуда в месте расширения, после чего происходит субарахноидальная или внутримозговая геморрагия.
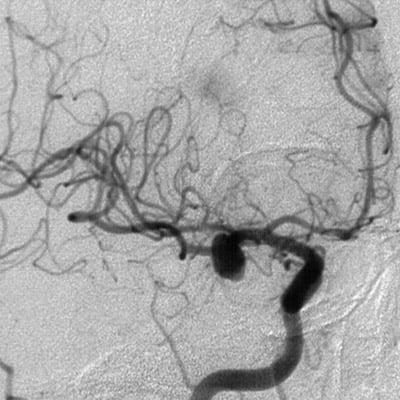
Аневризма на результатах ангиографии.
До момента криза болезнь может развиваться бессимптомно, иногда давать несильную неврологическую симптоматику, которую легко спутать с другими неопасными болезнями. Зачастую человек не предполагает, что у него в голове «бомба», которая «прячется» годами, но может разорваться в любой момент. После того как сосуд лопается и из него изливается кровь, заполняющая структуры головного мозга, аневризма уже проявляется в полную мощь. Основополагающими признаками произошедшего кровоизлияния являются внезапная жуткая головная боль и потеря сознания. К сожалению, позднее оказание медицинской помощи, как правило, оканчивается трагедией.
Заболевание может возникнуть в любом возрасте, однако чаще встречается у молодых людей (20-45 лет) и лиц среднего возраста (45-60 лет). Общий процент заболеваемости у взрослого населения составляет от 0,3% до 5%, у детей аневризмы – явление очень редкое. По статистике, из-за внезапного кровоизлияния в мозг вследствие аневризм 30%-50% людей погибает, 15%-30% становится инвалидами и только примерно к 20% возвращается относительно нормальная трудоспособность. Да, цифры неутешительные, но при ранней диагностике и своевременном лечении даже такой грозный очаг в головном мозге может быть успешно обезврежен.
Что может повлиять на образование сосудистой аневризмы, каких видов она бывает, как предотвратить трагедию, об этом важно знать абсолютно каждому. Итак, подробно переходим к главному.
Причины развития аневризм
Неблагополучными факторами, увеличивающими риски к тяжелой болезни, являются последствия некоторых патологий и образа жизни, это:
- любые заболевания соединительной ткани (они воздействуют на сосуды, делая их слабыми и неупругими);
- артериальная гипертензия и гипертония (высокое АД усиливает нагрузку на сосудистые образования, приводят к перерастяжению их стенок);
- пристрастие к курению, алкоголю, наркотикам (под действием токсических веществ ткани сосудов активно разрушаются, что чревато возникновением аневризмы, быстрым увеличением ее объема и стимуляцией разрыва);
- механические повреждения (травмы головы), спровоцировавшие функциональные и дегенеративные изменения в мозговых артериях;
- атеросклеротические и инфекционные явления (менингит, грибковая инфекция, эндокардит и пр.), от которых сильно страдает качество артериального компонента головного мозга;
- внутричерепные новообразования доброкачественной или злокачественной формы (они нарушают прочность сосудистых стенок, могут ускорить разрыв уже существующей аневризмы).
В формировании аневризм сосудов головного мозга нередко виноват генетический фактор. Вам и всем членам семьи следует срочно обследоваться, если известно, что кто-то из прямых родственников связан с данным диагнозом.
Классификация аневризм головного мозга
Сосудистые аневризмы головного мозга в нейрохирургии принято классифицировать по локализации, форме, размеру, количеству камер в образовании. Рассмотрим каждый параметр.
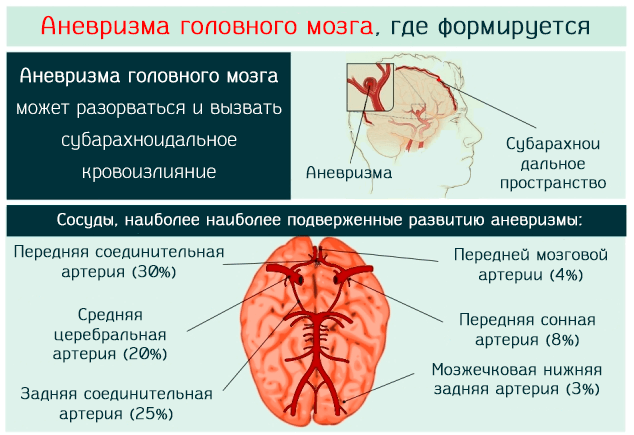
- По локальному признаку патологическое выпячивание бывает:
- передней мозговой/соединительной артерии (встречается в 45% случаев);
- внутреннего разделения сонной артерии (в 30%);
- средней мозговой артерии (в 20%);
- вертебробазилярного бассейна (4-5%);
- смешанного вида – поражены одновременно 2 и более отделов сосудистой сети (множественные очаги диагностируется у 10 % пациентов, у остальных же 90% определяется одиночная аневризма).
- По форме аневризматические расширения делят на:
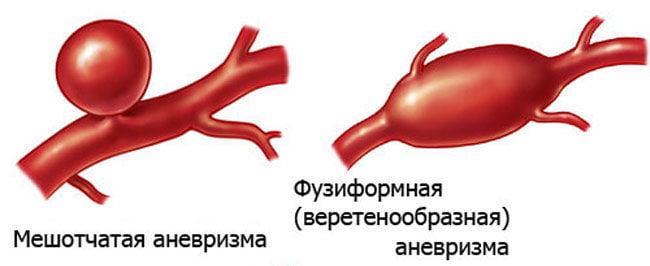
- мешковидные (мешотчатые) – самый распространенный вид формирований (98%), более других склонный к прободению;
- веретенообразные (фузиформные) – менее агрессивный и редкий тип образований, в структуре всех аневризм занимает лишь 2%;
- расслаивающиеся – образуются в межслойном пространстве сосудистой стенки, которое возникло из-за неплотного соединения ее слоев, куда под давлением попадает кровь (в артериях основания мозга развиваются в самых единичных случаях).
- Выпирание артериальной стенки по величине может быть:
- незначительным, или малым – до 4 мм;
- обычным, или средним – 5-15 мм;
- большим – 16-24 мм;
- гигантским – от 25 мм и более.
- По числу камер различают аневризму:
- однокамерную – состоит из одной камеры (типичное строение);
- многокамерную – ее рост происходит с формированием нескольких полостей.
Специалисты установили закономерность развития патологии у взрослых мужчин и женщин. Мужское население в 1,5 раза реже страдает от нее, чем женская популяция. В детском возрасте, напротив, болезнь преобладает немного чаще у мальчиков, чем у девочек (соотношение 3:2). У молодежи эпидемиология одинаковая.
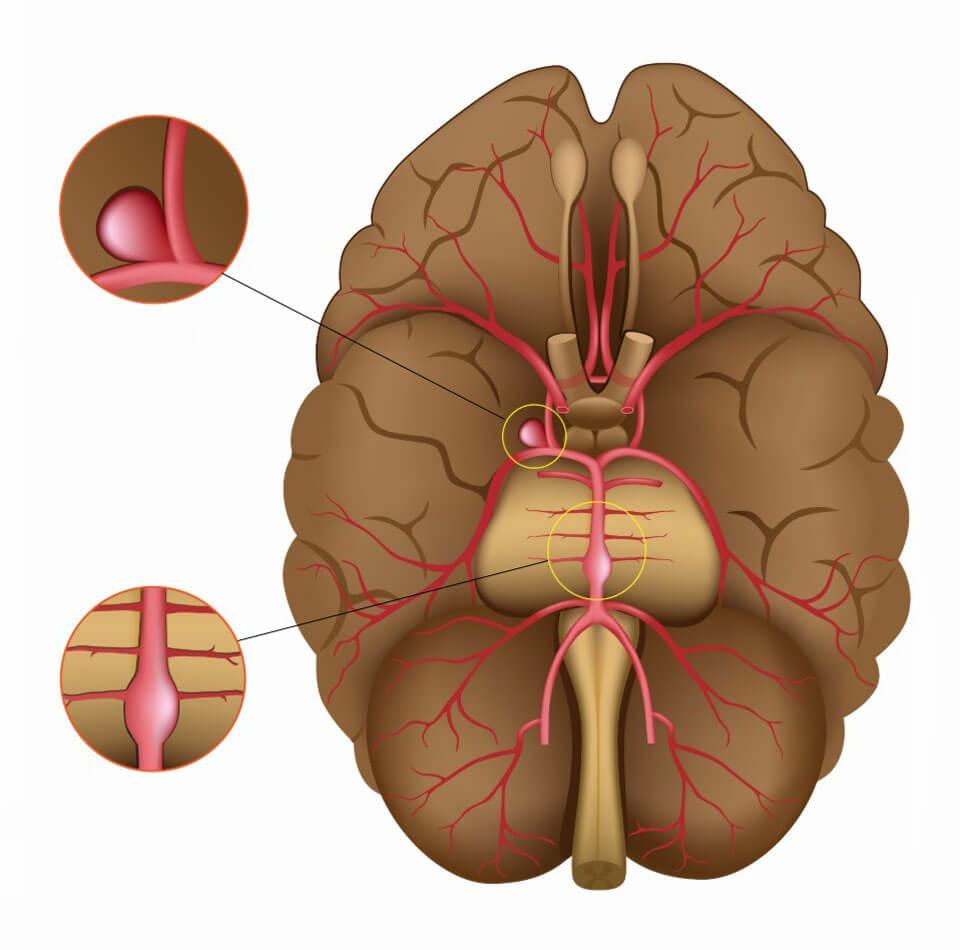
Схематичное изображение очагов в зависимости от расположения.
Симптомы аневризмы сосудов головного мозга
Как мы ранее отметили, в большинстве случаев аневризма клинически не проявляется, пока не наступит острая фаза разрыва. Но при крупных размерах, когда очаг серьезно давит на близлежащие структуры и нарушает передачу нервных импульсов, неврогенные симптомы обычно ощущаются. Поскольку мозговая аневризма ставит под угрозу жизнь человека, ее важно выявить на ранних стадиях, но беда в том, что никому и в голову не приходит обращаться в больницу при отсутствии или минимуме жалоб.
Врачи призывают каждого взрослого человека, тем более в возрасте после 35 лет, хотя бы 1 раз в год проходить диагностику сосудов головного мозга для своего же блага.
Теперь озвучим все возможные клинические признаки, которые в основном начинают тревожить при опасных объемах неразорвавшегося дефекта, когда затронуты черепные нервы:
- боль в области глаз, снижение или затуманенность зрения;
- расстройство слуха (снижение, ощущение шума),
- осиплость голоса;
- онемение, слабость, боль по ходу лицевого нерва, обычно с одной стороны лица;
- мышечный спазм в области шеи (невозможность коснуться подбородком груди);
- судороги скелетных мышц;
- слабость в руке или ноге;
- снижение чувствительности, нарушение тактильного восприятия на отдельных участках кожи;
- проблемы с координацией;
- головокружение, тошнота;
- необоснованная сонливость или, наоборот, бессонница;
- заторможенность движений и мыслительной деятельности.
Чтобы исключить или определить патологию, незамедлительно пройдите целевой медицинский осмотр, если отмечаете у себя хотя бы один симптом!
Последствия нелеченной аневризмы
Если сосуд разрывается, кровь изливается в головной мозг, специфика клинических признаков отличается большей конкретикой и выраженностью. Патогностический сценарий, присущий аневризматическому шоку, следующий:
- внезапная интенсивная головная боль, которая быстро распространяется и доходит до ужасного болевого пика;
- тошнота, многократная рвота;
- угнетение сознания различной продолжительности;
- менингеальный синдром;
- могут возникать судорожные припадки, напоминающие эпилептические;
- иногда повышение общей температуры тела, тахикардия, повышение/снижение АД;
- при массивной геморрагии из-за глубокого торможения в коре головного мозга человек впадает в кому с нарушением функций дыхания.
Тем, кто оказался рядом с таким пострадавшим (простой прохожий, друзья или родные), примите во внимание! От скорости вашей реакции сейчас зависит жизнь человека. Возникновение описанного симптомокомплекса (главные признаки в начале разрыва – первые 3 пункта) – сигнал к немедленному вызову бригады скорой помощи. Квалифицированные врачи окажут на месте адекватную первую помощь больному, отвезут в медучреждение для полного обследования и получения экстренной терапии.
Диагностические мероприятия
Обследование, позволяющее диагностировать аневризму сосудов головного мозга, построено на применении комплексной диагностики. Комплексный подход позволит выявить заболевание, установить его причину, точный участок эпицентра, количество поражений, разновидность, размер, взаимосвязь с мозговыми отделами и другими артериями.
Если говорить не об уже состоявшихся разрывах, а о намерении пациента обследоваться в целях проверки состояния сосудов, визит начинается с обращения к неврологу. Врач, досконально выслушав анамнез пациента, проводит общий физикальный осмотр, включающий:
- пальпацию отдельных частей тела на определение болезненных зон;
- перкуссию, или выстукивание участков тела для определения по характеру звука состояние испытуемых внутренних органов;
- аускультацию, которая помогает услышать ненормальные шумы в области сердца, сонной артерии как косвенный признак аневризмы мозга;
- стандартное измерение давления, позволяющее оценить уровень давления циркулирующей крови по артериям;
- оценку сердечного ритма, частоты дыхания (нередко патологические отклонения данных параметров свидетельствует о дисплазии соединительных тканей, инфекционных процессах);
- неврологические тесты, суть которых заключается в исследовании сухожильных, мышечных, кожных рефлексов, двигательных функций костно-мышечной системы, степень чувствительности в конечностях и туловище, пр.
На основании всех перечисленных методов предварительной оценки состояния поставить диагноз еще невозможно. Все эти способы могут лишь чисто гипотетически указывать на возможное (неточное) наличие данной болезни при обнаружении факторов риска. Поэтому далее специалист выписывает направления на базовые диагностические процедуры – прохождение инструментальных методов визуализации структур головного мозга. Их проводят на специальных аппаратах:
- компьютерной томографии (КТ);
- магниторезонансной томографии (МРТ);
- церебральной ангиографии.
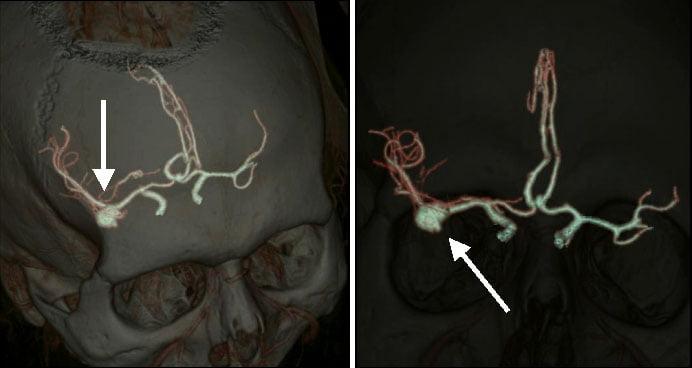
Стандартная ангиография наиболее выгодна по доступности цены для пациентов, пожелавших пройти первичный профилактический осмотр. Ее точность, конечно, ниже, чем у перспективных КТ и МРТ. Однако и ангиографическое исследование достаточно успешно справляется с задачей выявления аневризм, в том числе дает информацию о локализации, виде и масштабе расширения. Но для больных, поступивших в стационар с признаками разорвавшегося сосуда или давнего кровоизлияния, стандартом диагностики является использование всех указанных процедур. Наряду с ними выполняется электроэнцефалография (ЭЭГ) и транскраниальная допплерография (ТКДГ).
Принципы оказания первой помощи
До прибытия врачей те, кто находится рядом с больным, должны уметь оказать ему элементарную первую помощь. Инструкция срочных мер, направленных на спасение жизни до врачебного визита, понятно изложена далее.
- Уложить пострадавшего на ровную поверхность, голова обязательно должна находиться в возвышенном положении. Высокое положение головы поможет улучшить венозную циркуляцию крови, тем самым предупредить быстрое накопление жидкости в церебральных тканях и отекание мозга.
- Создать условия для хорошего притока свежего воздуха в месте, где произошел клинический инцидент. И крайне значимо освободить шею от стягивающих вещей, например, снять галстук, шейный платок, расстегнуть пуговицы на рубашке и т. п. Такая мера позволит посодействовать поддержанию функций кровообращения и притормозить процесс массовой гибели нервных клеток.
- Если больного человека настиг обморок, следует осуществить проверку дыхательных путей на проходимость. При запрокинутой голове нужно сделать нажатие на лоб с одновременным выдвижением нижней челюсти, захватив снизу подбородок. Открыв рот больного, произвести ревизию ротовой полости (пальцами) на присутствие инородного содержимого, западания языка. Надо извлечь съемные зубные протезы, если они есть. Чтобы человек не захлебнулся рвотными массами, вернуть голову на высокую подушку, повернув ее на бок.
- Для профилактики отека головного мозга и сокращения объемов кровоизлияния важно прикладывать к голове компрессы изо льда (можно использовать замороженные продукты, пакеты со льдом и др.).
- По возможности стоит наблюдать за изменением кровяного давления, используя тонометр, а также прослушивать биение сердца, следить за дыханием. Если в отсутствие врачей человек перестал дышать или его сердце прекратило биться, неотложно начинайте реанимационные мероприятия (искусственное дыхание, непрямой массаж сердца). Без них в этой ситуации риск трагического конца огромный.
К сожалению, даже все эти мероприятия не всегда оказываются эффективными после состоявшегося разрыва аневризмы. Смертельный исход у некоторых наступает молниеносно – в первые же минуты. Но без специального медоборудования и профессиональных знаний сложно понять, что творится в организме. Поэтому ценно не терять самообладания и веры в результат. Продолжайте беспрестанно бороться за жизнь, пока больного лично не передадите в руки специалистам.
Операция по удалению аневризмы сосудов головного мозга
Лечебная методика (хирургическая или безоперационная) определяется узкопрофильными докторами индивидуально на основании диагностических данных. При мелких аневризмах, которые не прогрессируют, могут быть предложены консервативные тактики. Их предназначение – уменьшение потенциала роста образования, снижение риска разрыва, купирование неврологических симптомов. Неинвазивная терапия – это обеспечение пациента качественным медикаментозным пособием, оказывающим поддерживающее действие за счет:
- сосудосуживающих средств;
- кардиотоников с антигипертензивным эффектом;
- противоэпилептических препаратов;
- обезболивающих таблеток;
- дофаминолитиков (от рвоты, тошноты).
Маленькие аневризмы, которые не оперируются, требуют постоянного наблюдения. При этом специалисты предупреждают, что избавиться от них консервативно нельзя. Поэтому основной подход в устранении заболевания и его последствий – нейрохирургическое лечение, то есть своеобразная операция на проблемном сосуде головного мозга.
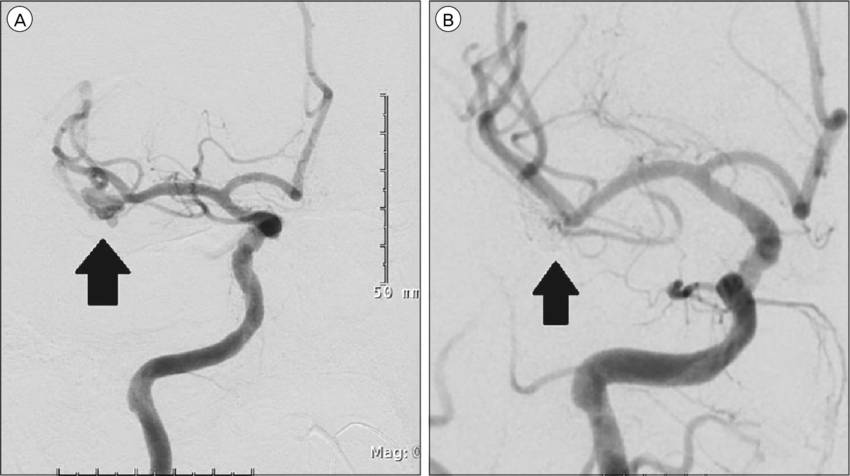
Слева состояние до операции, справа — после.
Выбор вида оперативного вмешательства зависит от показаний, места локализации, целостности, анатомических особенностей аневризмы сосуда, общего состояния пациента, степени угрозы жизни, технических возможностей нейрохирургического центра. Вмешательство может быть выполнено согласно одной из тактик хирургии.
- Эндоваскулярная операция – в полость сосуда (внутрь) чрескожным доступом (без вскрытия черепной коробки) под рентген-контролем вводится микрокатетер для установки сосудистого стента или спирали. Устройства полностью или субтотально «выключают» артерию из кровотока. Со временем аневризма тромбируется и уменьшается в размерах.
- Микрохирургическая (открытая под контролем микроскопа) – выполняется экономная трепанация черепа с последующим выделением несущей артерии и выполнением окклюзии путем наложения клипсы у основания шейки аневризмы. Клипсирование (сверху сосуда) позволяет пережать аневризматическую шейку, чем исключить из кровотока сосудистый дефект и свести к предельному минимуму вероятность его разрыва.
Видео как проходит операция по эндоваскулярному лечению нейрососудистой аневризмы головного мозга:
И лечебно-профилактические операции, и вмешательства по поводу разорванной аневризмы – сложнейший интраоперационный процесс, требующий величайшего опыта от микрохирурга, изумительного владения новыми нейрохирургическими технологиями, безупречной комплектации операционного блока.
Видео открытой операции по удалению:
Чехия — одно из немногих в мире государств, где приемы миниинвазивной современной нейрохирургии мозга освоены и отточены в совершенстве, послеоперационное ведение пациентов на высоте. Чешские нейрохирурги проводят ювелирной точности манипуляции даже в труднодоступных местах мозга, не прибегая к агрессивным открытым приемам. На заметку скажем, что стоимость нейрохирургических операций и реабилитации в Чехии в разы ниже, чем в Германии и Израиле.
Гид по эндоваскулярному лечению сосудистых заболеваний головного мозга
![]()
- Проблеме сосудистой патологии головного мозга уделяется большое внимание со стороны исследователей. Ежегодно на планете возникает 17,3 млн инсультов, умирает 6 млн человек, из них 29% — мужчин и 39% — женщин. Кыргызстан, к сожалению, относится к странам с высокими показателями заболеваемости и смертности от инсульта: ежегодно в Кыргызстане более 15000 людей получают инсульт, 80% из них становятся инвалидами по причине несвоевременно оказанной медицинской помощи и теряют трудоспособность в молодом возрасте! Доктор БОСТИ подготовил статью – гид по высокотехнологичным операциям, а именно эндоваскулярным вмешательствам при сосудистых заболеваниях головного и спинного мозга, выполняемых с помощью передовых медицинских технологий. Кроме того, Доктор БОСТИ поделился информацией о том, в каких клиниках Кыргызстана проводится качественная диагностика сосудов головного мозга.
Товар добавлен в избранное
Эндоваскулярное лечение сосудистых заболеваний головного мозга
Малоинвазивные вмешательства: эмболизация и стентирование
В большинстве случаев, эндоваскулярная эмболизация – наименее инвазивный на сегодня метод лечения аневризм сосудов головного мозга.
Эмболизация – к прекращению кровотока в аневризме (выпячивании), сохраняя нормальный кровоток по мозговой артерии с использованием специального материала (отделяемые микроспирали, стенты или баллоны); «заклеивание» специальным клеевым составом (цианакрилат) или жидким пластиком (поливинилакоголь – препарат “Onyx”), или же перекрытие микроспиралями из платины.

Рис. Эмболизация при аневризме
Проведение внутрисосудистой спиральной эмболизации возможно при мешковидной аневризме и небольшом просвете соустья. При широком просвете возможно одновременное наложение стента (закрытие просвета) с последующей спиральной эмболизацией аневризмы.
 Рис. Одновременное наложение стента (закрытие просвета) с последующей спиральной эмболизацией аневризмы
Рис. Одновременное наложение стента (закрытие просвета) с последующей спиральной эмболизацией аневризмы
В любом случае, тактику выбирает нейрорадиохирург после проведения ангиографии.
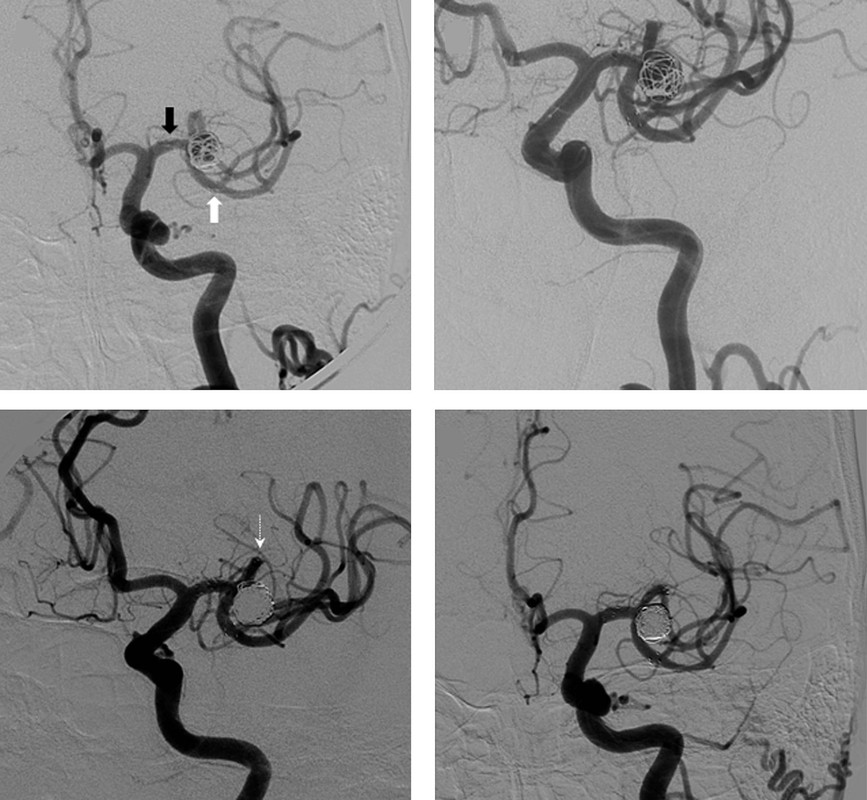 Рис. Ангиография сосудов головного мозга
Рис. Ангиография сосудов головного мозга
В процессе эмболизации через удобный сосудистый доступ (чаще паховый) под радиологическим контролем вводится катетер и проводится до аневризмы. Затем в катетер вводится более тонкий микро-катетер с уложенной внутри него проволочной микроспиралью, и заводится в полость аневризмы.
Как только кончик микрокатетера окажется в полости аневризмы, из микрокатетера высвобождается микроспираль, которая изменяет свою форму, и в виде беспорядочного мотка проволоки занимает собой полость аневризмы. При больших размерах аневризмы может понадобиться несколько спиралей. Заполненная проволочной спиралью аневризма выключается из кровотока и постепенно зарастает соединительной тканью, то есть, исключается возможность ее разрыва.
Эмболизация сосудов опухоли – малоинвазивная процедура, приводящая к прекращению “питания” опухоли и остановке ее роста.
Через прокол бедренной артерии по сосудам осуществляется доступ к объемному образованию. Процедура безболезненна и проводится без использования наркоза, под местной анастезией. С помощью специальных веществ (эмболизирующих материалов) сосуды, питающие опухоль, “заклеиваются”, после чего образование перестает расти.
Процедура применяется как самостоятельный метод лечения, а также как первый этап перед удалением опухоли.
При каких заболеваниях головного мозга применяется процедура эмболизации?
Современные достижения эндоваскулярной хирургии позволяют рассматривать этот метод как первый шаг в лечении таких заболеваний, как артериовенозная мальформация (АВМ) сосудов головного мозга, аневризма головного мозга, артериовенозная фистула.
Артериовенозная мальформация – патологический узел из переплетения тонких и извитых артерий и вен.
 Рис. Артериовенозная мальформация
Рис. Артериовенозная мальформация
Артерио‐венозная мальформация сосудов головного мозга – это врождённая патология сосудов головного мозга, требующая хирургического вмешательства. При отсутствии лечения АВМ существует высокий риск внутримозгового кровоизлияния. Современные методы эндоваскулярной хирургии позволяют провести малоинвазивное вмешательство для “выключения” аномального сосудистого образования из кровотока.
Дуральная артериовенозная фистула – патологическое сообщение между артериями и крупной веной головного мозга.

Рис. Дуральная артериовенозная фистула
Артериовенозная фистула провоцирует падение артериального давления, что приводит к увеличению числа сердечных сокращений. Иногда сопровождается сильной головной болью. Самое значимое осложнение, которое может привести к летальному исходу, – кровоизлияние в мозговую ткань.
Специалистами используется малоинвазивное эндоваскулярное вмешательство для облитерации («заклеевания» жидким пластиком или клеевым составом) просвета фистулы. Метод применяется когда открытое оперативное вмешательство невозможно из-за труднодоступности патологии, а также если пациент в тяжелом состоянии.
Аневризмы — одна из самых распространенных болезней сосудов головного мозга. Это истончение и выпячивание стенки артерии головного мозга. Самым опасным его проявлением может стать спонтанный разрыв аневризмы с кровоизлиянием в мозг. В таких случаях прогноз без высокотехнологичного лечения крайне неутешительный.

Рис. Аневризма
К сожалению, около 15% пациентов погибают в первые сутки, еще до поступления в стационар, у остальных в ближайшие полгода происходит повторное кровоизлияние, следом в 80% случаев летальный исход.
Рост аневризмы приводит к сдавлению окружающих нервов и структур мозга, что нередко вызывает снижение зрения, двоение или головные боли. Главная угроза аневризмы – разрыв ее стенок и кровоизлиянием под оболочки мозга или в вещество мозга с образованием внутримозговых гематом.
При данной патологии нейрохирургами применяется эмболизация – эндоваскулярное вмешательство, при котором специальным клеевым составом закупориваются кровеносные сосуды и кровоток по поврежденным сосудам будет прекращен.
Стентирование
Стентирование – восстановление кровотока по суженному участку сосуда с помощью стента, маленького сетчатого металлического каркаса, который помогает сохранить артерию открытой более длительно.
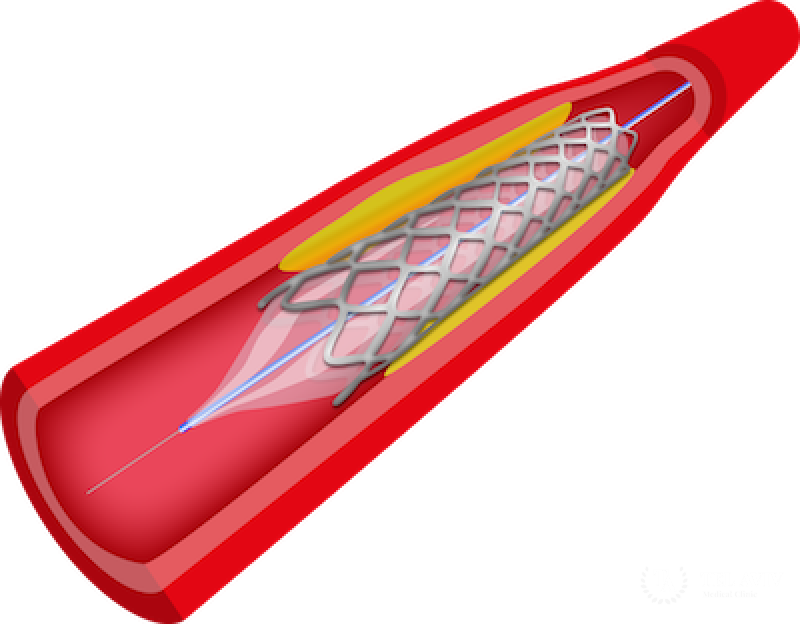 Рис. Стент
Рис. Стент
Стентирование сонной артерии – это процедура, заключающаяся в установке в просвет суженного сосуда тонкой проволочной конструкции в виде цилиндра, играющей роль каркаса – стента.
 Рис. Сонная артерия
Рис. Сонная артерия
Через катетер хирург вводит проводник со сдутым баллоном и стентом в пораженный участок. После проведения в место сужения баллончик со стентом расширяется до нормального диаметра сосуда. Имплантированный стент прижимается к стенкам сосуда и остается в этом положении, обеспечивая нормальный кровоток.
Процедура выполняется под местной анастезией и контролируется с помощью рентген-мониторов.
При каких заболеваниях головного мозга применяется процедура стентирования?
Процедура стентирования сосудов головного мозга проводится при сужении сонных артерий (атеросклерозе)
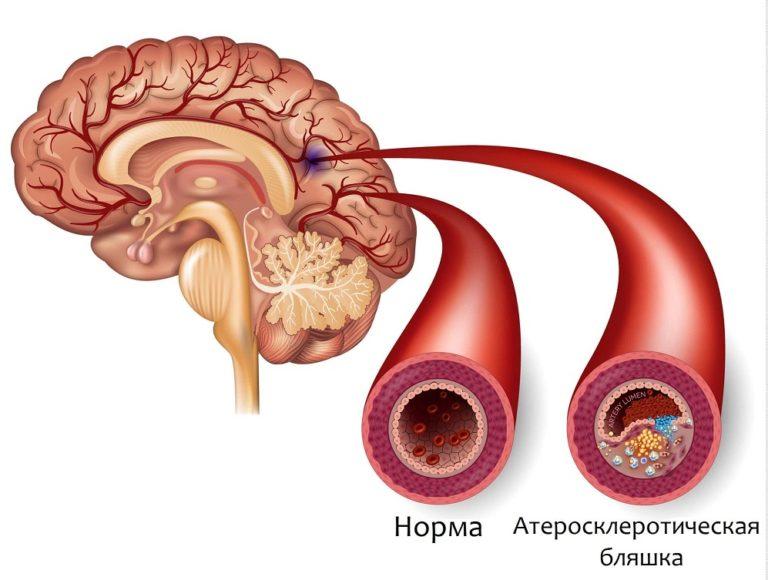
Атеросклероз – системный процесс, затрагивающий все артерии. Основное проявление атеросклероза – возникновение на внутренней стенке артерии атеросклеротических бляшек. Эти бляшки состоят из холестерина, кальция и фиброзной ткани. Постепенно увеличиваясь в объеме, бляшки сужают просвет артерий и нарушают нормальный кровоток. Когда бляшки образуются в просвете сонных артерий, нарушается мозговое кровообращение.

Рис. Атеросклероз сосудов головного мозга
Эндоваскулярные методы лечения заболевания артерий
Что такое «эндоваскулярная хирургия»?
Эндоваскулярная хирургия (endо — внутри, vascular — сосудистый) — современный метод лечения сосудистых заболеваний, при котором лечебное воздействие осуществляется изнутри сосуда.
Как проводятся эндоваскулярные вмешательства?
Эндоваскулярные вмешательства выполняются под местной анестезией через прокол в сосуде (как правило, пунктируется артерия на бедре или в области руки). Через прокол в сосуде вводится проводник, по которому в сосудистое русло доставляются катетеры и другие устройства, позволяющие осуществить лечебное воздействие на сосудистую стенку. Для выполнения эндовасулярных процедур требуется госпитализация больного в стационар на несколько дней. Ближайшие время после вмешательства (от нескольких часов до суток) пациент проводит в палате интенсивной терапии.
Какие методики лечения наиболее часто применяются в эндоваскулярной хирургии?
Баллонная дилатация (баллонная ангиопластика) — расширение просвета суженного сосуда изнутри специальным раздувающимся баллоном. Баллонная дилатация имеет хорошие результаты лечения только в определённых сосудистых бассейнах (например, подвздошные артерии). К сожалению, зачастую эффект от баллонной ангиопластики непродолжителен.
Стентирование — установка в просвет суженного или закупоренного сосуда цилиндрической пружинки (стента), расширяющей сосуд и восстанавливающей кровоток по ней. Стентирование относится к наиболее популярным хирургическим методам лечения атеросклероза, поскольку выполняется через небольшой прокол сосуда и легко переносится больными. Однако, этот метод лечения наиболее эффективен только при локальных и непротяжённых поражениях артерий, поэтому может быть применён далеко не у всех
Эндопротезирование — установка в просвет артерии трубки из синтетического материала, по окружности которой имеется вшитая саморасправляющаяся пружина в качетсве каркаса. Эндопротезирование чаще всего применяется в лечении сосудистых аневризм, например, аневризмы брюшного отдела аорты.
Эмболизация — установка в сосуд различных материалов (эмболов) для прекращения кровотока по нему. Эмболизация применяется при различных заболеваниях сосудистой и несосудистой природы, например, при опухолях матки, различных видах кровотечений, в лечении варикоцеле, а также при сосудистых мальформациях (артерио-венозная фистула, аневризма и другие).
Что такое ангиопластика?
Ангиопластикой называется процедура, при которой суженная артерия расширяется баллонным катетером, введенным в ее просвет, с последующей установкой в это место стента. Баллонный катетер устанавливается в место сужения артерии и раздувается для восстановления нормального диаметра сосуда. После этого в это место устанавливается стент для предотвращения повторного сужения (или закупорки) сосуда. Стент — это металлическая конструкция в виде пружинки, создающей каркас для сосуда, препятствуя повторному сужению сосуда в этом месте. Стентирование позволяет закрепить эффект баллонной дилатации на длительное время.
Какие существуют преимущества эндоваскулярной хирургии перед открытой операцией на сосудах?
Главным достоинством, которое делает эндоваскулярные методы лечения столь популярными, является низкий риск развития осложнений для пациента и меньший срок пребывания в стационаре в сравнении с открытыми хирургическими вмешательствами. Открытые операции в свою очередь имеют высокую эффективность в отдаленном периоде после вмешательства, но сопровождаются более длительной госпитализацией. Поэтому подход к выбору лечебной процедуры при сосудистых заболеваниях строго индивидуален и должен основываться на особенностях пациента и опыте специалиста.
При каких заболеваниях применяются эндоваскулярные методы лечения?
Эндоваскулярная хирургия применяется при заболеваниях различных сосудов, однако, наиболее часто ее применяют при поражении коронарных (артерии сердца), почечных, подвздошных, брахиоцефальных артерий и в лечении аневризм аорты.
Более подробную информацию о возможностях эндоваскулярных методов лечения вы можете получить в центре сосудистой хирургии клинической больницы № 122.
Запишитесь на прием
Сосудистый центр им. Т.Топпера оказывает квалифицированную помощь по всем видам заболеваний сосудов.
Для того, чтобы попасть на прием к сосудистому хирургу или пройти обследование просто позвоните по телефону +7 (812) 962-92-91 и согласуйте удобное для вас время.
Как подготовиться к операции
Вам предстоит оперативное лечение в нашем Центре. Подготовка к хирургическому вмешательству заключается в выполнении комплекса предоперационного обследования. По указанным ниже ссылкам Вы можете ознакомиться с перечнем необходимых исследований.

 Как проходит лечение
Как проходит лечение
