Тромбоз портальной вены (I81)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Обструкция портальной вены приводит к нарушению портального кровотока. Она может быть внепеченочной (вследствие тромбоза или врожденной атрезии портальной вены) или внутрипеченочной (микроваскулярная обструкция портальной вены при шистосоматозе).
Тромбоз портальной вены (обструкция портальной вены тромбом или опухолью) может локализоваться в различных ее отделах, в том числе и в селезеночных ветвях.
Основными причинами тромбоза портальной вены или селезеночной вены являются: цирроз печени , опухоли, панкреатиты , полицитемии, сепсис. У 50% пациентов причины возникновения тромбоза портальной вены установить не удается.
При остро возникшем тромбозе внезапно появляется боль в животе, тошнота. Нередко начальным симптомом является желудочно-кишечное кровотечение. В дальнейшем развивается асцит , в ряде случаев геморрагический. При вовлечении в процесс селезеночной вены отмечается боль в левом подреберье и быстрое увеличение селезенки.
При циррозе печени наблюдается хроническое течение тромбоза портальной вены. Он развивается длительно (от нескольких месяцев до нескольких лет).
Тромбоз портальной вены приводит к портальной гипертензии и желудочно-кишечным кровотечениям.
Диагноз основан на результатах допплеровского ультразвукового исследования, КТ и МРТ органов брюшной полости, ангиографии.
Лечение заключается в предупреждении возникновения желудочно-кишечных кровотечений, назначении антикоагулянтов и тромболитических препаратов.
Этиология и патогенез
Закрытие просвета (обструкция) портальной вены приводит к нарушению портального кровотока. Такое закрытие может быть вызвано закупоркой портальной вены тромбом. Обструкция и тромбоз портальной вены могут располагаться в различных ее отделах, но выше уровня слияния селезеночной и верхней брыжеечной вен.
- Причины развития тромбоза портальной вены
У 50% пациентов причины возникновения тромбоза портальной вены установить не удается.
Причины врожденного характера.
– Коагулопатии.
– Мутация гена протромбина (G20210).
– Мутация фактора V Лейдена.
– Дефицит протеина С .
– Дефицит протеина S.
– Дефицит антитромбина II.
Причины приобретенного характера.
– Цирроз печени .
– Системная красная волчанка.
– Ожоги.
– Злокачественные новообразования (холангиокарцинома, карцинома желудка и поджелудочной железы).
– Миелопролиферативные заболевания.
– Беременность/послеродовый период.
– Прием оральных контрацептивов.
– Травмы.
– Ятрогенная катетеризация пупочной вены.
– Абдоминальный сепсис.
– Хронический панкреатит .
– Инфекционные заболевания (аппендицит, дивертикулит, перинатальный омфалит, гнойный холангит).
– Трансплантация печени (тромбоз портальной вены осложняет течение послеоперационного периода в 5-15% случаев).
У взрослых тромбоз портальной вены в 24-32% случаев вызывается циррозом печени .
У 21-24% больных с обструкцией портальной вены обнаруживаются злокачественные опухоли (в большинстве случаев гепатоцеллюлярная карцинома и карцинома поджелудочной железы). Они оказывают компрессионное или прямое воздействие на портальную вену и приводят к формированию гиперкоагуляционного статуса.
Инфекционные заболевания брюшной полости также могут вызывать обструкцию и тромбоз портальной вены у взрослых пациентов, особенно при бактериемии возбудителем Bacteroides fragilis.
Миелопролиферативные заболевания, а также врожденные и приобретенные коагулопатии приводят к обструкции и тромбозу портальной вены в 10-12% случаев.
Венозный застой, вызванный резистентностью печеночной ткани, которая наблюдается при циррозе печени, также может провоцировать возникновение тромбоза портальной вены.
Портальная вена образуется слиянием селезеночной и верхней брыжеечной вен. Места обструкции и тромбоза локализуются выше уровня этого слияния.
При циррозе печени и злокачественных опухолях процесс тромбирования портальной вены начинается в ее внутрипеченочном отделе и распространяется на внепеченочную часть.
При тромбозе, вызванном другими причинами, патологический процесс возникает в месте начала портальной вены.
Тромбоз селезеночной вены, который наблюдается при хроническом панкреатите , также распространяется и на портальную вену.
Обструкция портальной вены не нарушает функцию печени до тех пор, пока у пациента не возникнет заболевание печени (например, цирроз). Это происходит за счет компенсаторного усиления кровотока в системе печеночных артерий.
Среднее время формирования коллатерального кровообращения составляет 5 недель; при остром тромбозе – 12 дней. При этом риск возникновения кровотечения из варикозно-расширенных вен пищевода, желудка и кишечника повышается. Развивается асцит .
Кавернозная мальформация портальной вены (т.е. развитие перипортальных коллатералей) возникает при длительном течении тромбоза портальной вены в результате разрастания мелких сосудов вокруг места тромбоза. Скорость кровотока по этим сосудам составляет 2-7 см/сек. На снимках, выполненных в ходе эндоскопической ретроградной холангиогепатографии, у пациентов с портальной гипертензией кавернозная трансформация портальной вены выглядит как губкоподобная масса, расположенная под печенью. Аналогичные данные можно получить и у пациентов с гемангиосаркомой поджелудочной железы, и у больных псевдохолангиосаркомой. После выполнения трансюгулярного внутрипеченочного портосистемного шунтирования и устранения явлений портальной гипертензии кавернозная мальформация портальной вены на снимках не визуализируется.
Эпидемиология
Обструкция портальной вены диагностируется у 5-18% пациентов с циррозом печени .
Частота возникновения тромбоза портальной вены у пациентов с гепатоцеллюлярной карциномой составляет 30%; у больных циррозом печени – 5%.
Смерть при обструкции портальной вены обусловлена возникновением кровотечений из варикозно-расширенных вен желудка, пищевода и кишечника.
Риск появления кровотечений в течение 2 лет у пациентов без цирроза печени составляет 0,25%, а смертность – 5%. Аналогичные показатели у больных циррозом печени: 20-30% и 30-70% соответственно.
У пациентов с тромбозом портальной вены показатели 10-летней выживаемости составляют 38-60%; у детей – 70%.
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Течение тромбоза портальной вены может быть острым и хроническим.
В некоторых случаях острая фаза заболевания может протекать бессимптомно. Для хронического течения тромбоза портальной вены характерно длительное развитие клинической симптоматики (от нескольких месяцев до нескольких лет).
У пациентов внезапно появляются боли в правом верхнем квадранте живота; беспокоит тошнота; может повышаться температура тела. Развивается асцит .
Могут возникать желудочно-кишечные кровотечения.
В хронической фазе тромбоз портальной вены может манифестировать симптомами портальной гипертензии . В 90% случаев в период 4-12 лет от начала формирования тромбоза возникает кровотечение из варикозно-расширенных вен пищевода, желудка и кишечника.
При наличии цирроза печени и признаков печеночной недостаточности , у пациентов с тромбозом портальной вены наблюдаются симптомы печеночной энцефалопатии, развивается асцит . При этом асцит и печеночная энцефалопатия – редкие осложнения, если у больного нет цирроза печени. Если у пациента имеются злокачественные новообразования, то симптомами тромбоза портальной вены являются: асцит , анорексия, снижение массы тела, боли в эпигастральной области или в верхнем правом квадранте живота.
Диагностика
- Рентгенография органов брюшной полости.
С помощью этого исследования можно выявить гепатоспленомегалию, варикозно-расширенные непарную, паравертебральные вены и варикозно-расширенные вены пищевода.
Эндоскопическая ретроградная холангиогепатография.
Кавернозная мальформация портальной вены (т.е. развитие перипортальных коллатералей) возникает при длительном течении тромбоза портальной вены в результате разрастания мелких сосудов вокруг места тромбоза. Скорость кровотока по этим сосудам составляет 2-7 см/сек. На снимках, выполненных в ходе эндоскопической ретроградной холангиогепатографии, у пациентов с портальной гипертензией кавернозная мальформация портальной вены выглядит как губкоподобная масса, расположенная под печенью. Аналогичные данные можно получить и у пациентов с гемангиосаркомой поджелудочной железы, и у больных псевдохолангиосаркомой. После выполнения трансюгулярного внутрипеченочного портосистемного шунтирования и устранения явлений портальной гипертензии кавернозная трансформация портальной вены на снимках не визуализируется.
УЗИ.
Чувствительность эндоскопического УЗИ для диагностики тромбоза портальной вены составляет 81%, специфичность – 93%. Тромб в портальной вене визуализируется как эхогенное образование в просвете портальной вены. Недавно сформировавшийся тромб может быть гипо- или анэхогенным.Допплеровское ультразвуковое исследование.
Чувствительность метода составляет 70-90%, специфичность – 99%. Ложно-позитивные результаты можно получить в 9% случаев у пациентов с циррозом печени из-за турбулентного кровотока в портальной вене.
В ходе этого исследования можно обнаружить: кавернозную мальформацию портальной вены, шунты, спленоренальные и портосистемные коллатерали, геатоцеллюлярную карциному , метастазы в печень , цирроз печени , опухоли поджелудочной железы.
В 38% случаев у пациентов с тромбозом портальной вены диаметр сосуда более 15 мм. При развитии портального флебита стенки сосуда утолщены, а просвет сужен. Можно выявить кальцифицированные тромбы.
Компьютерная томография – КТ.
Чувствительность метода составляет 65-85%.
С помощью этого исследования можно выявить тромб в просвете портальной вены, нарушения структуры печени, варикозно-расширенные вены пищевода и желудка.
При комбинировании этого метода с допплеровским ультразвуковым исследованием можно обнаружить обструкцию портальной вены.
Проводится также КТ-портография. На снимках тромбоз портальной вены визуализируется как участок пониженной плотности в просвете портальной вены, периферия которого определяется как зона повышенной плотности. Кроме того, у пациентов с портальной гипертензией можно обнаружить сеть коллатералей, варикозно-расширенные вены.
Магнитнорезонансная томография – МРТ.
Чувствительность, специфичность и точность метода составляет 100, 98 и 99% соответственно. С помощью этого исследования можно изучать состояние паренхимы печени (с целью выявления злокачественных опухолей); выявлять нарушения кровотока в системе портальной и печеночной вен (с целью решения вопроса о целесообразности хирургического лечения и для выбора необходимого метода). Кроме того, можно обнаружить коллатеральное кровообращение. Можно отдифференцировать причины тромбоза: кровяной тромб дает более интенсивное окрашивание при введении гадолиния, чем обструкция сосуда опухолью.
Остро возникший тромб (давностью менее 5-недельной) визуализируется как участок повышенной плотности в просвете портальной вены.
Ангиография.
Как правило, перед проведением шунтирующих операций или трансплантации печени, выполняются артериальная портография или спленопортография. С помощью этих методов можно оценить операбельность опухолей печени и поджелудочной железы. Кроме того, они незаменимы перед выполнением транскатетерной эмболизации опухолей или хемоэмболизации гепатоцеллюлярной карциномы .
Биопсия печени.
При наличии цирроза и злокачественных новообразований у пациента гистологическая картина биоптатов печени характерна для этих заболеваний.
У пациентов с тромбозом или обструкцией портальной вены, не страдающих циррозом и онкозаболеваниями, в биоптатах печени может не быть специфических изменений.
Лабораторная диагностика
- Общий анализ крови.
У больных циррозом печени наблюдается уменьшение количества тромбоцитов . Развитие анемии или других цитопений характерно для поздних стадий заболевания. При гиперспленизме развивается панцитопения (анемия, лейкопения, тромбоцитопения).
Выполняется для диагностики врожденных коагулопатий (мутация гена протромбина (G20210), мутация фактора V Лейдена, дефицит протеина С , дефицит протеина S , дефицит антитромбина II), которые могут стать причиной развития тромбоза портальной вены.
У пациентов с циррозом печени наблюдается снижение протромбинового индекса (отношение стандартного протромбинового времени к протромбиновому времени у обследуемого больного, выраженное и процентах). Референтные значения: 78 – 142 %.
Биохимический анализ крови.
У пациентов без цирроза печени и злокачественных новообразований может отмечаться незначительное увеличение показателей функции печени.
Дифференциальный диагноз
Дифференциальный диагноз тромбоза портальной вены проводится со следующими заболеваниями:
Тромбоз воротной вены ( Пилетромбоз )
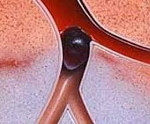
Тромбоз воротной вены – это полная или частичная окклюзия ствола воротной вены и ее ветвей тромботическими массами. Патология проявляется абдоминальным синдромом, рвотой, диареей, признаками портальной гипертензии (асцит, спленомегалия, расширение венозных коллатералей), осложняется кровотечением из верхних отделов пищеварительного тракта, инфарктом кишечника и другими состояниями. Основу диагностики составляют методы визуализации – УЗДС, МР- и КТ-ангиография, венография пораженных участков. Лечебная тактика предполагает антикоагулянтную терапию, тромболизис, хирургическую коррекцию.
МКБ-10
- Причины
- Патогенез
- Классификация
- Симптомы
- Стволовой тромбоз
- Радикулярный тромбоз
- Хронический тромбоз
- Осложнения
- Диагностика
- Лечение тромбоза воротной вены
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Тромбоз воротной вены (пилетромбоз) считается достаточно редким явлением, риск возникновения которого не превышает 1% в общей популяции. Его распространенность среди пациентов с циррозом печени варьируется от 0,6 до 26%, что, по-видимому, связано с различием в критериях выборки и диагностических методах. Заболевание называют причиной 5–10% случаев портальной гипертензии у жителей развитых стран и до 40% – в азиатском регионе (из-за более высокой частоты инфекционной патологии). Распространенность первичного тромбоза у взрослых и детей одинакова. Гендерных отличий в развитии болезни не выявлено, кроме цирротической обструкции, чаще диагностируемой у мужчин.

Причины
Заболевание имеет мультифакторную природу. Тромбоз развивается под влиянием системных и локальных нарушений, участвующих в повреждении сосудистой стенки, усилении коагуляции, замедлении венозного кровотока. Среди наиболее значимых причин отмечают следующие:
- Цирроз печени. Является основным этиологическим фактором, составляя 24–32% случаев тромботической окклюзии. Вероятность тромбоза повышается на поздних стадиях болезни, при необходимости трансплантации органа. Переход цирроза в гепатоцеллюлярную карциному увеличивает частоту внепеченочных пилетромбозов.
- Новообразования. Злокачественные новообразования печеночного или панкреатического происхождения являются причиной 21–24% случаев тромбоза. Развитие патологии опосредовано компрессией или прямой опухолевой инвазией, сопутствующей гиперкоагуляцией, гормональными сдвигами.
- Тромбофилии. Системные нарушения вызваны врожденными дефектами коагуляции – генетическими мутациями (фактора V Лейдена, протромбина, ингибитора активатора плазминогена), дефицитом протеинов C и S, антитромбиновой недостаточностью. К приобретенным факторам относят хроническую миелопролиферативную патологию, антифосфолипидный синдром, пароксизмальную ночную гемоглобинурию.
- Воспалительные заболевания. Патологический процесс может возникать на фоне абдоминальной воспалительной патологии (панкреатита, холецистита, гепатита), инфекционных заболеваний (малярии, брюшного тифа, амебиаза). У детей и новорожденных половина случаев тромбоза приходится на долю омфалита, пупочного сепсиса, аппендицита.
- Травмы и оперативные вмешательства. Воротная вена подвергается повреждению при травмах живота и хирургических вмешательствах на органах брюшной полости (спленэктомии, холецистэктомии, трансплантациии печени). Патология возникает после портосистемного шунтирования, тонкоигольной аспирационной биопсии печени, склеротерапии вен пищевода.
К другим факторам риска тромбоза воротной вены относят беременность, прием пероральных контрацептивов, гиперхолестеринемию. Отмечена роль внутрибрюшной аденопатии, синдрома системного воспалительного ответа. В детском возрасте окклюзия возникает при врожденных аномалиях сосудистой системы (дефектах межжелудочковой и межпредсердной перегородок, деформации полой вены) и желчевыводящих путей. Причина 10–30% тромботических стенозов остается невыясненной.
Патогенез
Исходя из современных представлений, пилетромбоз является результатом системных коагулопатий (наследственных, приобретенных) и действия локальных факторов. Повреждение стенки сосуда опухолью, инвазивными процедурами или травмами характеризуется выработкой цитокинов, активацией тромбоксана A2 и тромбина, усилением адгезии и агрегации тромбоцитов. Венозный застой при наружной компрессии сопровождается гипоксией эндотелия, накоплением активированных факторов свертывания. Все это запускает формирование пристеночного кровяного сгустка с дальнейшим его увеличением.
Сосудистая окклюзия сопровождается портальной гипертензией, что ведет к изменению системной и внутриорганной гемодинамики. Печень теряет около 2/3 своего кровоснабжения, но это компенсируется дилатацией печеночной артерии и быстрым развитием сети коллатералей. Вокруг тромбированной вены формируется кавернома, а сама она превращается в фиброзный тяж. Новообразованные сосуды расположены в пределах желчных протоков и пузыря, поджелудочной железы, антрального отдела желудка, двенадцатиперстной кишки.
Патогенез тромбоза при печеночном циррозе до конца не ясен. Важное значение отводят портальной гипертензии с замедлением кровотока по воротной вене, периферическому лимфангииту, перипортальному фиброзу. Системное шунтирование крови провоцирует гемосидероз, гепатоциты в зонах гипоперфузии подвергаются апоптозу. В тонком и толстом кишечнике выше уровня окклюзии определяются застойные явления, в желудке – гастропатия. Брыжеечная ишемия может привести к переходу тромботического процесса на мезентериальные сегменты.
Классификация
Формальной классификации тромбоза воротной вены не существует. Согласно клиническим рекомендациям по портальной гипертензии, при постановке диагноза учитывают участок тромбоза и его проявления, наличие и характер основного заболевания, степень окклюзии (частичную, полную), вовлеченность внепеченочных сегментов. В зависимости от локализации тромба различают несколько форм патологии:
- Стволовая (трункулярная). Участок окклюзии расположен в стволе воротной вены, дистальнее слияния селезеночной и верхней мезентериальной. Возникает первично или путем распространения из корешкового сегмента.
- Радикулярная (корешковая). Характеризуется поражением корешковых ветвей – селезеночной вены и брыжеечных сосудов.
- Терминальная. Пилетромбоз распространяется на внутрипеченочные разветвления и капилляры, сопровождаясь мелкими или развитыми коллатералями.
Представленная классификация позволяет оценить последствия тромботической обструкции и трудоспособность пациента. При поражении сначала интерстициальных сосудов, а затем крупных стволов констатируют восходящий (первичный) процесс. Мезентериальный тромбоз, возникающий из-за обструкции воротной или селезеночной вен, называют нисходящим (вторичным). В клинической флебологии также различают острую, подострую и хроническую стадии, последовательно сменяющие друг друга.
Симптомы
Клиническая картина тромбоза воротной вены определяется происхождением, степенью, протяженностью, локализацией, темпами нарастания окклюзии, выраженностью коллатералей. Частичное тромбирование протекает бессимптомно, выявляясь лишь при инструментальной диагностике, полной обструкции (90–100% просвета) присуще бурное развитие за несколько суток. Подострая форма прогрессирует на протяжении 4–6 недель, а хронический процесс характеризуется медленным нарастанием симптоматики (от нескольких месяцев до года).
Стволовой тромбоз
Острый стволовой пилетромбоз проявляется резкими болями в правом подреберье и эпигастрии, сочетающимися с метеоризмом, частой рвотой, диареей (нередко с примесью крови). Быстро нарастают признаки портальной гипертензии – расширение подкожных, пищеводных, геморроидальных вен, асцит. Зачастую выявляют желтуху, недостаточность печеночной функции. Общее состояние пациентов быстро становится тяжелым, что в основном обусловлено рецидивирующими кровотечениями из желудочно-кишечного тракта.
Радикулярный тромбоз
Радикулярный тромбоз на уровне селезеночного сегмента начинается остро, с боли в левом подреберье, кровавой рвоты и дегтеобразного стула. Увеличение селезенки и субфебрильная лихорадка сочетаются с обычными размерами печени. В подостром периоде постепенно нарастают спленомегалия, асцит, расширяется венозная сеть на животе. Терминальная форма патологии выявляется только при распространенном поражении – у таких пациентов обычно определяют увеличенную селезенку, широкие подкожные коллатерали.
Хронический тромбоз
Хронический пилетромбоз не имеет специфических проявлений. Отсутствие аппетита и общая слабость – иногда единственные симптомы болезни. У большинства пациентов выявляют подкожные анастомозы, умеренный асцит. В 20–40% случаев патология манифестирует кровотечением из варикозных расширений пищевода. Вялотекущие варианты тромбоза воротной вены характеризуются нерезким болевым синдромом, субфебрилитетом, чувствительностью печении при пальпации. Отмечаются спленомегалия с признаками гиперспленизма, тяжестью в подреберье, исхуданием.
Осложнения
Наиболее опасное следствие острой окклюзии мезентериальных сосудов – инфаркт кишечника с развитием перитонита и полиорганной недостаточности (характерно для 5% случаев). Большинство осложнений длительного пилетромбоза обусловлено портальной гипертензией. Расширение пищеводных вен у многих пациентов сопровождается кровотечением, риск которого в 100 раз выше при циррозе печени. Выраженное портосистемное шунтирование приводит к печеночной энцефалопатии, вторичным изменениям в желчевыводящих путях (портальной билиопатии, холангиопатии). При сохраняющихся факторах риска тромбозы могут рецидивировать, осложняться эмболизацией.
Диагностика
Отсутствие специфических признаков тромбоза, необходимость определения предпосылок, уровня, степени и последствий поражения создают потребность в комплексном обследовании пациента. Основой диагностической программы выступают методы инструментальной визуализации:
- УЗАС воротной вены. Обладая высокой специфичностью (60–100%), признано методом выбора при первичной диагностике. УЗДС определяет неоднородный очаг повышенной эхогенности с нечеткими контурами, частично или полностью перекрывающий сосудистый просвет. Допплеровское картирование дает возможность выявить отсутствие кровотока в вене и ее притоках, наличие портосистемных шунтов, каверноматозную трансформацию.
- КТ и МР-ангиография сосудов.КТ с контрастированием дает точную информацию о состоянии венозных стенок, протяженности тромбированных участков, наличии перивисцеральных коллатералей, варикозных вен в забрюшинном пространстве. Магнитно-резонансную ангиографию используют для выяснения состоятельности портального кровотока, оценки просвета шунтов – ее результаты более надежны, чем УЗДС.
- Портальная венография. Используется в случаях, когда неинвазивными методами подтвердить или исключить тромботическое поражение не удается. Контрастная венография выявляет не только стенозы, но и дефекты наполнения от сдавления извне. Однако при установленной проходимости сосуда в ней нет необходимости.
Проводя диагностику пилетромбоза, врачи-флебологи обращают внимание на показатели коагулограммы (увеличение фибриногена, протромбинового индекса, замедление времени свертывания крови), низкий уровень антитромбина. Выявить варикозно-расширенные вены пищевода позволяет ФГДС, исключить цирроз удается благодаря эластографии и биопсии печени. Дифференциальная диагностика осуществляется с печеночным шистосомозом, тромбозом нижней полой вены, сдавливающим перикардитом, рестриктивной кардиомиопатией.
Лечение тромбоза воротной вены
Задачами лечебной коррекции являются восстановление проходимости сосуда, предотвращение прогрессирования патологии, устранение осложнений венозной гипертензии. Исходя из остроты процесса, возраста пациента, этиологических и прочих факторов, применяют комбинацию консервативных и радикальных методов:
- Антикоагулянтная терапия. Является лучшим способом для реканализации венозного просвета, но единого мнения о ее применении нет. Длительность лечения антикоагулянтами (низкомолекулярными гепаринами, пероральными средствами) у лиц с острым пилетромбозом составляет от 3 до 6 месяцев, а при хроническом решается в индивидуальном порядке.
- Введение тромболитиков.Регионарный тромболизис (введение стрептокиназы, альтеплазы, тенектеплазы) транспеченочным или трансъюгулярным доступом позволяет обеспечить реканализацию, избежав побочных эффектов антикоагулянтной терапии. При острой тотальной или субтотальной окклюзии может выполняться системный тромболизис.
- Хирургические методы. При неэффективности консервативных мероприятий операцией выбора является дистальное спленоренальное шунтирование. В условиях нарушенной проходимости селезеночного участка накладывают мезентерикопортальный или мезентерикокавальный анастомоз с применением сосудистых протезов.
Варикозные расширения пищевода лечат с помощью лигирования, эндоскопической склеротерапии. В ургентных ситуациях при кровотечении могут производить операции азигопортального разобщения (гастротомию с прошиванием нижней трети пищевода, деваскуляризацию желудка). Тяжелый гиперспленизм требует спленэктомии.
Прогноз и профилактика
В целом прогноз при заболевании относительно благоприятный. Сгустки могут подвергаться асептическому аутолизу, организации, васкуляризации. Десятилетняя выживаемость для взрослых достигает 60%, а общий уровень смертности составляет менее 10%. При наличии цирроза и злокачественных новообразований прогноз ухудшается. Иногда тромбы превращаются в эмболы, становятся источником сепсиса. Но своевременное и интенсивное лечение приводит к реканализации сосуда, что сопровождается полным клиническим выздоровлением. Профилактика рецидивов проводится путем назначения антикоагулянтов.
Портальная гипертензия
 Портальная гипертензия – повышение давления в венах брюшной полости вследствие нарушения венозного оттока через венозную систему печени. Следствием портальной гипертензии является варикозное расширение вен органов брюшной полости с истончением их стенок, что может привести к тяжелым кровотечениям, угрожающим жизни пациента.
Портальная гипертензия – повышение давления в венах брюшной полости вследствие нарушения венозного оттока через венозную систему печени. Следствием портальной гипертензии является варикозное расширение вен органов брюшной полости с истончением их стенок, что может привести к тяжелым кровотечениям, угрожающим жизни пациента.
Чаще всего портальная гипертензия развивается у больных с циррозом печени и является одним из факторов, приводящим к летальному исходу при данном заболевании. Для портальной гипертензии характерно расширение вен передней брюшной стенки, геморроидальных вен и вен пищевода. Печеночная недостаточность при циррозе печени приводит к недостаточной выработке белков свертывания крови, поэтому у этих пациентов повышенная кровоточивость. Этим обусловлена высокая летальность от кровотечений при портальной гипертензии. Даже при современном состоянии медицины летальность при кровотечении из варикозно расширенных вен составляет более 50%.
Лечение портальной гипертензии в Инновационном сосудистом центре
В Инновационном сосудистом центре для лечения портальной гипертензии применяются как классические операции по созданию сплено-ренальных анастомозов, так и экстренные эндоваскулярные операции трансъягулярного портокавального шунтирования (TIPS).
Эндоваскулярные операции выполняются на ангиографическом комплексе с дополнительным использованием визуализации воротной вены с помощью УЗИ навигации. Такие вмешательства проводятся под местной анестезией с внутривенной седацией.
Операции сплено-ренального анастомоза выполняются у сохранных пациентов, перенесших кровотечение из варикозно-расширенных вен пищевода. Такие вмешательства мы выполняем под наркозом через доступ в левой боковой стенке живота с переходом на грудную клетку. Подобные вмешательства позволяют избежать смертельно-опасных осложнений портальной гипертензии.
 Причины и факторы риска
Причины и факторы риска
Портальная гипертензия возникает, когда что-то препятствует кровотоку через печень, повышая давление внутри воротной вены. Эта обструкция (закупорка) может быть внутрипеченочной, подпеченочной (внепеченочной) или надпеченочной.
Внутрипеченочные причины портальной гипертензии
Основной причиной возникновения гипертензии является цирроз (в 70% случаев). Есть много причин возникновения цирроза, наиболее распространенной из них является злоупотребление алкоголем. Цирроз печени может вызвать обширный фиброз (рубцевание). Интенсивное рубцевание препятствует прохождению жидкостей через печень. Фиброз окружает сосуды в печени, что затрудняет кровообращение.
В качестве причины портальной гипертензии выступает большое количество болезней:
- Вирусный гепатит,
- Аутоиммунный гепатит,
- Фиброз печени,
- Опухолевый процесс в печени,
- Болезнь Вильсона, врожденное нарушение метаболизма меди,
- Гемохроматоз, избыточное накопление железа,
- Муковисцидоз, системное наследственное заболевание,
- Холангит, воспаление желчных протоков, связанное с инфекцией,
- Атрезия желчных путей, слабо образованные желчные протоки,
- Инфекции,
- Некоторые метаболические заболевания.
Подпеченочные причины портальной гипертензии
- Тромбоз воротной и селезёночной вены,
- Врожденные аномалии воротной вены, в частности атрезия,
- Сдавление воротной вены опухолью,
- Гематологические заболевания.
Надпеченочные причины портальной гипертензии
Эти причины вызваны обструкцией кровотока из печени в сердце и могут включать:
- Тромбоз печеночной вены, синдром Бадда-Киари,
- Травматический тромбоз нижней полой вены,
- Слипчивый перикардит, воспаление околосердечной сумки, характеризующееся увеличением проницаемости и расширением кровеносных сосудов.
Международные данные по распространенности портальной гипертензии неизвестны, хотя известно что 80% пациентов страдают от портальной гипертензии из-за внутрипеченочных причин, то есть цирроза печени.
Течение заболевания
Течение заболевания можно разбить на 4 стадии:
I стадия — начальная
Заболевание уже появилось, но ещё не может диагностироваться. Протекает бессимптомно, либо пациенты ощущают тяжесть в правом подреберье и легкое недомогание.
II стадия — умеренная
Появляются выраженные клинические симптомы заболевания. Боли в верхней половине живота, метеоризм, расстройства пищеварения (отрыжка, изжога, тяжесть в животе и т.д.), спленомегалия и гепатомегалия (увеличение печени).
III стадия — выраженная
Присутствуют все признаки и симптомы портальной гипертензии в резко выраженной форме.
IV стадия — стадия осложнений
Развивается напряженный асцит, плохо поддающийся терапии, повторяющиеся кровотечения, а также возможные осложнения.
Осложнения
Основные осложнения: желудочно-кишечные кровотечения, асцит и печеночная энцефалопатия (печеночная недостаточность, комплекс психических, нервных и мышечных нарушений).
Спленомегалия часто вызывает анемию, низкие показатели лейкоцитов и низкие показатели тромбоцитов.
Общими осложнениями, связанными с портальной гипертензией, являются аспирационная пневмония, сепсис, почечная недостаточность, кардиомиопатия, аритмии и гипотония.
Портальная гипертензия является опасным заболеванием, поскольку может вызвать кровотечение. Во многих случаях эпизоды кровотечения считаются неотложными медицинскими ситуациями, потому что смертность от варикозных кровотечений составляет около 50%. Варикоз пищевода очень распространен у людей с прогрессирующим циррозом, и считается, что у каждого из трех человек с варикозом развивается кровотечение.
Прогноз
Портальная гипертензия является осложнением основного заболевания печени. Это заболевание часто можно контролировать, а выживаемость зависит от сохранения функций печени. Чем хуже печень выполняет свои функции, тем хуже прогноз.
Более высокие показатели смертности и заболеваемости у пациентов с тяжелым и стойким желудочно-кишечным кровотечением. Смертность пациентов с диагнозом варикозного расширения вен пищевода составляет 30%.
Пациенты, которые имели хотя бы один эпизод кровотечения из-за варикоза пищевода, имеют 80% шансов повторного кровотечения в течение 1 года. У пациентов с варикозом пищевода осложнения иммунных, сердечно-сосудистых и легочных систем способствуют примерно 20-45% смертей.
Преимущества лечения в клинике
Диагностика
 Варикозное расширение вен пищевода
Варикозное расширение вен пищевода
Когда кровь не может легко протекать через печень, она пытается обойти портальную систему, используя венозную систему, чтобы вернуться к сердцу. Возникают осложнения, связанные со снижением кровотока через печень и повышенным давлением внутри вен, что приводит к расширению вен. Варикоз может возникать в пищеводе, желудке и прямой кишке.
- Кровотечение из варикозно-расширеных вен
Когда кровь пытается найти другой путь к сердцу, открываются новые кровеносные сосуды. Среди них те, которые проходят вдоль стенки верхней части желудка и нижнего конца пищевода. Эти вены могут кровоточить. Кровотечение может быть мягким, в этом случае анемия является наиболее распространенным симптомом; либо серьезным, сопровождающееся кровавой рвотой или меленой (черным, смолистым стулом, который появляется из-за кровотечения из верхних отделов желудочно-кишечного тракта). Варикоз пищевода и желудка может привести к кровотечениям, угрожающим жизни.
Брюшная водянка — избыточное скопление жидкости внутри брюшины, обусловленное сочетанием факторов, включая повышенное давление в портальной системе, застой крови и уменьшение уровня белка в крови. Асцит может достигать огромных размеров, сдавливая диафрагму и мешая нормальному дыханию.
- Печеночная энцефалопатия
Обратимое расстройство нервной и психической деятельности при заболеваниях печени. Проявляется спутанностью сознания, раздражительностью и сонливостью из-за накопления токсических веществ из-за неспособность печени адекватно фильтровать их.
- Спленомегалия
Увеличение селезенки основной симптом при внепеченочной гипертензии, часто сопровождается анемией и тромбоцитопенией (низким уровнем тромбоцитов в кровотоке).
Снижение количества лейкоцитов в крови увеличивает риск инфицирования. Спонтанный бактериальный перитонит наиболее частое инфекционное заболевание, сопровождающее цирроз и печеночную гипертензию. Сопровождается ознобом, лихорадкой и болью в животе.
Портальная гипертензия является опасным осложнением многих заболеваний печени и несет значительные риски для жизни. Диагностика данного заболевания основана на клинических данных, результатах ультразвуковых и эндоскопических исследований желудка.
Лабораторные исследования позволяют оценить функцию печени и почек, что влияет на прогноз заболевания. С целью подготовки к возможному вмешательству при портальной гипертензии используются методы визуализации сосудов воротной системы. Нами используются методы компьютерной томографии и магнито-резонансной диагностики вен брюшной полости.
В клинике применяются следующие диагностические методы:
Лечение
Лечение портальной гипертензии представляет собой сложную задачу. Сложность связана с тем, что развивающаяся печеночная недостаточность обуславливает плохую переносимость тяжелых сосудистых вмешательств. Однако в нашей клинике отработали технологии лечения портальной гипертензии с низким риском для жизни пациента.
Операции по поводу кровотечений из вен портальной системы
- Операции на желудке и пищеводе
При кровотечениях из варикозно-расширенных вен пищевода нередко применяются методы прямого хирургического гемостаза – прошивание кровоточащих вен после рассечения желудка. Такие операции, выполняемые на фоне кровотечения, часто заканчиваются неблагоприятно для пациента. Летальность после таких операций составляет не менее 40%. Иногда общие хирурги дополняют эту операцию спленэктомией, исходя из соображений уменьшения притока крови из-за перевязки селезеночной артерии.
 Использование зонда Блэкмора
Использование зонда Блэкмора
Специальный двухкомпонентный зонд позволяет плотно сжать верхний отдел желудка и нижний отдел пищевода, придавив расширенные вены. Наряду с другими мероприятиями (переливанием плазмы, крови и гемостатических препаратов) позволяет остановить тяжелое желудочно-кишечное кровотечение. Остановка кровотечения не устраняет его причины, поэтому неизбежен рецидив. Но использование этого зонда позволяет отложить вмешательство на портальной системе на более спокойный период и провести его в плановом порядке. Держать зонд в раздутом состоянии рекомендуется не более 6 часов, после чего распускать его на час. Общая продолжительность использования не должна превышать более 2 суток.
- Эмболизация вен пищевода и селезеночной артерии
Эндоваскулярная технология остановки кровотечения из варикозно-расширенных вен пищевода. Редко выполняется как самостоятельное вмешательство, так как требует чреспеченочного доступа, однако применяется совместно с созданием транспеченочного портокавального анастомоза (TIPS). В просвет варикозно-расширенных вен вводятся спирали и микроэмболы, которые блокируют кровоток в кровоточащих сосудах и способствуют остановке кровотечения.
ТИПС – транспеченочное портокавальное шунтирование
Современный высокотехнологичный метод лечения портальной гипертензии, применяемый в экстренном порядке или как подготовка к пересадке печени. Смысл вмешательства заключается в создании искусственного соустья между ветвями воротной вены в толще печени и печеночной веной из системы нижней полой. В результате улучшается отток из воротной системы и снижается давления в варикозно-расширенных венах пищевода. Кровотечение быстро останавливается.
Возможности ультразвукового исследования с цветовым допплеровским картированием в диагностике тромбоза в системе воротной вены


Журнал “SonoAce Ultrasound”
Содержит актуальную клиническую информацию по ультрасонографии и ориентирован на врачей ультразвуковой диагностики, выходит с 1996 года.
Тромбоз воротной вены (ВВ) – процесс образования тромба вплоть до полной окклюзии просвета сосуда, дренирующего русло органов желудочно-кишечного тракта. Тромбоз воротной вены является редким заболеванием сосудов печени. Он может быть результатом большого количества различных заболеваний и оставаться бессимптомным или проявляться симптомами основного заболевания [1-4]. Диагностика заболевания сложна. Прогноз при тромбозе воротной вены всегда серьезен и неблагоприятен, часто наблюдаются смертельные исходы вследствие кровотечений или печеночной комы.
Цель работы – показать на клинических примерах возможности ультразвукового исследования с цветовым допплеровским картированием (ЦДК) в диагностике тромбоза в системе воротной вены.
Прижизненный диагноз тромбоза основного ствола воротной вены в России впервые поставил С.П. Боткин в 1862 г. В 1934 г. Н.Д. Стражеско впервые в мировой литературе описал прижизненно распознанный тромбоз правой ветви ствола воротной вены и на основании собственных исследований и данных литературы разработал симптоматологию закупорки правой ветви воротной вены.
Достоверных сведений о частоте тромбоза воротной вены нет. По секционным данным, тромбоз выявляют в 0,14-0,34% всех вскрытий (L. Lissauer, 1908; L.Т. Webster, 1921; Е.С. Pallette, 1936). По другим данным (А.И. Грицюк, 1973), при вскрытии умерших от основных сердечно-сосудистых заболеваний (атеросклероза, гипертонической болезни, эндокардитов и пороков сердца) тромбоз воротной вены был обнаружен в 0,56% случаев (у 10 из 1763 умерших), что составляет 0,8% всех тромбоэмболий, развивающихся при этих заболеваниях. Известно, что тромбоз воротной вены поражает до 30% больных гепатоцеллюлярной карциномой и до 5% больных портальной гипертензией на фоне цирроза печени.
Возникновение заболевания, как и иных венозных тромбозов, может быть объяснено триадой Вирхова, в которую входят следующие элементы.
- Травма стенки вены во время хирургической операции.
- Снижение скорости потока крови в воротной вене: сдавление сосуда извне опухолью, рубцами, эхинококковой кистой, альвеококком; хроническая сердечная недостаточность; констриктивный перикардит; синдром Бадда – Киари (тромбоз печеночных вен).
- Повышение свертываемости крови либо изменение соотношения ее клеточных элементов: в послеоперационном периоде – особенно у онкологических больных, а также после спленэктомии; при воспалительных процессах – как осложнение острого аппендицита, при гнойных холангите и лимфадените гепатодуоденальной связки, язвенном колите; панкреонекрозе; умбиликальной инфекции в неонатальном периоде (неонатальная септициемия, омфалит, инфицирование при катетеризации пупочной вены с целью обменного переливания крови); при осложнениях беременности (в частности, эклампсии); при некоторых гематологических заболеваниях, обусловливающих повышение свертываемости крови (например, псевдосиндром Банти при висцеральном лейшманиозе).
Клиническая картина зависит от локализации и протяженности тромбоза воротной вены, быстроты его развития и природы предрасполагающего заболевания печени. Наиболее тяжелое проявление заболевания – инфаркт печени либо атрофия ее сегмента. Однако в 1/3 случаев тромбоз формируется медленно, вследствие чего успевает развиться коллатеральный кровоток, а воротная вена со временем реканализируется и происходит ее кавернозная трансформация. Тем не менее даже при относительно благоприятном течении заболевания развивается портальная гипертензия [1-4].
При диагностике тромбоза воротной вены следует обратить внимание на коагулограмму: повышение содержания фибриногена, появление активированного фибриногена Б, увеличение протромбинового индекса, уменьшение времени свертывания крови [2].
При ультразвуковом исследовании (УЗИ) в серошкальном режиме в просвете воротной вены можно выявить неоднородное образование повышенной или смешанной эхогенности, с неровными, нечеткими контурами, препятствующее кровотоку, размеры которого могут быть различными: от 0,5 см до полной окклюзии воротной вены и/или ее ветвей (рис. 1, а). Эхогенность тромба чаще является более высокой, чем окружающей его крови. Однако на ранних стадиях формирования эхогенность может отличаться настолько незначительно, что визуализация тромба чрезвычайно сложна. Могут определяться увеличение диаметра сосуда с нечеткостью контуров, увеличение печени и снижение ее эхогенности, увеличение селезенки. Могут быть найдены первопричины тромбоза воротной вены: гепатоцеллюлярная карцинома, метастазы, цирроз печени, новообразования поджелудочной железы и др. При пилефлебите обнаруживают абсцессы печени [3].
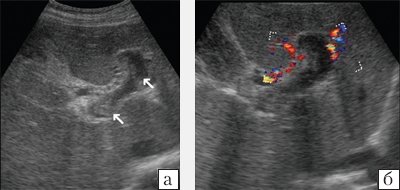
a) В-режим. Неоднородное образование повышенной эхогенности с неровными, нечеткими контурами в просвете воротной вены (стрелки).
б) Режим ЦДК. Полное отсутствие допплеровских сигналов внутри просвета сосуда; допплеровский сигнал определяется в сети мелких коллатералей.
При ЦДК отмечается полное или частичное отсутствие допплеровских сигналов внутри просвета сосуда; в случае частичного тромбоза сигнал определяется пристеночно вокруг тромба, частично окклюзирующего вену, либо в сети узких коллатералей (рис. 1, б). В случае частичного тромбоза определяется допплеровский сигнал с признаками турбулентности на фоне повышенной скорости кровотока. При опухолевом тромбозе кровоток может быть пульсирующим либо непрерывным [2, 3]. Визуализируются мелкие или крупные коллатерали. При кавернозной трансформации воротной вены в режиме ЦДК в коллатералях определяется сглаженная допплеровская кривая со средней скоростью кровотока меньше 8 см/с [5]. Возможны кавернозные мальформации вены, спонтанные порто-портальные, порто-кавальные и спленоренальные шунты.
При компьютерной томографии (КТ) обнаруживается тромб как дефект наполнения в просвете воротной вены, не усиливающий сигнала.
При магнито-резонансной томографии (МРТ) в просвете воротной вены выявляются участки патологического сигнала, не отличающегося по интенсивности от окружающих тканей на Т1-взвешенных изображениях и имеющие повышенную интенсивность на Т2-взвешенных изображениях.
Ангиография является методом окончательного подтверждения диагноза. Из соображений безопасности чаще исследуется венозная фаза верхнебрыжеечной артериографии, реже выполняется спленопортография. В воротной вене выявляют дефект наполнения, либо она вообще не контрастируется.
В зависимости от локализации тромба различают три вида тромбоза воротной вены: радикулярная форма (тромбоз селезеночной вены и мезентериальных сосудов); терминальная форма (тромбозы мелких разветвлений и капилляров воротной вены в печени); стволовой тромбоз (в самом стволе воротной вены) [1-3].
Кроме того, тромбоз воротной вены бывает острым (после спленэктомии, при циррозе) и хроническим (развивается долго – от нескольких месяцев до нескольких лет) [1-3].
Стадии тромбоза
- Острая – эхогенный тромб. Воротная вена может быть увеличена.
- Подострая – визуализируются тромб и мелкие коллатерали. Воротная вена может быть увеличена.
- Хроническая – крупные коллатерали в проекции облитерированной воротной вены (кавернозная трансформация воротной вены). Воротная вена уменьшена или не визуализируется [1-3].
Приводим несколько клинических наблюдений пациентов с тромбозом воротной вены и ее ветвей.
Клиническое наблюдение 1
Пациент Ц., 39 лет. В анамнезе тупая травма живота с последующим развитием геморрагического панкреонекроза. Неоднократные оперативные вмешательства: дренирование сальниковой сумки. Предъявляет жалобы на боли в эпигастральной области.
УЗИ брюшной полости
Печень увеличена в размерах, контуры ее ровные, четкие, структура диффузно неоднородная, смешанной эхогенности, признаков билиарной гипертензии нет. Ствол воротной вены виден как образование неоднородной структуры с множеством эхогенных, параллельно идущих стенкам сосуда перегородок. Наличие гиперэхогенных участков в паравенозной области воротной вены (рис. 2, а). При ЦДК – выраженные коллатерали в проекции воротной вены (рис. 2, б). Желчный пузырь удален. Поджелудочная железа увеличена в размерах, головка – до 40 мм, контуры неровные, нечеткие, структура диффузно неоднородная, отмечается чередование участков повышенной и пониженной эхогенности, проток визуализируется на всем протяжении, на уровне тела поджелудочной железы он расширен до 10 мм. В проекции головки поджелудочной железы – выраженные околоподжелудочные коллатеральные анастомозы (рис. 3). Селезенка нормальных размеров, ее структура однородная, средней эхогенности. Селезеночная вена 7 мм, ход ее извит, деформирован, в проекции ворот селезенки имеются выраженные коллатерали (рис. 4). Заключение: гепатомегалия. Диффузные изменения печени. Картина хронического головчатого панкреатита. Тромбоз воротной вены с последующей реканализацией и кавернозной трансформацией воротной вены, развитием коллатеральных анастомозов.
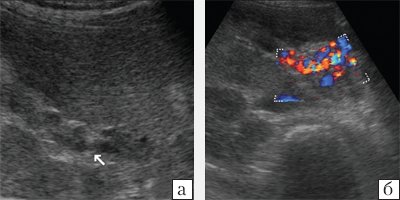
а) В-режим. Отсутствие типичного трубчатого анэхогенного ствола воротной вены с гиперэхогенными стенками. Ствол воротной вены виден как образование неоднородной структуры с множеством эхогенных, параллельно идущих стенкам сосуда перегородок (стрелка). Наличие гиперэхогенных участков в паравенозной области воротной вены.
б) режим ЦДК – выраженные крупные коллатерали в проекции воротной вены.
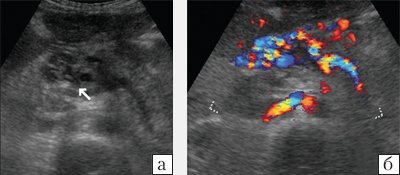
а) В-режим.
б) Режим ЦДК.
Тромбозы артерий и вен: симптомы, причины, лечение и профилактика

Тромбоз — опасное состояние, при котором в сосуде образуется кровяной сгусток. Такой тромб может расти, закупоривая сосуд вплоть до полного перекрытия последнего, но при определенных условиях может и «оторваться», становясь тромбоэмболом.
Лечение данной патологии всё ещё сложное, после него возможны рецидивы 1 . Поэтому важно знать причины тромбоза, чтобы, обнаружив их у себя, вовремя приступить к профилактике. Об этом, а также о проявлениях заболевания, мы и поговорим.
Причины образования тромбов
Сгустки крови в кровеносных сосудах возникают под воздействием комплекса факторов, которые смогли изменить:
- вязкость крови;
- скорость её движения;
- состояние стенки кровяных клеток, в особенности, тромбоцитов, что повлияло, в том числе, и на их электрический заряд.
К основным причинам возникновения тромбоза относятся:
A. Состояния, при которых свертывающая система крови становится чрезмерно активной, и её антагонист — белки и ферменты противосвёртывающей системы крови — не могут этому воспрепятствовать
Это могут быть наследственные или приобретённые заболевания, самые частые из которых:
- антифосфолипидный синдром;
- гемофилия;
- повышенный уровень в крови аминокислоты гомоцистеина;
- системная волчанка;
- снижение концентрации в крови протеинов C или S;
- недостаточность антитромбина;
- ДВС-синдром — острое состояние, которое развивается при многих тяжёлых заболеваниях (в том числе и инфекционных), после операций, при осложнениях беременности: преэклампсии и эклампсии, несовместимости матери и плода по группе крови и других.
Б. Травмы сосудов

Они происходят при постановке венозных катетеров (тогда наблюдаются симптомы венозного тромбоза верхних конечностей), операциях — в особенности, при установке протезов и консолидации переломов, хирургическом лечении органов таза.
В. Обеспечение условий для застоя крови
К этому приводят:
- длительное обездвиживание: при лечении переломов, а также других тяжёлых заболеваний;
- параличи;
- парезы;
- длительные переезды;
- авиаперелеты — в особенности, при наличии сопутствующих патологий, например, нарушений ритма или перенесенного инфаркта миокарда;
- наркоз, когда он длился более 60 минут и при нём использовались искусственная вентиляция и, соответственно, применялись препараты, расслабляющие мышцы.
Г. Отдельные заболевания
Ещё одними причинами развития тромбоза являются патологии, влияющие на свертываемость крови или ход сосудов. Это:
- опухоли: любые злокачественные, в том числе, лейкозы;
- острый инфаркт миокарда;
- воспаления толстой кишки;
- ожирение;
- инсульт;
- сердечная недостаточность;
- заболевания почек, при которых развивается нефротический синдром (отеки, потеря белков с мочой, повышение уровня холестерина);
- пароксизмальная гемоглобинурия;
- системные васкулиты, в том числе, сопровождающие заболевания суставов;
- перенесенные тромбоэмболии;
- снижение уровня тромбоцитов, связанное с необходимостью длительного употребления гепарина;
- атеросклероз сосудов.
Кроме того, довольно частой причиной тромбоза является беременность, особенно вторая её половина, а также послеродовый период. Это связано с повышением уровня прогестерона, повышающего вязкость крови. Увеличенная матка может сдавливать вены таза, в результате чего скорость кровотока в них снижается в 2–3 раза 1 . Тромбообразование может также начаться, когда в послеродовом периоде запускается физиологическое тромбирование вен того участка матки, который ранее сообщался с плацентой 1 .
Д. Прием препаратов
Повышают риск образования внутрисосудистых тромбов противозачаточные средства, гормональные препараты — в том числе, для лечения злокачественных новообразований, медикаменты для химиотерапии, в том числе, тамоксифен.
Отличие причин артериального и венозного тромбозов

В целом, выше перечислены причины развития тромбоза в венозном русле. Венозные сосуды отличаются тем, что в них слабо развита мышечная стенка, и движение крови в них происходит медленно. Это способствует застою и образованию тромбов.
В этом плане наиболее уязвимы сосуды системы нижней полой вены: кровь в них вынуждена подниматься против силы тяжести — только с помощью мышц голени, присасывающего давления лёгких и перикарда. Поэтому симптомы тромбоза нижних конечностей и вен таза — а именно они и входят в систему нижней полой вены — встречаются в 95% случаев венозного тромбоза (флеботромбоза) 2 .
Наиболее часто сгустки крови формируются в глубоких венах голени. Этому способствуют такие состояния, при которых отключается «второе сердце» организма — икроножные мускулы. Главное из них — это наркоз с применением миорелаксантов, препаратов для расслабления всех мышц, делающими многие полостные операции возможными. Миорелаксанты вызывают гораздо более глубокую мышечную релаксацию, чем это возможно во сне или даже при параличе мускулов. Именно поэтому перед операцией важно надевать компрессионное бельё: оно поддерживает «второе сердце» в искусственном тонусе.
Теперь о причинах тромбоза артерий. В артериальных сосудах крупного и среднего калибра скорость кровотока высокая 3 . Поэтому тромбы могут возникать:
- На атеросклеротических бляшках: данные отложения липидов возникают, в основном, в местах неравномерного кровотока, поэтому тромбу здесь удержаться легче.
- В артериях небольшого диаметра, где невысокая скорость кровотока.
- На стенках аневризмы — патологического расширения сосуда. Следовательно, при синдромах Марфана, Элерса-Данлоса, нейрофиброматозе, опухоли Эрдгейма и других патологиях, при которых аневризмы образуются очень часто — из-за нарушения строения сосудистых стенок.
- В области воспалённой или поражённой собственным иммунитетом стенки артерии.
- В месте, где артерия пережата: костью, опухолью, кистой.
- В месте, где стенка артерии (в основном, мелкого диаметра) состоит из «неправильных» белков, которые притягивают к себе тромбоциты, хотя должны их отталкивать ввиду разности электрических зарядов. Это происходит при коллагенозах.
- При генерализованном ДВС, когда свёртывающую систему крови уже практически не останавливает скорость кровотока.
Предрасполагающие к ангиотромбозу факторы

Не у всех, кто имеет вышеуказанные причины возникновения тромбоза, заболевание обязательно развивается. Зачастую нужны ещё внешние воздействия, которые запустят патологическое образование тромбов в сосудах.
Такими факторами становятся:
- Курение. В этом случае тромбоз, в основном, развивается в артериях — причем сосуды нижних конечностей от курения страдают в 2–3 раза чаще 4 , чем эта вредная привычка вызывает ишемию сердца. Причина — длительный спазм сосудов (vasa vasorum), мелких сосудов, питающих артерии и вены.
- Сахарный диабет. Данная патология приводит к нарушению свойств сосудистой стенки, в основном, артериальной. В результате, хоть диабет и не является непосредственной причиной развития тромбоза, но увеличивает риск его развития в 2–4 раза 1 . Кроме того, патология является и тем фактором, который будет ухудшать прогноз после хирургического лечения артериального тромбоза, поэтому, при его наличии, необходимо поддерживать глюкозу крови в пределах нормы.
- Нарушение жирового обмена. Каждое повышение концентрации общего холестерола на 10 мг/дл повышает риск облитерирующего атеросклероза, а с ним и тромбоза нижних конечностей, на 5–10% 1 .
- Воздействие местных факторов. При наличии причины развития тромбоза, его риск выше у тех людей, чьи конечности чаще травмируются (в счёт идут мелкие царапины и порезы), переохлаждаются или перегреваются.
- Стрессы. Психогенные стрессы приводят к выработке повышенного уровня кортизола, и он приводит к длительному спазму артерий с нарушением нормального кровотока по сосудам сосудов.
К факторам риска ангиотромбоза — венозного и артериального — относят также и те обстоятельства, которые нельзя изменить, но можно учесть, вовремя начав профилактику. Это:
- Возраст: чем человек старше, тем больше внимания он должен обращать на своё здоровье, в том числе и на состояние нижних конечностей. Описываемые ниже симптомы тромбоза не являются нормой ни в каком возрасте.
- Мужской пол: при этом увеличивается риск образования сгустков и в венах, и в артериях.
Как проявляется ангиотромбоз

В целом, симптомы тромбоза зависят от трёх факторов:
- где образовался сгусток крови — в артерии или в вене;
- в каком сосуде, и на каком его уровне появился тромб;
- перекрыл ли сгусток сосуд, насколько быстро это произошло.
Проявлениями флеботромбоза являются отёк и боль в конечности, усиливающаяся при ходьбе. При этом отёчная кожа становится синюшной, этот цвет становится более ярким в положении стоя. Пораженная конечность более тёплая, чем здоровая. Под отёчной кожей можно прощупать болезненный тяж — это пораженная вена. Активное прощупывание или сдавливание конечности опасно развитием ТЭЛА.
Уровень отёка зависит от места, где находится тромб: чем он ниже, тем меньшая поверхность ноги или руки будет отекать. В некоторых случаях болезнь протекает скрыто. Тогда тромбоз нижних конечностей выявляется после симптомов ТЭЛА: резкого чувства нехватки воздуха, одышки, обморока, сильного сердцебиения и кашля.
При артериальном тромбозе симптоматика отличается. Пока тромб растет и перекрывает артерию на 25% или меньше, в конечности будут появляться:
- онемение;
- покалывание;
- зябкость, которая накатывает «приливами» и локализуется ближе к пальцам;
- тяжесть в ногах — при нагрузке.
С увеличением тромба наблюдаются более заметные симптомы тромбоза: конечности начинают быстрее уставать, становятся более чувствительными к холоду, а «мурашки» и онемение возникают чаще и длятся дольше. Одна конечность становится более бледной, сухой и холодной, чем вторая. На ней часто возникают гнойнички и воспаления, которые долго не заживают.
При прогрессировании заболевания в пораженной ноге или руке возникает боль, при тромбозе артерий нижней конечности появляется хромота. А в далеко зашедшей стадии, если не развивается острый тромбоз, возникают трофические язвы — сначала как поверхностные раны, которые не заживают, а потом как глубокие «рытвины» с неровными краями. Финальными симптомами тромбоза, который развивается постепенно, становится развитие влажной гангрены, появление признаков общей интоксикации: тошноты, слабости, потери аппетита, головных болей. Вместе с этим зачастую также повышается температура тела. Если поражённую часть конечности не ампутировать, нарушается работа почек, сердечной и дыхательной системы.
Если же тромб в артерии растет быстро, появляются симптомы тромбоза конечности острого характера:
- кожный отёк;
- сильнейшая боль в ноге или руке;
- болезненность при прикосновении к конечности;
- быстрое развитие гангрены.
Изменения наблюдаются ниже перекрытой тромбом артерии. На ней же и пропадает пульс, что отмечается в самом начале заболевания.

Независимо от причины возникновения тромбоза, основными его осложнениями являются тромбоэмболические. Этот термин обозначает отрыв тромба от стенки сосуда и закупорка им подходящей по диаметру артерии, в результате чего участок органа, питавшегося от этой артерии, не получает питания и отмирает.
Наиболее часто тромбоэмбол попадает в артерии, отходящие от дуги аорты (это, в том числе, и питающие мозг артерии), на втором месте стоят крупные артерии таза и нижних конечностей, затем — артерии, идущие к внутренним органам. Очень редко развивается тромбоэмболия верхнеконечностных артерий 1 .
Одним из распространенных осложнений самого частого тромбоза — тромбоза глубоких вен нижних конечностей — является ТЭЛА (тромбоэмболия легочной артерии), когда перестает кровоснабжаться больший или меньший участок лёгких. Развивается ТЭЛА не в каждом случае флеботромбоза, но, к сожалению, выявить факторы риска этого опасного заболевания так и не смогли. Считается, что наибольшая опасность ТЭЛА существует в ранние сроки после возникновения симптомов тромбоза конечностей — пока тромб ещё неплотно фиксирован к стенке вены, и может оторваться. Тем не менее, тромбоэмболия может возникнуть и через длительный промежуток времени после флеботромбоза, особенно если не предпринимать никаких профилактических мер.
Кроме тромбоэмболии, флеботромбоз может осложниться ростом тромба и его распространением на близлежащие вены. Например, из глубоких вен голени сгусток может «дорасти» до подколенной вены, а из поверхностой бедренной — до общей бедренной вены. В этом случае ухудшается отток крови от конечности, а также увеличивается риск отрыва тромба.
Терапия должна быть начата как можно раньше. При острых тромбозах — как венозном, так и артериальном — она заключается во введении тех препаратов, которые могут растворить тромб. Если медикаментозный тромболизис оказался неэффективен, выполняется операция по удалению тромба из сосуда. После этого продолжается антикоагулянтная терапия под контролем показателей свёртывания.
Лечение зачастую выполняется в отделении реанимации, под контролем сосудистого хирурга.
При симптомах тромбоза верхних конечностей или ног, имеющих хронический характер, лечение также назначается сосудистым хирургом. На начальных стадиях оно консервативное, заключается в назначении сосудорасширяющих препаратов, ангиопротекторов, витаминов группы B, средств, снижающих холестерин; при флеботромбозе — венотоников.
Обязательным является назначение лекарственных средств, разжижающих кровь. Тромбо АСС — препарат ацетилсалициловой кислоты, который блокирует оседание тромбоцитов на стенках сосудов, в том числе и поражённого, тем самым, не давая тромбу разрастаться. Таблетки Тромбо АСС покрыты кишечнорастворимой плёночной оболочкой, что снижает вероятность развития местного раздражающего действия на желудок.
При далеко зашедших хронических тромбозах необходимо восстановить проходимость сосуда. Решение по оперативному лечению для восстановления проходимости сосуда принимает врач. Независимо от причины тромбоза после операции назначается прием антикоагулянтов и/или антиагригантных препаратов на длительный период.

Она заключается в улучшении кровотока в конечностях. Для этого нужно:
- поддерживать артериальное давление, холестерин и глюкозу крови в пределах нормы;
- проходить профилактические осмотры, вовремя реагировать на патологические изменения в сердце и сосудах;
- больше ходить пешком;
- избегать длительного стояния на ногах;
- сократить употребление соли;
- обогатить рацион продуктами, богатыми клетчаткой, а также полиненасыщенными жирными кислотами, витаминами E и P;
- беречь конечности от травм, переохлаждения и перегревания.
Если имеется один или несколько факторов его риска, необходимо получить рекомендации врача по профилактическому приёму Тромбо АСС. Препарат адаптирован для длительного приёма. Ацетилсалициловая кислота в кардиологических дозировках на протяжении многих лет активно используется специалистами для профилактики тромбозов и их тромбоэмболических осложнений.
* Имеются противопоказания, перед применением необходимо проконсультироваться со специалистом 1 Затевахин И.И. Тактика лечения при острых тромбозах артерий нижних конечностей // Материалы четвертого международного хирургического конгресса «Научные исследования в реализации программы Здоровье населения России» — М., 2012. 2 Артериальные тромбозы и эмболии конечностей / Под. ред. В.И. Лупальцова, С.С. Мирошниченко, И.А. Дехтярук / Харьков, ХНМУ, 2010 г. 3 Министерство здравоохранения Российской федерации. Клинические рекомендации. Заболевания артерий нижних конечностей. 2016 год (пересмотр каждые 3 года). 4 А. К. Лебедев, О. Ю. Кузнецова. Тромбоз глубоких вен нижних конечностей. Клинические рекомендации. / М, 2015.
Тромбоз: причины, симптомы, диагностика, лечение
Тромбоз – полная или частичная закупорка просвета сосуда пристеночным или подвижным тромбом. Тромб – это плотный сгусток крови, появляющийся вследствие изменения ее текучести. В норме тромбообразование – защитный механизм. Повреждение сосудистой стенки влечет замедление кровотока, накапливание тромбоцитов вокруг повреждения. Тромб буквально «штопает» стенку сосуда.
Классические причины тромбообразования описываются триадой Вихрова: повреждение сосудистой стенки, замедление кровотока и изменение свойств крови [3]. Некоторые тромбы (их называют эмболами) способны передвигаться до более узких участков сосуда, которые и закупоривает полностью или частично. Ежегодно около 25 млн человек погибают от тромбозов, еще больше сталкиваются с нарушениями трофики, вызванными тромбами [3].
Типы сосудистых тромбозов
Наиболее распространены тромбозы нижних конечностей, однако наибольшую опасность представляют собой тромбоэмболия легочной артерии – ТЭЛА – и синдром диссеминированной внутрисосудистой свертываемости – ДВС-синдром.
Тромбоз артерий развивается при закупорке ее просвета тромбом или эмболом. Клинические признаки определяются местом, где произошла такая закупорка, органом или тканью, плохо снабжающемуся кровью или не снабжающемуся ею вовсе. Если закупорка с нарушением проходимости сосуда происходит медленно, открываются «запасные», коллатеральные, сосуды, что смягчает клинические симптомы артериального тромбоза [3]. Тромбозы артерий чаще возникают у мужчин среднего и пожилого возрастов [7].
Тромбоз вен различается в зависимости от локализации поражения на тромбоз глубоких или поверхностных вен и тромбоэмболию легочной артерии. Среди всех сердечно-сосудистых патологий венозные тромбозы по частоте встречаемости занимают третье место, уступая лишь ИБС и атеросклерозам. Третье место в структуре причин смертности занимает ТЭЛА. Начиная с 40 лет, риск развития венозных тромбозов увеличивается вдвое каждые 10 лет [5].
Описывают два варианта поражения вен нижних конечностей: флеботромбоз (первичный тромбоз, тромб непрочно фиксирован) и тромбофлебит (вторичный тромбоз на фоне воспаления стенки сосуда, тромб фиксирован прочно) [6]. Тромбофлебиты чаще ассоциируются с тромбозом вен поверхностных [2]. Чем более крупная вена пострадала от тромбоза, тем ярче его клинические проявления. Окружающие ткани сдавливаются застоем крови, так как к месту окклюзии кровь пребывает, а по направлению к сердцу не движется. Венозные тромбы склонны отрываться и разноситься с током крови (тромбоэмболы). При их попадании в жизненно важные органы развиваются жизнеугрожающие состояния [3].
Причины тромбоза
Факторы риска образования тромбозов
Клиника тромбоза
Симптомы тромбоза могут быть общими независимо от локализации или специфичными. Общие симптомы включают боль при движении и в покое, ограничение подвижности и снижение функционирования пострадавшего органа или ткани.
Симптомы нарушения артериальной проходимости (острого тромбоза, или постепенного нарушения проходимости сосуда):
- асимметрия АД при измерении на обеих руках [7];
- бледность кожи, переходящая в синюшность [7];
- боль в покое по ночам [7];
- боль при движении в бедре, ягодице, голени, стопе, стреляющая или ноющая [7];
- нарушения сна [7];
- онемение, похолодание конечности [7];
- отсутствие периферической пульсации [7];
- омертвение (некроз) пострадавших тканей, трофические язвы, гангрена [7];
- перемежающаяся хромота [7].
Симптомы венозного тромбоза:
- боль [6];
- отеки, мягкие и асимметричные [6];
- посинение кожных покровов (цианоз кожи) [6];
- повышение температуры кожи конечностей [6];
- повышенная чувствительность и уплотнение в проекции поверхностных вен [2];
- поствоспалительная гиперпигментация [2];
- расширенные подкожные вены [6];
- эритема [2].
Иногда единственным симптомом венозного тромбоза является ТЭЛА [6].
Диагностика тромбоза
Первичная диагностика основана на подробном анамнезе и антропометрии (окружность голени или бедра). Используются шкалы Уэллса для диагностики острого тромбоза и диагностики ТЭЛА [8,9].
Инструментальная диагностика включает компрессионное или дуплексное сканирование вен, допплерографию с компрессией вен, импедансную плетизмографию, пульмоноангиографию, рентгеноконтрастную или МРТ-флебографию [6,9], КТ и МРТ-ангиографию [7,9].
Для диагностики артериальных тромбозов применяют физические тесты (тест 6-минутной ходьбы, тредмил тест), определение пульсации поверхностно расположенных артерий (артерии тыла стопы), дуплексное сканирование артерий конечностей, ангиографию (рентгеновский снимок сосуда, заполненного рентгенконтрастным веществом) и измерение транскутанного напряжения кислорода [7].
Анализы при тромбозе
Значительную роль в своевременной диагностике тромбозов играют лабораторные показатели. Так, методические рекомендации по ведению пациентов с новой коронавирусной инфекцией предусматривают стратификацию риска коагулопатии у пациентов с СOVID-19 на основе простых лабораторных тестов: D-димер, протромбиновое время, количество тромбоцитов, уровень фибриногена [1,9].
Клинический анализ крови позволяет выявить воспаление. Он же определяет уровень тромбоцитов, то есть самого субстрата тромбоза.
Дополнительно об уровне воспаления в крови и риске тромбоза свидетельствует повышенный уровень С-реактивного белка.
Биохимический анализ в первую очередь демонстрирует уровень глюкозы крови. По ней можно судить о наличии диабета, одного из серьезнейших факторов риска тромбозов.
Также биохимический анализ способен определить уровень протеина С, что также характеризует выраженность риска тромбоза.
Повышенный уровень гомоцистеина в крови также является доказанным на сегодняшний день риском тромбозов, приводящим к невынашиванию беременности и сердечно-сосудистым событиям (инфарктам и инсультам).
D-димер – лабораторный маркер фибринообразования [8]. Он же говорит о наличии воспаления, как и С-реактивный протеин. Уровень D-димера является контрольным показателем COVID-19 и его осложнений, в том числе связанных с тромбозами.
Можно сдать анализы по комплексной программе «Тромбоз», включающей определение уровней Антитромбин-III, D-димера и генетических факторов кардиологических заболеваний и уровень тромбоцитов. Эта программа позволяет определить факт свершившегося тромбоза где-то в организме, а также определить генетическую предрасположенность к нему. Такую программу, как и прочие анализы, предлагает сеть клиник СИТИЛАБ.
Дополнительное определение уровня гомоцистеина, С-реактивного белка поможет определить биохимический риск тромбоза.
Лечение и профилактика тромбозов
Лечение тромбоза включает антикоагулянтную и антиагрегантную, тромболитическую терапию, установку кава-фильтра нижней полой вены, хирургическое удаление тромба [5]. Необходимо иметь в виду осложнения антикоагулянтной терапии: большое кровотечение, гепарин-индуцируемую тромбоцитопению и варфарин-индуцируемый некроз кожи [5]. Для снижения риска продолжения тромбообразования применяют НПВС [2]. С целью вторичной профилактики назначают небольшие дозы гепарина.
Также назначают немедикаментозные методы лечения – эластичное бинтование, компрессионный трикотаж, локальную гипотермию и ЛФК [2, 4].
Профилактика тромбоза включает ряд мероприятий, применяемых в ситуациях повышенного риска тромбообразования.
Первичная профилактика атеротромбоза:
- систематические физические нагрузки в виде ходьбы или утренней гимнастики;
- контроль АД, поддержание рабочего артериального давления ниже 140/90 мм ртутного столба;
- контроль уровня сахара крови (менее 6 Ммоль/л), раннее выявление и лечение сахарного диабета;
- снижение веса, индекс массы тела менее 25 кг на м2;
- диета с ограниченным содержанием холестерина и жиров высокой плотности (общий холестерин менее 5 Ммоль/л), фрукты и овощи;
- отказ от курения [3,7].
Первичная профилактика тромбоза вен:
- компрессионное белье;
- бинтование эластичными бинтами;
- обильное питье, особенно после операции;
- регулярные физические упражнения, ходьба, особенно при путешествиях;
- запрет приема алкоголя и снотворного в большой дозе;
- запрет использования сдавливающей обуви и одежды [2,5,6].
Иногда, на периоды особого риска, назначают антикоагулянты за несколько дней до перелета. Аспирин принимать в таких случаях не имеет смысла [5].
Визуализация тромбоза портальной вены
Авторы: Ali Nawaz Khan, Kyung J Cho
Практические основы
Тромбоз воротной вены (ТВВ) все чаще распознается с помощью УЗИ. Снижение портального кровотока, вызванное заболеванием паренхимы печени и сепсисом в брюшной полости (т. е. инфекционным или восходящим тромбофлебитом), являются основными причинами.
ТВВ является частым осложнением цирроза печени, и его распространенность увеличивается с тяжестью заболевания печени: от 1% у пациентов с компенсированным циррозом печени до 8-25% у кандидатов на трансплантацию печени.
Правильный диагноз и характеристика ТВВ важны для прогноза и дальнейшего лечения. Тромбоз воротной вены является плохим прогностическим показателем, который обнаруживается при диагностике у 10-40% пациентов с гепатоцеллюлярной карциномой (ГЦК). Выживаемость составляет примерно 2-4 месяца.
CEUS позволяет детально визуализировать микроциркуляторное русло печеночной системы, очаговые поражения печени и тромбоз воротной вены. Злокачественные тромбы имеют тот же паттерн усиления, что и опухоль, из которой они возникли, включая быстрое повышение артериальной фазы и медленное или слабое вымывание в воротной вене.
Предпочитаемые методы исследования
Предпочтительные исследования включают дуплексную допплерографию и / или цветную допплерографию, компьютерную томографию, магнитно-резонансную ангиографию и артериальную портографию или спленопортографию.
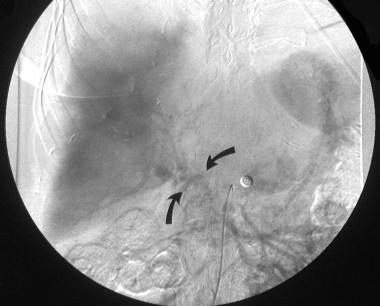
Рисунок 1 : Тромбоз воротной вены.Верхняя брыжеечная ангиограмма показывает коллатеральные сосуды на воротной части печени, но нет открытой воротной вены. Обратите внимание, что в результате асцита печень смещается от грудной клетки. У этого пациента была тяжелая печеночная недостаточность, и он умер через 72 часа после визуального исследования. Посмертное исследование показало ранний цирроз, молниеносный пиогенный холангит, множественные абсцессы печени, тромбоз воротной вены и селезенки и левой желудочной вены.
Опухоль в воротной вене может иметь вид, идентичный тромбозу, но этот вид встречается гораздо реже, чем у других. Тромб может быть частичным или полным. Он также может быть смешан с мягким тромбом.
Взрослые, у которых острый ТВВ вторичен по отношению к абдоминальному сепсису, могут полностью восстановиться, и сосуд может быть повторно проанализирован с успешным лечением основного сепсиса.
Невизуализация воротной вены убедительно свидетельствует об окклюзии. В этом случае воротную вену можно рассматривать как полосу эхо-сигналов высокого уровня у воротной части печени.
Развитие ТВВ может ускорить необходимость экстренной эндоскопии для склеротерапии варикозных вен, TIPS, хирургического создания портокавального шунта, трансъюгулярного или трансгепатического портомезентериального тромболизиса и тромбэктомии или даже резекции. Однако ТВВ может осложнить склеротерапию. Тонкоигольная аспирационная биопсия ТВВ может быть выполнена под цветным доплеровским сонографическим контролем для оценки терапевтической эффективности.
Ранние осложнения трансъюгулярного внутрипеченочного портосистемного шунта (TIPS), которые можно обнаружить с помощью ультрасонографии, включают следующее:
- внутрибрюшинное кровоизлияние,
- тромбоз шунта,
- гематома шеи,
- нарушение кровоснабжения печени,
- ТВВ,
- окклюзия печеночной артерии,
- инфаркт печени,
- неудачное развертывание стента,
- неадекватное расширение стента,
- расширение стента,
- обструкция желчных путей.
Исследователи, рассматривающие результаты пациентов с циррозом печени, перенесшим TIPS, отметили, что, хотя достигается увеличение скорости кровотока в воротной вене и снижение портальной гипертензии, состояние гиперкоагуляции сохраняется и может вызвать расширение остаточного ТВВ или ретромбоз.
ТВВ также может прерывать перфузию печени, вызывая ишемию гепатоцитов и гормональную депривацию, что может привести к гибели гепатоцитов, исчезновению паренхимы и, в конечном итоге, к ухудшению фиброза и функции печени, что приводит к увеличению смертности.
Компьютерная томография
Воротная вена обеспечивает 75% кровотока в печени. Следовательно, пиковое усиление контрастности печени происходит во время портальной венозной фазы, примерно через 60 секунд после начала болюсной инъекции контрастного вещества. При спиральной КТ исследование печени занимает около 20 секунд; изображения обычно могут быть получены в одном дыхании.
Эта методика может быть расширена для получения двухфазной компьютерной томографии с контрастным усилением, при которой печень визуализируется дважды одним болюсным средством контрастного вещества, сначала во время артериальной фазы, а затем через портальную венозную фазу.
Двухфазная КТ показана в некоторых случаях, связанных с доброкачественными или злокачественными поражениями, при которых характеристики сосудов указывают на правильный диагноз.
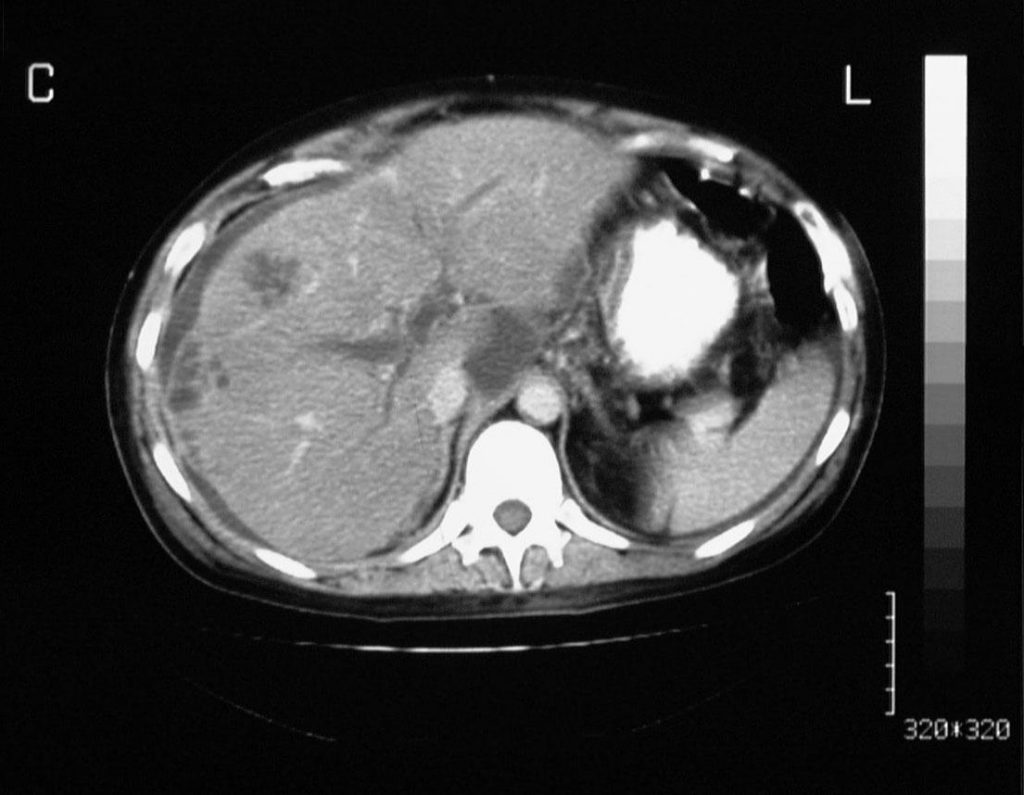
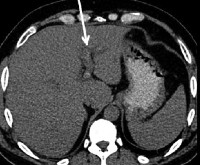
Рисунок 2 : Тромбоз воротной вены. Портальная венозно-фазовая усиленная осевая компьютерная томография не показывает кровоток в воротной вене. Обратите внимание на множественные мелкоєховые образования на периферии правой доли печени.
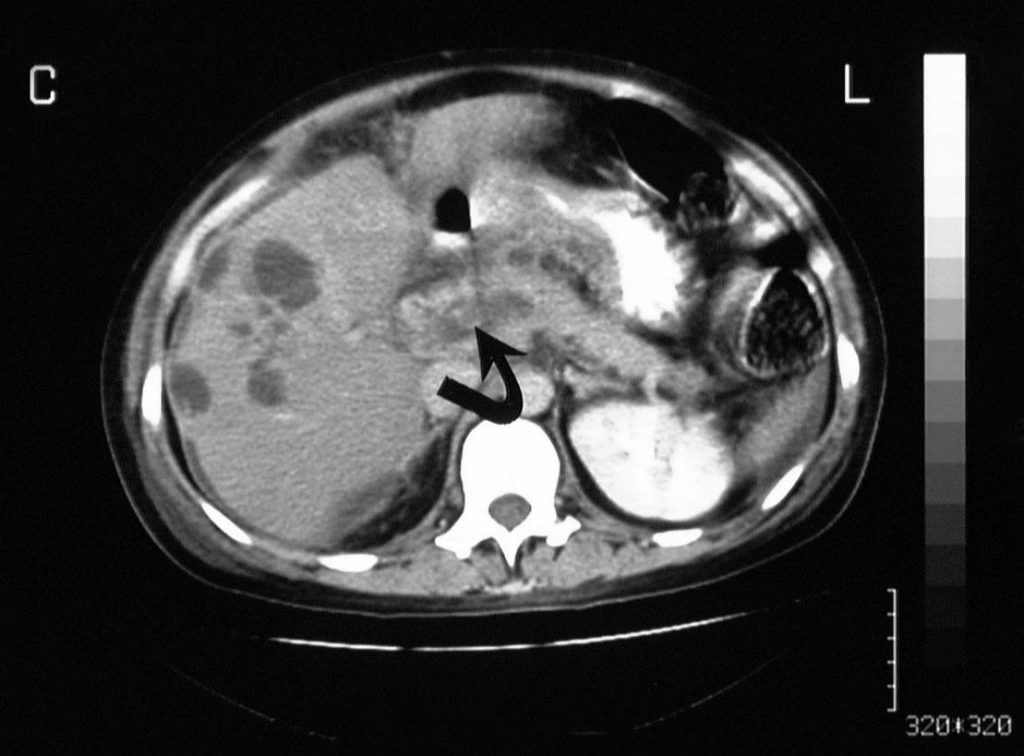
Рисунок 3 : Тромбоз воротной вены. Портальная венозно-фазовая усиленная аксиальная компьютерная томография, полученная у того же пациента, что и на предыдущем изображении, показывает образование в конце селезеночной вены (стрелка). Обратите внимание на множественные мелкоєховые образования на периферии правой доли печени.
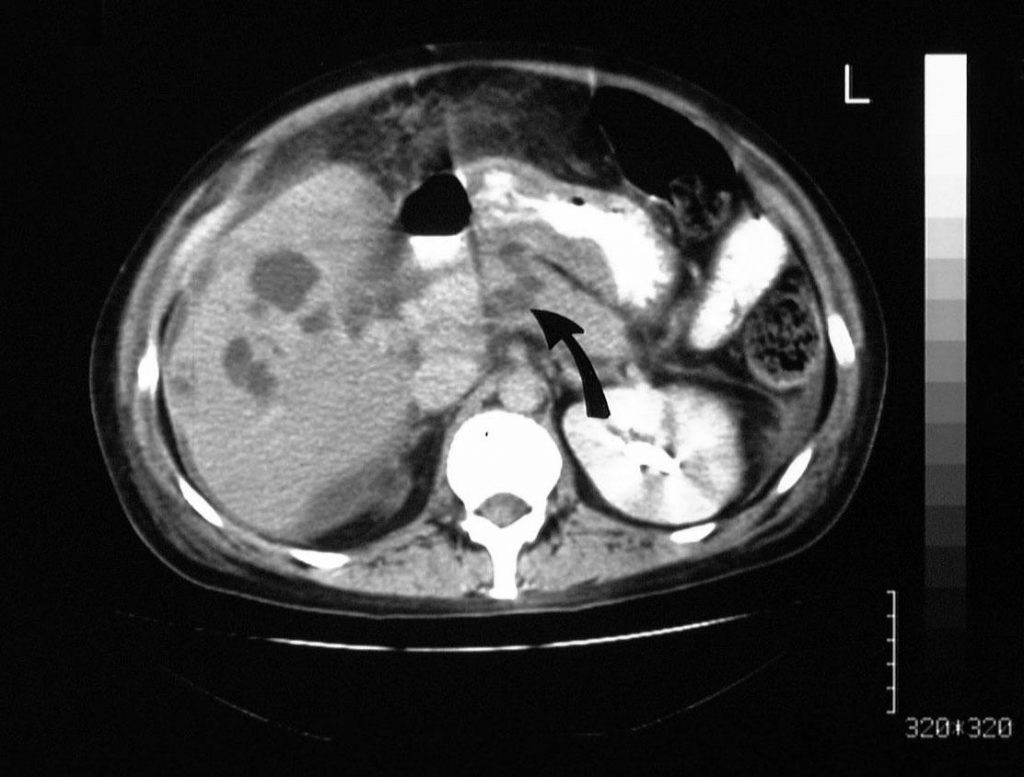
Рисунок 4 : Тромбоз воротной вены. Портальная венозная фаза, усиленная осевая КТ, полученная у того же пациента, что и на предыдущих 2 изображениях, показывает увеличенную левую желудочную вену. Никакого усиления контраста в вене не наблюдается; это открытие наводит на мысль о тромбозе (стрелка).
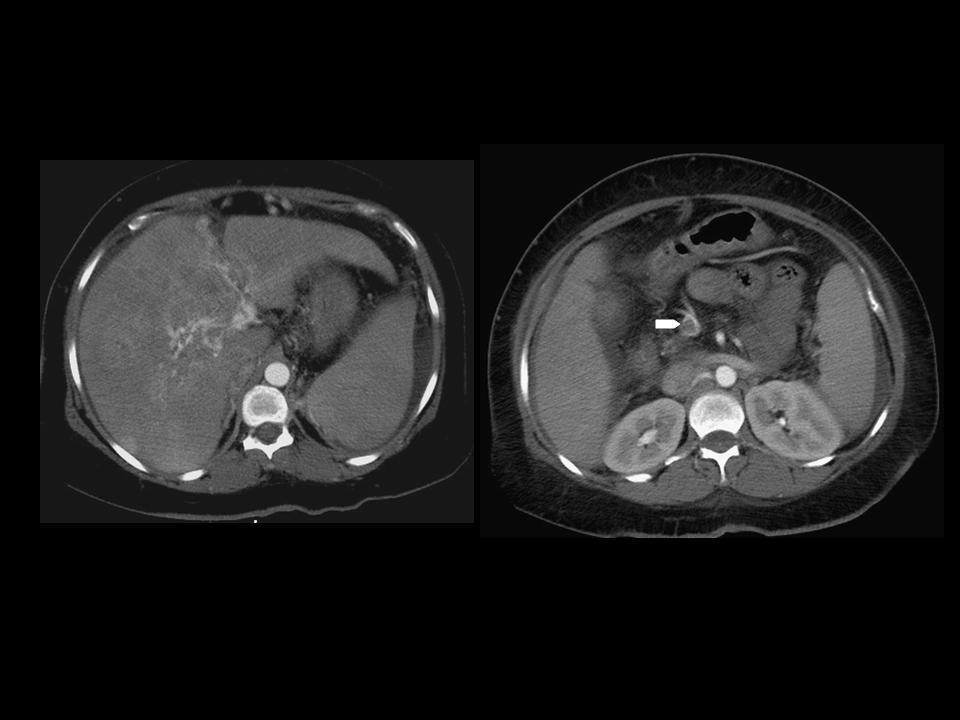
Рисунок 5 : Осевая КТ с контрастом изображает кавернозную трансформацию после портального венозного тромбоза.
КТ с помощью ангиографии или КТ-артериальная портография могут обеспечить лучшее разграничение портальной венозной системы и портального венозного усиления печени.
Ангиографический катетер помещают в общую брюшную ось, печеночную артерию или верхнюю брыжеечную артерию с использованием модифицированной техники Сельдингера через бедренную артерию. Получение изображения начинается через 3-5 секунд после начала введения контрастного вещества.
Исследование должно быть завершено как можно скорее, прежде чем контрастный материал рециркулирует. Для предотвращения значительных артефактов, связанных с плотностью контрастного вещества, используют 70 мл разбавленного (1-30%) йодированного контрастного вещества со скоростью инфузии 2 мл / с.
На КТ с усилением контраста ТВВ может быть изображен как слабо визуализируемый центр в воротной вене, окруженный периферическим усилением. Затухание воротной вены на 20-30 HU меньше, чем у аорты.
Магнитно-резонансная томография
Фазово-контрастная кинематографическая МРА может показать направление воротного венозного кровотока и наличие тромба портальной вены.
Магнитно-резонансная оценка портальной венозной системы точно демонстрирует тромбоз и коллатеральную циркуляцию.
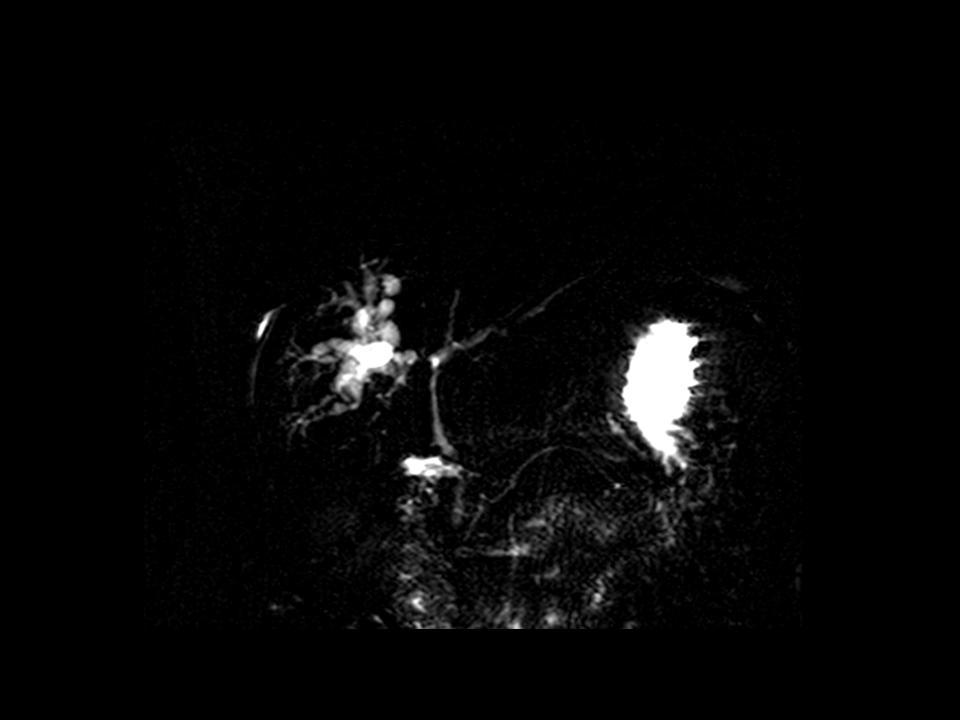
Рисунок 6 : МРТ показывает внутрипеченочную дилатацию желчных протоков правой доли и длинную стриктуру общего желчного протока.
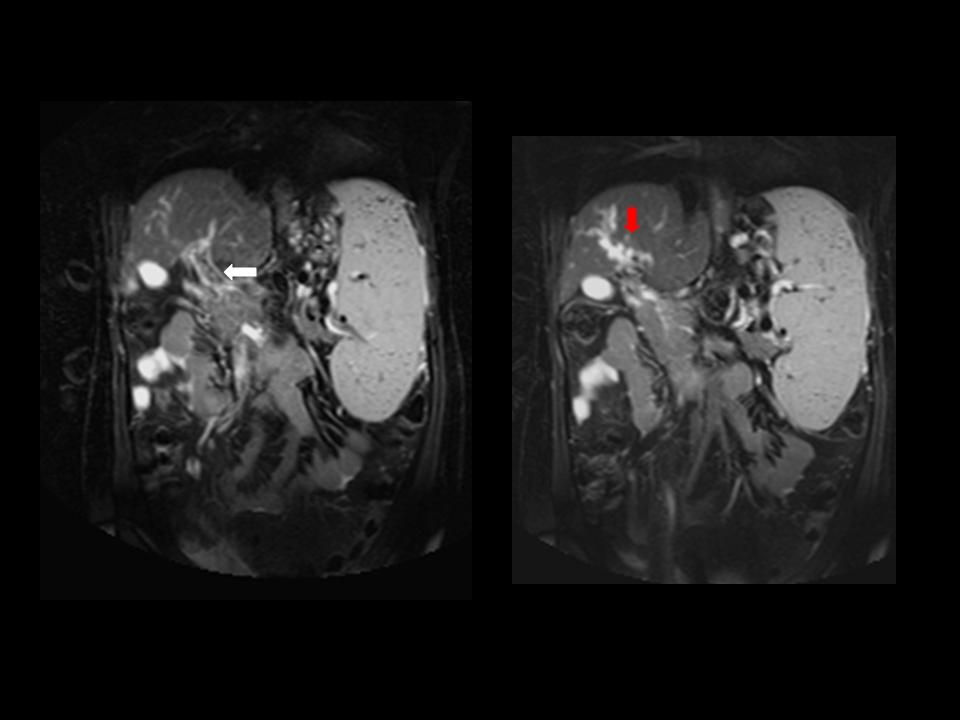
Рисунок 7 : МРТ с усилением контрастности, T1, показывающая тромб в воротной вене и кавернозную трансформацию воротной вены.
МРТ в сочетании с динамической трехмерной визуализацией может не только обнаруживать окклюзию портальной вены, кавернозную трансформацию и варикозное расширение желчного пузыря, но также отображать аномалии желчных протоков, связанные с портальной билиопатией.
Шах и коллеги сравнили МРТ с интраоперационными данными в диагностике тромбоза воротной вены у кандидатов на трансплантацию. В этом исследовании чувствительность и специфичность МРТ для выявления основного ТВВ составляли 100% и 98% соответственно. Причиной несоответствия между данными МРТ и трансплантации в 2 случаях был уменьшенный калибр воротной вены, который был интерпретирован как реканализированный хронический тромбоз при МРТ.
Ультразвуковое исследование
Тромбоз воротной вены (ТВВ) все чаще распознается с помощью УЗИ. Абдоминальный сепсис и снижение портального кровотока в результате паренхиматозной болезни печени являются основными причинами.
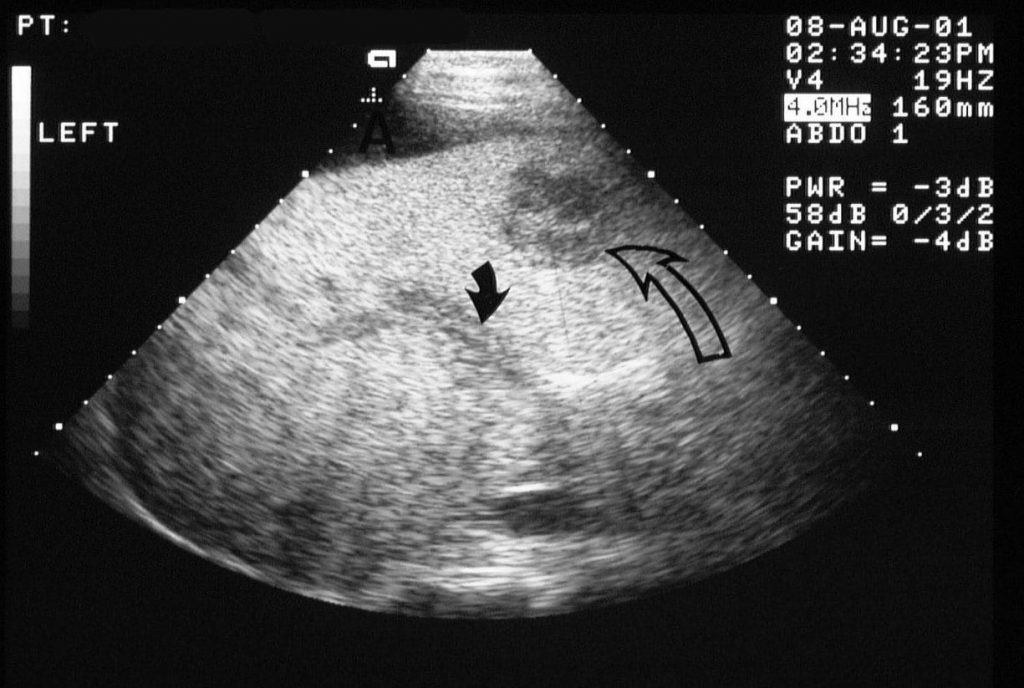
Рисунок 8 : Тромбоз воротной вены. Продольная косая сонограмма у 36-летней женщины с историей атрофии зрительного нерва Лебера (наследственная зрительная нейроретинопатия) и злоупотреблением алкоголя, у которой были неспецифические жалобы на плохое самочувствие и неопределенные боли в животе. Изображение показывает асцит и яркую печень (ожирение). Воротная вена имеет линейную эхогенную структуру, проходящую по длине воротной вены (сплошная стрелка). В печени присутствует кистозное образование (открытая стрелка).
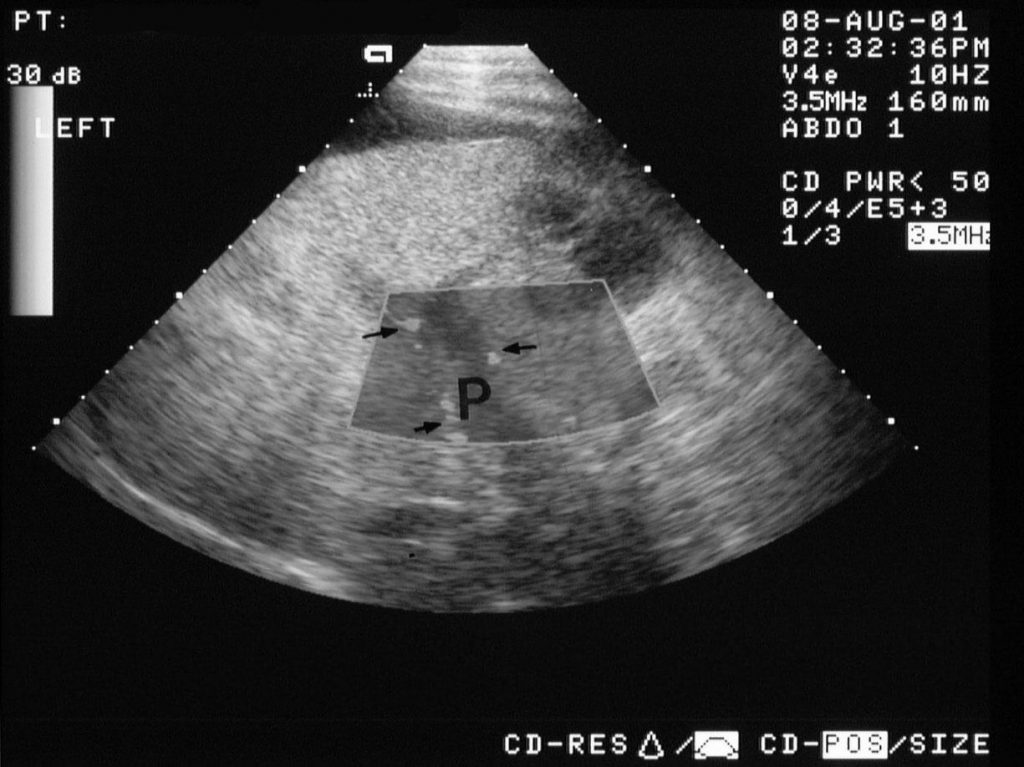
Рисунок 9 : Тромбоз воротной вены. Энергетическая допплерограмма печени показывает кровоток вокруг дефекта внутрипросветного наполнения в воротной вене (P).
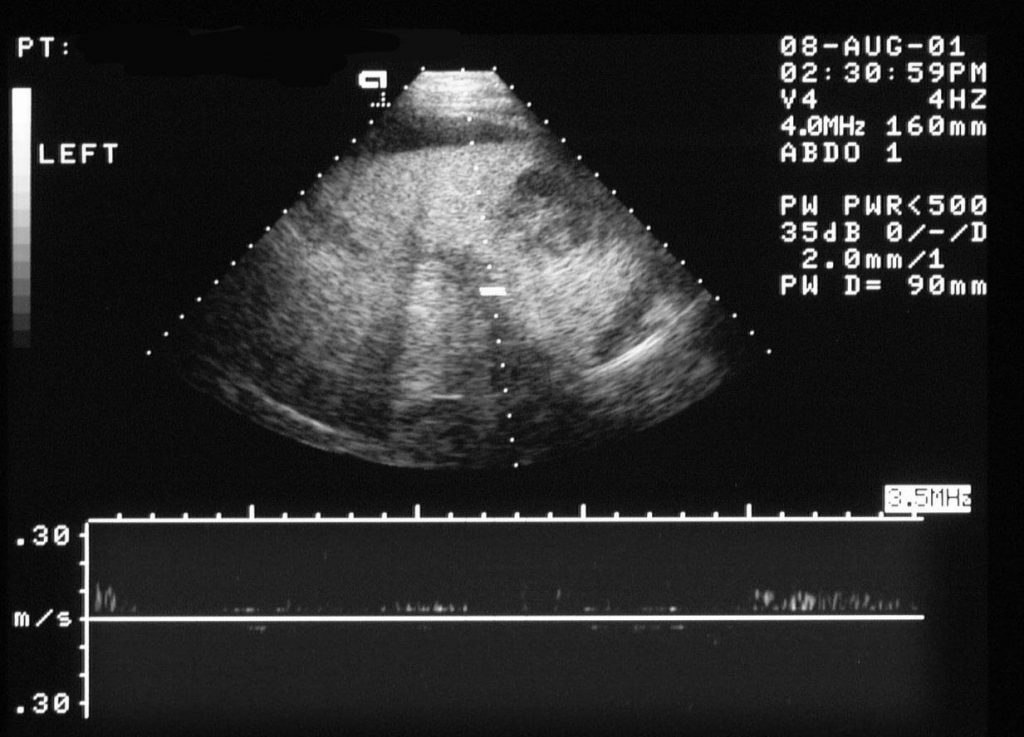
Рисунок 10 : Тромбоз воротной вены. Спектральная доплеровская сонограмма печени, полученная у того же пациента, что и на предыдущем изображении, показывает воротную вену (курсор), которая не демонстрирует кровоток.
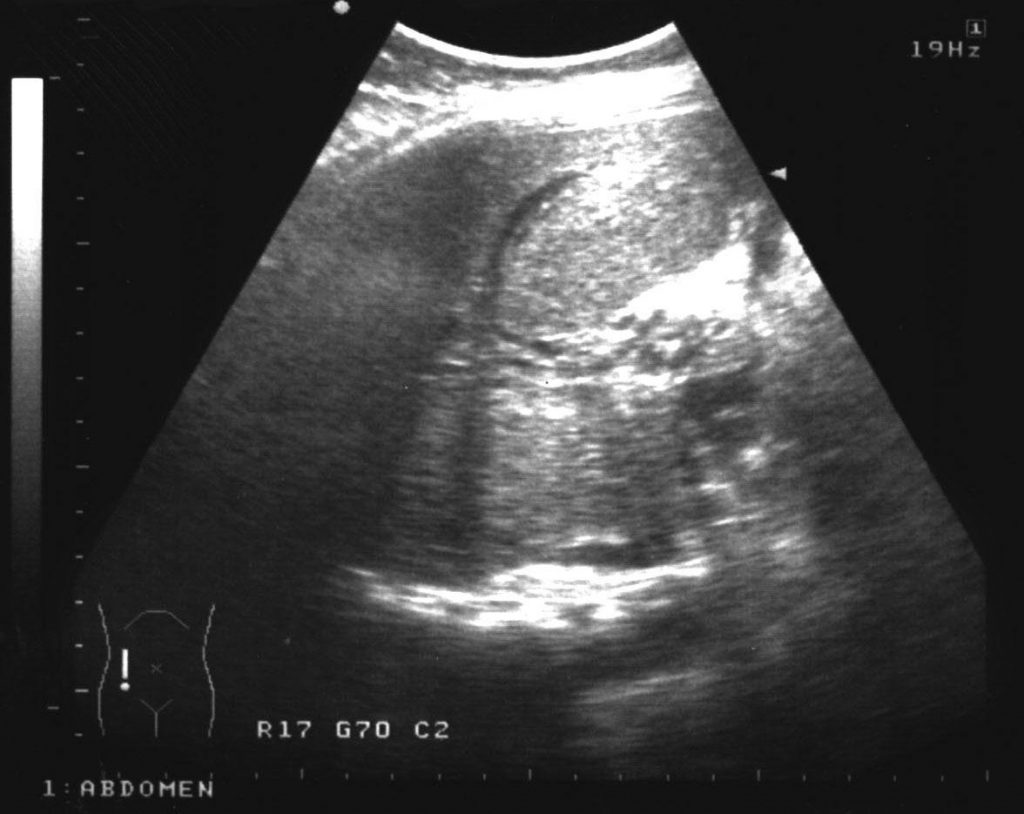
Рисунок 11 : Тромбоз воротной вены. Продольная косая сонограмма была получена у 28-летней женщины, которая была направлена на УЗИ желчного пузыря. Изображение показывает несколько сосудистых канальцевых структур у ворот печени, которые наводят на мысль о кавернозной трансформации.
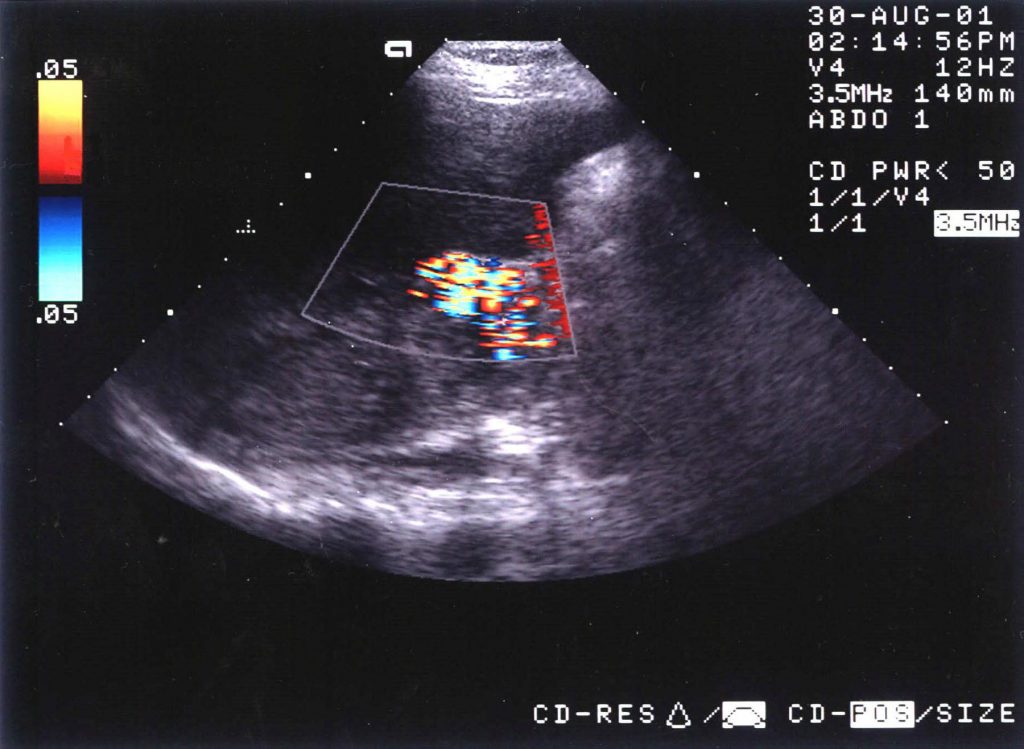
Рисунок 12 : Тромбоз воротной вены. Цветная допплеровская сонограмма, полученная у того же пациента, что и на предыдущем изображении, показывает кровоток в кавернозном образовании.
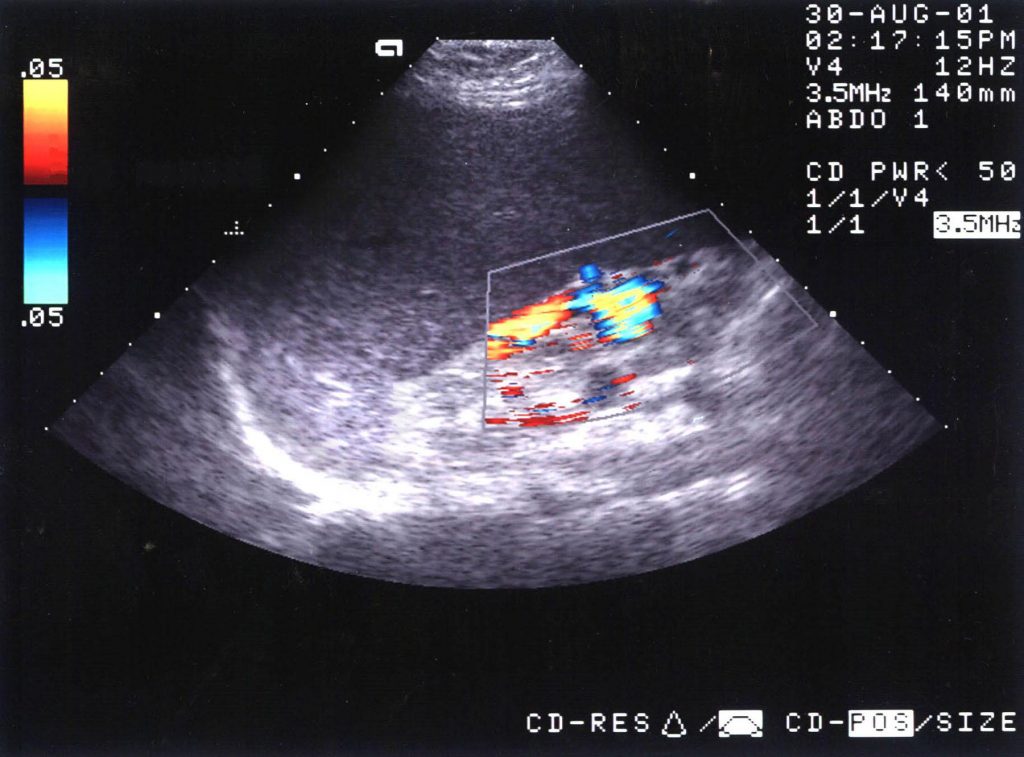
Рисунок 13 : Тромбоз воротной вены. Цветная допплерография селезенки, полученная у того же пациента, что и на предыдущих 2 изображениях, показывает умеренную спленомегалию с варикозным расширением вен в селезенке. Эндоскопические данные подтвердили наличие варикозного расширения вен пищевода.
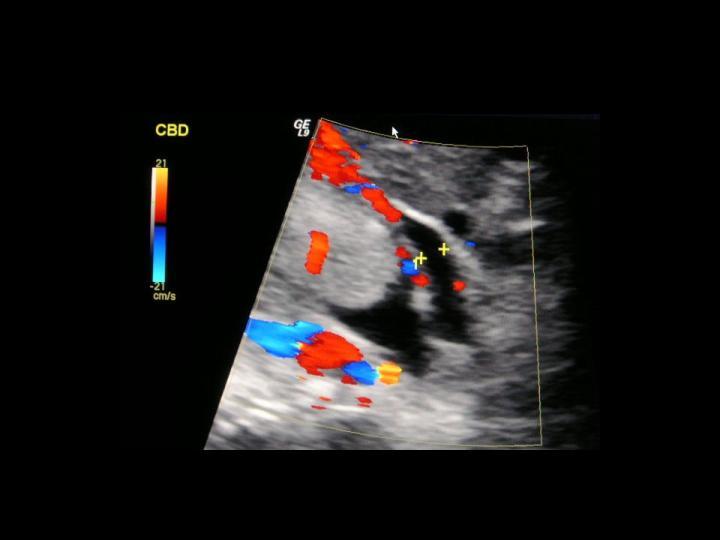
Рисунок 14 : Ультразвуковая цветная допплерография изображает васкуляризованный портальный тромб.
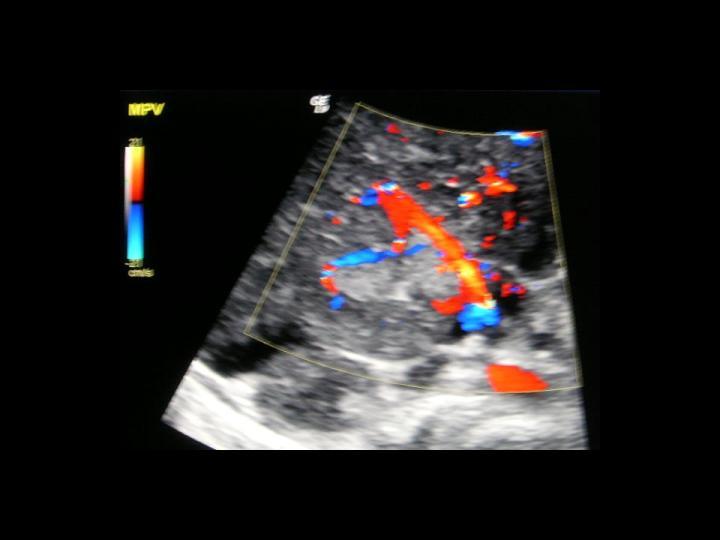
Рисунок 15 : Ультразвуковая цветная допплерография изображает васкуляризованный портальный тромб.
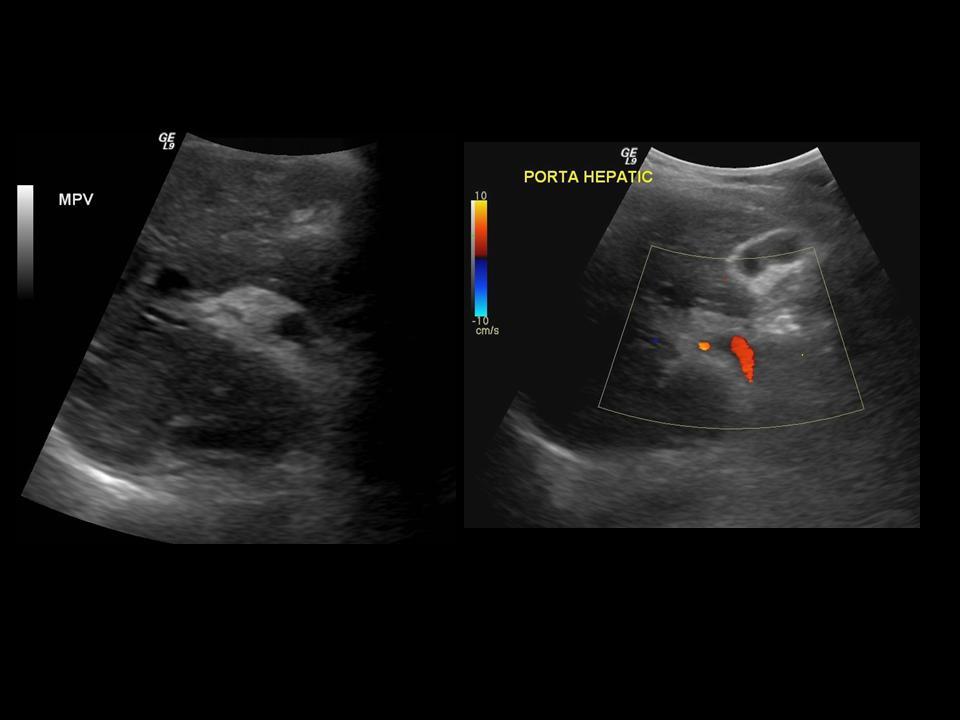
Рисунок 16 : Эхогенный частично реканализированный тромб воротной вены. Пациентка 36-летняя женщина с идиопатическим хроническим тромбозом воротной вены продолжительностью 2 года. У нее холестатическая желтуха.
На сонограммах в воротной вене могут присутствовать эхогенные поражения. Может быть изображен сгусток с переменной эхогенностью. Сгусток обычно имеет умеренную эхогенность, но если он образовался недавно, он может быть гипоэхогенным.
Открытые сосуды могут иметь повышенную внутрипросветную эхогенность из-за образования скопления эритроцитов, что делает медленную кровь слегка эхогенной. Повышенная или пониженная эхогенность может наблюдаться в просвете воротной вены.
ТВВ устраняет обычный сигнал венозного кровотока из просвета портальной вены во время импульсной или цветовой допплерографии. Цветовые доплеровские изображения потока могут показать обтекание тромба, который частично блокирует вену. Однако, если поток медленный, доплеровский сигнал может быть не обнаружен. Цветной поток может присутствовать в других небольших коллатеральных сосудах.
Может возникнуть неполная окклюзия. Это характерно для опухолевого поражения. Альтернативно, может произойти тромболитическая реканализаци. Также можно обнаружить кавернозные мальформации, спонтанные шунты, спленоренальные и портосистемные коллатерали. Может быть очевидной основная причина: гепатоцеллюлярная карцинома, метастазы, цирроз печени, новообразования поджелудочной железы.
Предполагается, что утолщение воротной вены с сужением ее просвета, вызвано портальным флебитом. Это считается предшественником ТВВ у пациентов с острым панкреатитом. Диаметр воротной вены больше 15 мм в 38% случаев ТВВ.
Ангиография
Среди катетер-ориентированных методов артериальная портография в настоящее время является предпочтительным методом оценки портальной венозной системы, поскольку она менее инвазивна и имеет более низкую частоту осложнений, чем другие методы.
ПРАВИЛЬНО ЛИ ВЫ УХАЖИВАЕТЕ ЗА УЗ-АППАРАТОМ?
Скачайте руководство по уходу прямо сейчас

3 основных показания для артериальной портографии следующие:
- обследовать пациентов с портальной гипертензией и ее последствиями, особенно когда планируется хирургическое лечение;
- определить резектабельность опухолей печени и поджелудочной железы, когда ангиографические данные артериальной и венозной фаз вносят значительный вклад;
- выполнить транскатетерную эмболизацию в случаях метастазов опухолей островковых клеток или карциноидных метастазов или химиоэмболизации в случаях гепатоцеллюлярной карциномы.
Подготовка пациента и противопоказания такие же, как при обычной ангиографии.
Методы диагностики, такие как УЗИ, КТ и МРТ, снизили диагностическую значимость артериографии в диагностике опухолей печени. Роль ангиографии печени, по-видимому, ограничивается периодическим картированием анатомии сосудов перед операцией и транскатетерным лечением опухолей печени.

 Причины и факторы риска
Причины и факторы риска Варикозное расширение вен пищевода
Варикозное расширение вен пищевода Использование зонда Блэкмора
Использование зонда Блэкмора
