Для чего нужны оральные антикоагулянты?
Антикоагулянты — это лекарственные препараты, снижающие активность свертывающей системы крови и препятствующие чрезмерному образованию тромбов. Современные антикоагулянты оказывают влияние на различные звенья процесса коагуляции крови и применяются для профилактики и лечения артериальных или венозных тромбозов и тромбоэмболий.
Классификация антикоагулянтов
Все антикоагулянтные препараты разделяются на две большие группы:
- антикоагулянты прямого действия (препараты назначаются в виде инъекций), угнетающие активность тромбина — прямые антикоагулянты;
- антикоагулянты непрямого действия, или оральные антикоагулянты (назначаются в виде таблеток), нарушающие образование протромбина в печени. Их также называют антагонистами витамина К, или непрямыми антикоагулянтами.
Антикоагулянты непрямого действия
Витамин К — витамин естественного происхождения, содержащийся в основном в зеленых листовых овощах (шпинат, брокколи, латук) и попадающий в организм с пищей. Кроме того, витамин K синтезируется бактериями в кишечнике. Организм использует витамин К для образования в печени целого ряда белков, участвующих в свертывании крови. Суточная потребность витамина К: 0,03-1,5 мкг/кг/сут (до 105 мкг/сут).
Таблица 1. Содержание витамина К в продуктах (мкг/100 г продукта)
| Продукты | Содержание витамина К |
| Зеленый чай, листья | 964 |
| Салат-латук, зеленые листья | 850 |
| Мангольд, листья сырые | 830 |
| Капусты лист | 817 |
| Кочанная капуста, сырая | 487 |
| Брюссельская капуста | 434 |
| Шпинат, листья сырые | 383 |
| Шпинат, листья свежие/замороженные, сваренные | 360 |
| Черный чай, листья | 42 |
| Брюссельская капуста, свежая, замороженная | 289 |
| Цикорий сырой | 231 |
| Салат краснолистный | 210 |
| Брокколи сырая | 205 |
| Соевое масло | 193 |
| Брокколи свежая/замороженная, сваренная | 192 |
| Зеленый лук | 190 |
| Фасоль | 140 |
| Салат Айсберг | 123 |
Оральные антикоагулянты, вмешиваясь в этот процесс, существенно увеличивают время свертывания крови. Однако пероральные антикоагулянты не разжижают кровь и не растворяют уже образовавшиеся сгустки крови, хотя и позволяют прекратить рост имеющихся тромбов.
В норме естественные антикоагулянты крови способствуют тому, что ее свертывание происходит только при нарушении целостности кровеносных сосудов. Однако при определенных клинических состояниях, называемых тромбозными нарушениями, этот же механизм может приводить к нежелательному образованию опасных для жизни кровяных сгустков — тромбов. В таких ситуациях действие антикоагулянтов позволяет предотвратить избыточное тромбообразование.
Если у вас обнаружили тромб или существует опасность образования кровяных сгустков, в качестве одного из элементов лечения врач может назначить лечение антикоагулянтами (например, варфарином), которые предотвращают образование тромбов.
Классификация антикоагулянтов непрямого действия
Все антикоагулянты непрямого действия подразделяются на три основные группы:
- монокумарины – варфарин, маркумар, синкумар;
- дикумарины – дикумарин, тромексан;
- индандионы – фенилин, дипаксин, омефин.
Самым распространенным непрямым антикоагулянтом является варфарин, что связано с предсказуемостью его действия и стабильными показателями антикоагуляции.
Показания к назначению пероральных антикоагулянтов
Можно выделить следующие основные причины применения оральных антикоагулянтов:
- мерцательная аритмия: нарушение сердечного ритма в виде беспорядочного сокращения предсердий, которое может приводить к образованию сгустков на их стенках;
- механические клапаны сердца: хирургическая замена поврежденных сердечных клапанов их механическими аналогами. При этом организм реагирует на «чужеродный» механических клапан и запускает нежелательный процесс свертывания крови.
Примерно 75% осложнений после операций по протезированию клапана связано с кровотечением и тромбоэмболией, которые могут возникнуть в течение первого года после операции 1 .
У пациентов с механическим протезом митрального клапана массивная тромбоэмболия происходит с частотой 4-12 % в год. У больных с механическим протезом в аортальной позиции этот показатель выше 2 .
Варфарин помогает снизить эти показатели примерно до 1 % и продолжает оставаться наиболее эффективным препаратом для большинства пациентов 3 .
- Тромбоз глубоких вен: при замедлении кровообращения сгустки могут образовываться в глубоких венах мышц бедра или таза.
Аспирин Кардио или варфарин?
Исходя из определенных критериев (возраста и дополнительных факторов риска), лечащий врач может назначить пациентам с мерцательной аритмией, один из двух вариантов антитромботических средств: антиагрегантные препараты, например, аспирин (препятствует склеиванию тромбоцитов) или антикоагулянтные препараты, например, варфарин (блокирует факторы свертывания крови):
- ацетилсалициловая кислота (аспирин), если риск инсульта невысок;
- варфарин, который рекомендуется при более высоком риске инсульта.
Фармакологическое действие аспирина как антикоагулянта заключается в угнетении слипания тромбоцитов — основного компонента тромба, таким образом, ацетилсалициловая кислота, предупреждает развитие тромбоза кровеносных сосудов.
Показанием к применению аспирина для разжижения крови является наличие преходящего нарушения мозгового кровообращения в прошлом – т.е. такого нарушения, при котором неврологическая симптоматика проявлялась не более 24 часов.
Оба препарата принимаются в виде таблеток, однако при приеме варфарина необходим более тщательный контроль коагуляции крови. Поэтому сегодня типичным решением ежедневной профилактики тромбоза является длительное применение низких доз аспирина для разжижения крови (Аспирин Кардио). Но результаты исследований свидетельствуют о том, что для уменьшения риска инсульта варфарин более эффективен 4 .
Кроме того, в инструкции по применению Аспирин Кардио для разжижения крови отдельно указан значительный перечень противопоказаний. Так же в любой инструкции к аспирину упоминается о выраженных нежелательных эффектах, развивающихся при длительном применении аспирина для разжижения крови даже в низких дозировках. При длительном приёме ацетилсалициловой кислоты, входящей в состав Аспирин Кардио, возможно развитие эрозий и язв желудочно-кишечного тракта, тромбоцитопения (снижении числа тромбоцитов), повышение уровня печёночных ферментов.
У таблеток аспирина нет явных преимуществ и в отношении стоимости. Цена «аспирина для сердца» вполне сравнима со стоимостью лечения варфарином. Даже американский аспирин для разжижения крови – далеко не панацея.
В сравнении со случаями, когда никакое лечение не проводится, варфарин снижает опасность инсульта на 64 %, что почти в три раза больше, чем при приеме аспирина для разжижения крови (для получения дополнительной информации обратитесь к врачу, который сможет рекомендовать наиболее подходящий вам препарат).

Рисунок 1. Варфарин и риск инсульта
В некоторых случаях препараты непрямых антикоагулянтов нужно принимать несколько месяцев, иногда на протяжении всей жизни. Продолжительность курса определяет врач.
Прямые и непрямые антикоагулянты снижают свертываемость крови, следовательно, повышают риск кровотечения, поэтому соблюдение режима дозирования имеет жизненно важное значение. Ни в коем случае нельзя увеличивать дозировку или сокращать интервал приема антикоагулянтов.
Первостепенное значение также имеет контроль эффективности этих препаратов: анализ крови, который называется МНО (международное нормализованное отношение), помогает подобрать наиболее оптимальную дозировку оральных антикоагулянтов.
Гемостатические средства
Гемостатические средства — лекарственные средства, способствующие остановке кровотечений. Все гемостатики, в зависимости от механизма действия, подразделяются на три большие группы:
- ингибиторы фибринолиза (антифибринолитики);
- средства, усиливающие свертывание крови (коагулянты);
- средства, понижающие сосудистую проницаемость.
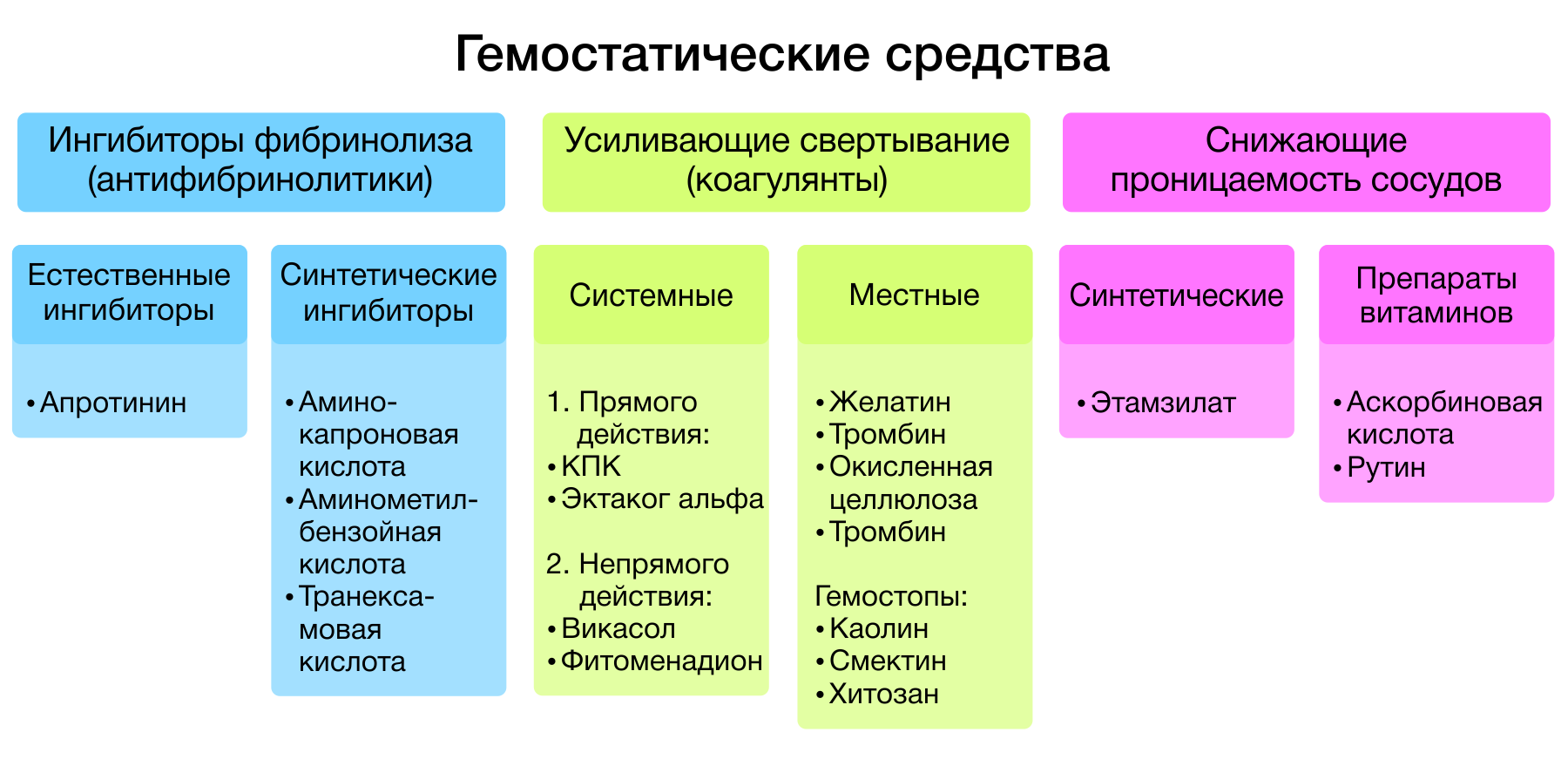
Рисунок 1 | Классификация гемостатиков.
1. Ингибиторы фибринолиза.
В клинической практике широкое распространение получили две группы препаратов ингибиторов фибринолиза: естественные ингибиторы фибринолиза (апротинин и его аналоги) и синтетические ингибиторы фибринолиза (аминокапроновая кислота, аминометилбензойная кислота, транексамовая кислота).
Апротинин — полипептид, получаемый из легких, поджелудочной и околоушной желез крупного рогатого скота, действующий аналогично α2-антиплазмину. Апротинин разрушает свободный плазмин, практически не взаимодействует со связанным плазмином, а также угнетает активацию тромбоцитов. Являясь сериновой протеазой, апротинин блокирует калликреин-кининовую систему путем разрушения калликреина, снижает активность отдельных протеолитических ферментов, таких как: трипсин, химотрипсин, кининогеназа. Изначально препарат был включен в рекомендации по лечению острого панкреатита и панкреонекроза, однако не подтвердил свою эффективность, и показания к его применению были пересмотрены.[1]
Аминокапроновая кислота – 6-аминогексановая кислота — синтетическое производное лизина. Присоединяясь к лизин-связывающему участку плазминогена, аминокапроновая кислота обратимо блокирует процесс фибринолиза, снижает активность стрептокиназы, урокиназы, тканевых киназ, калликреина, трипсина и гиалуронидазы. Аналогичным фармакологическим эффектом обладает производное аминокапроновой кислоты — аминометилбензойная кислота, отличающаяся улучшенной фармакокинетикой. Аминокапроновая кислота снижает активность тромболитических препаратов и может быть использована для нейтрализации их эффекта.
Транексамовая кислота — транс-4-(аминометил)-циклогексанкарбоновая кислота — обратимо блокирует эффект плазминогена, адгезию лейкоцитов и тромбоцитов на поверхность тромба за счет конкурентного ингибирования активатора плазминогена. Оказывает противоаллергическое и противовоспалительное действие посредством подавления образования кининов и других активных пептидов, участвующих в аллергических и воспалительных реакциях. По мощности антифибринолитического действия транексамовая кислота значительно превосходит аминокапроновую кислоту. Активность препарата в плазме сохраняется на протяжении 7-8 часов, в тканях — до 17 часов.[2]
У больных с высоким риском массивной кровопотери в плановой хирургии (сердечно-сосудистая хирургия, травматология и ортопедия, трансплантология) применение ингибиторов фибринолиза уменьшает интраоперационную кровопотерю и снижает потребность в трансфузии донорской крови. На протяжении 20 лет проводилось множество исследований, результаты которых были неоднозначны: мнения склонялись то в пользу апротинина, то в пользу синтетических производных лизина.
В 2007 году компания Bayer завершила исследование BART (Blood conservation using antifibrinolytics in a randomized trial), в котором было изучено действие апротинина у кардиохирургических больных высокого риска. Исследователи выявили большой риск летальных исходов и осложнений при использовании апротинина. В группе апротинина количество больных с массивной кровопотерей было несколько меньше, но 30-дневная летальность на 50% превышала аналогичный показатель в других группах.[3]
После публикации результатов BART компания Bayer уведомила Управление по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) о намерении изъять апротинин с рынка. Показания к назначению были пересмотрены, и препарат был исключен из списка безопасных лекарственных средств.
Огромный мета-анализ позволил сделать вывод, что транексамовая кислота обеспечивает такое же снижение периоперационной трансфузии, какое наблюдается при использовании апротинина, но более безопасна. Согласно рекомендациям Европейского общества анестезиологов по ведению пациентов с массивной периоперационной кровопотерей (2013 г.), при массивном кровотечении рекомендуется применение транексамовой кислоты (20-25 мг/кг); она может быть введена повторно или применяться в виде пролонгированной инфузии (1-2 мг/кг/ч).[4]
2. Препараты, усиливающие свертывание крови
Среди средств, повышающих скорость свертывания крови, выделяют: средства системного действия и для местного применения. К препаратам системного действия относят непрямые коагулянты (фитоменадион, менадиона натрия бисульфит) и коагулянты прямого действия (факторы свертывания: концентрат протромбинового комплекса, эптаког альфа).
Менадиона натрия бисульфит — синтетический водорастворимый аналог витамина К3. Субстратно стимулирует витамин K-редуктазу, активирующую витамин К и обеспечивающую его участие в печеночном синтезе витамин K-зависимых плазменных факторов гемостаза (II, VII, IX, X). Фитоменадион является синтетическим структурным аналогом витамина К1, обладает большей активностью и более ранним началом реализации эффектов (через 6-10 часов после перорального применения, против 18-24 часов у менадиона натрия бисульфита). Данная группа препаратов показана для коррекции нарушений системы гемостаза, вызванных дефицитом витамина К1, передозировкой антикоагулянтов непрямого действия (варфарина), а также для предоперационной профилактики кровотечений.
Концентрат протромбинового комплекса (КПК) — лекарственный препарат, содержащий факторы II, VII, IX, X, а также следовые концентрации антитромбина III, гепарина, протеинов С и S. Основным показанием к применению КПК служит коррекция приобретенного дефицита витамин К1-зависимых факторов в экстренных ситуациях (кровотечение, экстренная операция). Помимо этого, КПК широко используется как средство для лечения и профилактики кровотечений у пациентов с врожденным дефицитом одного из К1 зависимых факторов свертывания (врожденная гипопротромбинемия, врожденный дефицит фактора Стюарта – Прауэра).[5]
Эптаког альфа — рекомбинантный активированный VII фактор свертывания. Механизм действия препарата заключается в прямой активации фактора Х на поверхности активированных тромбоцитов. Это вызывает «тромбиновый взрыв» независимо от имеющейся концентрации факторов VIIIa и IXa. В результате образуется стабильный фибриновый сгусток. Считается, что эптаког альфа инициирует гемостаз только в месте повреждения ткани и не вызывает системной активации механизмов свертывания. Препарат был разработан для лечения кровотечений и проведения хирургических вмешательств у пациентов с наследственной или приобретенной гемофилией и высоким титром ингибитора факторов свертывания VIIIa или IXa. Его применение у пациентов с массивным кровотечением можно сформулировать согласно рекомендациям ESA (2013): «Применение рекомбинантного фактора VII возможно только при кровотечениях, которые не могут быть устранены хирургическими методами или путем комплексной гемостаз-корригирующей терапии». Необходимо серьезное обоснование для применения данного препарата [6].
3. Местные гемостатики
Местные гемостатики используются для остановки капиллярных и паренхиматозных кровотечений преимущественно в неотложной хирургии и стоматологии. Данная группа включает в себя широкий спектр препаратов с различным механизмом действия.
Препараты на основе желатина, получаемого из свиной кожи, существуют в трех формах: пленка, губка и порошок. Желатин чрезвычайно гигроскопичен, и за счет этого свойства он абсорбирует влагу, увеличиваясь в размерах и заполняя тканевой дефект. Существуют комбинации желатина с тромбином, которые помимо пассивного гемостатического эффекта напрямую запускают коагуляционный каскад и активируют тромбоциты в месте нанесения. Желатин разрушается протеиназами в течение 4-6 недель. Несмотря на абсолютную индифферентность, желатин может служить в качестве хронического очага инфекции. Помимо этого, одним из существенных недостатков данных препаратов является отсутствие прочных связей с окружающими тканями [7].
Тромбин является естественным компонентом свертывающей системы крови. Раствор тромбина используют только местно при капиллярных или паренхиматозных кровотечениях в ходе нейрохирургических вмешательств, операций на печени и почках, в стоматологической практике. Попадание тромбина в крупные кровеносные сосуды может вызвать распространенный тромбоз [7].
Окисленная целлюлоза выпускается в виде пленок, сеток, пучков и губок. Данный биологический агент играет роль субстрата для агрегации тромбоцитов и активации механизмов гемостаза. Целлюлоза значительно снижает рН среды, что приводит к лизису эритроцитов с образованием кислого гематина, который формирует дополнительный искусственный сгусток. Помимо этого окисленная целлюлоза обладает антибактериальным эффектом, в том числе в отношении антибиотикорезистентных микроорганизмов [7].
Микрофибриллярный коллаген, производимый из кожи крупного рогатого скота, имеет ряд преимуществ перед остальными топическими биологическими кровоостанавливающими агентами, среди которых: быстрый гемостатический эффект, минимальная реактивность тканей и высокая способность к реабсорбции. Аналогично целлюлозе, микрофибриллярный коллаген является матрицей для активации тромбоцитов, агрегации и образования тромбов [7].
Подвидом местных кровоостанавливающих средств являются гемостопы, получившие большое распространение в военной медицине. Это препараты внешнего воздействия, которые почти не влияют на свертывающую и противосвертывающую системы крови. Многообразие форм выпуска обеспечивает удобство применения в полевых условиях и полностью удовлетворяет потребностям оказания неотложной помощи при любых кровотечениях. На сегодняшний день наиболее эффективным средством считается хитозан.
Хитозан – это полисахаридный биополимер, получаемый из хитиновых панцирей ракообразных. Кровоостанавливающий эффект данного вещества достигается путем связывания хлопьев хитозана с отрицательно-заряженными эритроцитами и образования гелеобразного сгустка в месте контакта с кровью. Среди преимуществ препаратов на основе хитозана выделяют его антимикробные свойства, длительный срок хранения, стабильность при перепадах температур и безопасность при наружном использовании [8].
Наиболее известным представителем группы средств, понижающих сосудистую проницаемость, является этамзилат. Гемостатический эффект данного препарата обусловлен активацией тромбопластина в месте повреждения сосудов микроциркуляторного русла и снижением синтеза простациклина PGI-2 в эндотелии сосудов, что в конечном итоге приводит к усилению адгезии и агрегации тромбоцитов, остановке или уменьшению кровоточивости. За счет антигиалуронидазного действия этамзилат обладает ангиопротективным эффектом, улучшает микроциркуляцию и нормализует проницаемость сосудистой стенки при патологических процессах [9].
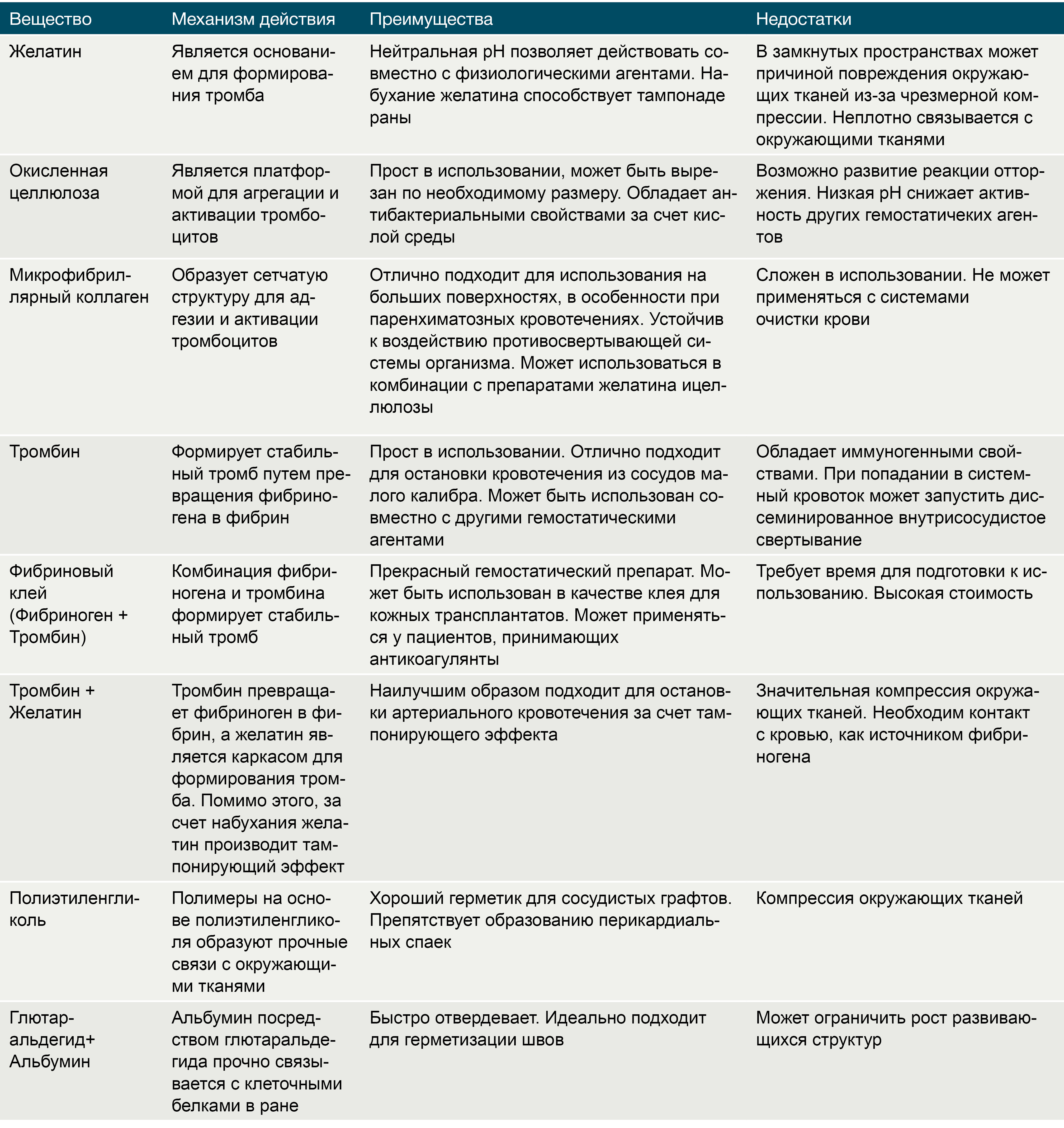 Таблица 1 | Характеристика местных гемостатиков.
Таблица 1 | Характеристика местных гемостатиков.
Источники
- Fergusson D. A. et al. A comparison of aprotinin and lysine analogues in high-risk cardiac surgery //New England Journal of Medicine. – 2008. – Т. 358. – №. 22. – С. 2319-2331.
- Williams-Johnson J. A. et al. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): a randomised, placebo-controlled trial //West Indian Medical Journal. – 2010. – Т. 59. – №. 6. – С. 612-624.
- Ferraris V. A. et al. Perioperative blood transfusion and blood conservation in cardiac surgery: the Society of Thoracic Surgeons and The Society of Cardiovascular Anesthesiologists clinical practice guideline //The Annals of thoracic surgery. – 2007. – Т. 83. – №. 5. – С. S27-S86.
- Sedrakyan A., Treasure T., Elefteriades J. A. Effect of aprotinin on clinical outcomes in coronary artery bypass graft surgery: a systematic review and meta-analysis of randomized clinical trials //The Journal of thoracic and cardiovascular surgery. – 2004. – Т. 128. – №. 3. – С. 442-448.
- Song H. K. et al. Safety and efficacy of prothrombin complex concentrates for the treatment of coagulopathy after cardiac surgery //The Journal of thoracic and cardiovascular surgery. – 2014. – Т. 147. – №. 3. – С. 1036-1040.
- Shapiro A. D. et al. Prospective, randomised trial of two doses of rFVIIa (NovoSeven) in haemophilia patients with inhibitors undergoing surgery //Thrombosis and haemostasis. – 1998. – Т. 79. – №. 05. – С. 773-778.
- Achneck H. E. et al. A comprehensive review of topical hemostatic agents: efficacy and recommendations for use //Annals of surgery. – 2010. – Т. 251. – №. 2. – С. 217-228.
- McManus J. G., Wedmore I. Modern Hemostatic Agents for Hemorrhage Control â A Review and Discussion of Use in Current Combat Operations. – 2005.
- Okuma M. et al. Effects of etamsylate on platelet functions and arachidonic acid metabolism //Thrombosis and haemostasis. – 1982. – Т. 48. – №. 3. – С. 330-333.
Препараты, снижающие свертываемость крови. Когда используются антикоагулянты?
” data-image-caption=”” data-medium-file=”https://unclinic.ru/wp-content/uploads/2020/10/preparaty-snizhajushhie-svertyvaemost-krovi.-kogda-ispolzujutsja-antikoaguljanty-900×600.jpg” data-large-file=”https://unclinic.ru/wp-content/uploads/2020/10/preparaty-snizhajushhie-svertyvaemost-krovi.-kogda-ispolzujutsja-antikoaguljanty.jpg” title=”Препараты, снижающие свертываемость крови. Когда используются антикоагулянты?”>
Алена Герасимова (Dalles) Разработчик сайта, редактор
- Запись опубликована: 30.10.2020
- Время чтения: 1 mins read
Свертывание крови – это многоступенчатый процесс, необходимый для поддержания гемостаза организма.
Гемостаз заключается в обеспечении непрерывного потока крови по кровеносным сосудам либо за счет свертывания крови при разрыве сосуда, либо за счет процесса фибринолиза – разрушения сгустка крови. Антикоагулянты выпускаются в форме таблеток, капсул, мазей, кремов, гелей и инъекций.
Антикоагулянты – это препараты, которые, уменьшая свертываемость крови, снижают риск образования опасных сгустков крови в кровеносных сосудах и сердце или растворяют существующие сгустки крови.
Показания к приему антикоагулянтов
Антикоагулянты в основном используются при таких заболеваниях, как:
- венозный тромбоз;
- артериальный тромбоз;
- легочная эмболия;
- стойкая фибрилляция предсердий;
- состояние после имплантации искусственных клапанов сердца.
Препараты свертывания крови следует принимать регулярно. Если пациент забыл принять дозу, нельзя принимать двойную дозу на следующий день.
Антикоагулянты, отпускаемые без рецепта:
- ацетилсалициловая кислота;
- гепарин.
Рецептурные препараты для свертывания крови:
- лекарства, блокирующие рецепторы тромбоцитов;
- лекарства, подавляющие выработку тромбоцитов;
- препараты, подавляющие активность тромбина;
- ингибиторы фактора свертывания Ха;
- активный протеин C.;
- антагонисты витамина К.
Ацетилсалициловая кислота
Ацетилсалициловая кислота – это основной препарат, предотвращающий агрегацию тромбоцитов (разжижающий кровь), которые играют важную роль в свертывании крови. Ацетилсалициловая кислота необратимо подавляет механизм, стимулирующий агрегацию тромбоцитов. Введение даже небольшой дозы лекарства вызывает снижение коагуляции на период от 4 до 7 дней, то есть на время жизни тромбоцитов.
Пероральный препарат используется для предотвращения сердечных приступов, сердечно-сосудистых заболеваний у людей со стенокардией и для предотвращения вторичной церебральной ишемии.
Ацетилсалициловую кислоту из-за ее раздражающего действия на слизистую оболочку глотки следует принимать после еды. Наиболее важные побочные эффекты – аллергические реакции, поэтому людям, страдающим астмой, ацетилсалициловую кислоту не выписывают.
Гепарин
Гепарин – это смесь гликозаминогликанов, полученных из ткани легких крупного рогатого скота или эпителия кишечника свиней. Используется в безрецептурных кремах, мазях и гелях, а также в виде рецептурных инъекций.
Этот препарат используется местно при лечении поверхностного тромбофлебита, травм мягких тканей и варикозного расширения вен. При подкожном или внутривенном введении эффект достигается через несколько секунд. В таком виде он используется для профилактики венозных и артериальных сгустков, в острой фазе инфаркта миокарда и при переливаниях крови.
Побочный эффект гепарина – кровотечение. Также использование гепарина может вызвать позднюю тромбоцитопению, что может привести к парадоксальному тромбозу. В случае передозировки гепарином в качестве специфического антидота используют сульфат протамина.
Антиагрегантные препараты
Антитромбоцитарные препараты останавливают активность или производство тромбоцитов. Такие лекарства используются для профилактики инфарктов и инсультов. Дополнительные показания к применению этой группы препаратов включают поддержание проходимости пересаженных сосудов и улучшение кровоснабжения конечностей при лечении атеросклеротических поражений.
В группу антиагрегантов, разрешенных в Европе, входят:
- Тиклопидин . Препарат, выпускаемый в форме таблеток. Препарат показан для снижения риска ишемического инсульта, для профилактики ишемических состояний, особенно коронарных сосудов, а также при нарушениях кровоснабжения конечностей, вызванных атеросклерозом. Максимальный эффект наступает через 3-7 дней после начала использования. Основные побочные эффекты – нарушения пищеварительной системы и изменение картины крови.
- Клопидогрель. Этот препарат оказывает аналогичное, но более сильное действие, чем тиклопидин. Клопидогрель более эффективный, более быстрый и с меньшим количеством побочных эффектов, чем тиклопидин. Это лекарство в таблетках, которое обычно принимают один раз в день.
- Прасугрел. Самый современный препарат этой группы. Фармакологическое действие проявляет активный метаболит этого вещества. Этот препарат действует лучше и быстрее, чем клопидогрель. Он используется у людей с острым коронарным синдромом для предотвращения сердечно-сосудистых заболеваний. Препарат может вызвать носовое и желудочно-кишечное кровотечение, что может привести к анемии.
- Тикагрелор . В отличие от тиклопидина и прасугреля, является активным веществом и не требует метаболических превращений для достижения желаемого эффекта. Он используется в сочетании с ацетилсалициловой кислотой для предотвращения сердечно-сосудистых заболеваний у людей с коронарным синдромом. Побочные эффекты помимо кровотечения: потенциальная одышка и повышение уровня креатина и мочевой кислоты в крови.
Лекарства, блокирующие рецепторы тромбоцитов
Блокаторы рецепторов тромбоцитов действуют путем связывания с рецепторами GP IIb / IIIa на поверхности тромбоцитов, предотвращая их активацию другими факторами, что приводит к снижению свертывания крови.
- Эптифибатид . Антикоагулянтный препарат, применяемый только внутривенно в условиях стационара. Этот препарат предназначен для использования с ацетилсалициловой кислотой и гепарином. Он показан для профилактики раннего инфаркта миокарда. Наиболее частое побочное действие препарата – кровотечения как низкой, так и высокой интенсивности.
Эптифибатид
Лекарства, подавляющие выработку тромбоцитов
Они работают, подавляя созревание тромбоцитов. Эти препараты используются при тромбоцитемии. Этот препарат может вызвать серьезные проблемы с сердечно-сосудистой системой, поэтому людям с сердечными заболеваниями следует применять его очень осторожно под тщательным медицинским наблюдением.
- Анагрелид. Препарат, механизм действия которого до конца не изучен. Этот препарат снижает количество вырабатываемых тромбоцитов в зависимости от дозы. Вполне вероятно, что этот препарат действует через активный метаболит, который образуется в организме после приема. Этот препарат не оказывает значительного влияния на уровень лейкоцитов в крови и мало влияет на эритроциты.
Препараты, подавляющие активность тромбина
Тромбин – ключевой фермент, участвующий в образовании сгустка. Помимо активации тромбоцитов, этот фермент непосредственно влияет на образование сгустка. Среди этих препаратов есть препараты, которые прямо ингибируют активность тромбина и косвенно ингибируют этот фермент.
- Антитромбин III. Естественный ингибитор свертывания крови, вырабатываемый в организме печенью. Помимо ингибирования активации тромбина, он влияет на другие факторы свертывания крови. Этот препарат применяется при врожденном или приобретенном дефиците антитромбина и при тромбоэмболических синдромах, при которых гепарин неэффективен. Антитромбин вводится путем инъекции.
- Гирудины. Это препараты, подавляющие активность тромбина независимо от наличия антитромбина в крови. Натуральный гирудин получают из слюнных желез медицинской пиявки Hirudo medicinalis. Гирудины не снижают количество тромбоцитов и не изменяют кровяное давление. Помимо природного гирудина, существуют также рекомбинантные гирудины – лепирудин и дезирудин – и синтетический гирудин – бивалирудин.
- Дабигатран. Препарат для перорального применения. Он напрямую подавляет активность тромбина. Его вводят в виде неактивного пролекарства, которое затем метаболизируется в организме до активной формы препарата. Это лекарство используется для предотвращения тромбоэмболических осложнений после установки протеза бедра и колена.
- Низкомолекулярные гепарины . Получают путем химической или ферментативной модификации структуры животного гепарина. Механизм их действия заключается в первую очередь в ингибировании активности фактора Ха и, в меньшей степени, в ингибировании активности тромбина. По сравнению с гепарином животного происхождения, низкомолекулярные гепарины более биодоступны, но меньше ингибируют агрегацию тромбоцитов. Вещества этой группы вводятся инъекционно. Гепарины с низкой молекулярной массой включают в себя: ardeparin, certoparin, дальтепарин, enoxyparin, Надропарин, ревипарин и tinazaparin.
Фондапаринукс
Ингибиторы фактора свертывания Ха
Этот класс препаратов действует путем прямого или косвенного ингибирования фактора Ха. Лекарства, которые косвенно влияют на фактор Ха, действуют, стимулируя антитромбин III, тем самым снижая эффект фактора Ха. Препараты этой группы вводятся инъекционно.
- Фондапаринукс (фондапаринукс натрия). Препарат, вводимый под кожу. Это вещество не метаболизируется в организме и в неизмененном виде выводится почками. Препарат вводят 1 раз в сутки в связи с длительным периодом полувыведения в организме. Фондапаринукс используется для предотвращения тромбоэмболических осложнений, ишемической болезни сердца и сердечного приступа.
- Сулодексид . Препарат, вводимый в инъекциях и капсулах. Препарат представляет собой производное гепарина с аналогичным действием. Помимо антикоагулянтной активности, сулодексид снижает липиды крови. Этот препарат используется при заболеваниях, связанных с повышенным риском тромбоза, атеросклероза и ишемической болезни сердца.
- Ксабаны . Это пероральные прямые ингибиторы фактора свертывания крови Ха. Они не действуют против тромбина и не уменьшают количество тромбоцитов. Эти препараты, вводимые в рекомендуемых дозах, не требуют контроля свертывания крови. Ривароксабан, эдоксабан и апиксабан показаны для профилактики ВТЭ и для профилактики тромбоэмболических осложнений у пациентов с фибрилляцией предсердий.
Активный протеин C
Активный протеин C – это ненумерованный фактор свертывания крови. Этот белок синтезируется в печени с помощью витамина К. Дротрекогин альфа – рекомбинантная форма белка С. Этот препарат показан для предотвращения смертности при сепсисе и септическом шоке. Показанием к применению этого препарата также является дефицит протеина С.
Побочный эффект препарата – кровотечение, что требует немедленного прекращения терапии.
Антагонисты витамина К
Антагонисты витамина К составляют группу соединений, действующих противодействуя витамину К. Эта группа включает как производные кумарина (аценокумарол и варфарин), так и производные индандиона. Механизм действия этих препаратов связан с ингибированием превращения витамина К в активную форму витамина К.
Когда антагонисты витамина К вводятся перорально, ожидаемый терапевтический эффект проявляется только после периода истощения полных факторов крови, доступных в организме. Полный эффект от препаратов из этой группы наступает только через 2-4 дня от начала применения. В случае передозировки лекарством витамин К используется как специфический антидот.
Показание к применению – тромбоэмболия. Обычно эти препараты используются с гепарином быстрого действия.
Средства, повышающие свертываемость крови коагулянты
Средства, повышающие свертываемость крови (гемостатики) коагулянты
Согласно классификации,эту группу препаратов делят на коагулянты прямого и непрямого действия, однако иногда их делят и по другому принципу :
1) для местного применения (тромбин, губка гемостатическая, пленка фибринная и др.)
2) для системного применения (фибриноген, викасол).
ТРОМБИН (Trombinum; сухой порошок в амп. по о,1, что соответствует 125 ед. активности; во флаконах по 10 мл) коагулянт прямого действия для местного применения. Являясь естественным компонентом свертывающей системы крови, вызывает эффект in vitro и in vivo.
Перед использованием порошок растворяют в физрастворе. Обычно порошок в ампуле представляет собой смесь тромбопластина, кальция и протромбина.
Применяют только местно. Назначают больным с кровотечениями из мелких сосудов и паренхиматозных органов (операции на печени, почках, легких, мозге), кровотечениями из десен. Используют местно в виде пропитанной раствором тромбина гемостатической губки, губки гемастатической коллагеновой, или просто прикладывая тампон, пропитанный раствором тромбина.
Иногда, особенно в педиатрии,тромбин применяют внутрь (содержимое ампулы растворяют в 50 мл хлорида натрия или 50 мл 5% раствора амбена,назначают по 1 столовой ложке 2-3 раза в день) при желудочных кровотечениях или путем ингаляции при кровотечениях из дыхательных путей.
ФИБРИНОГЕН (Fibrinogenum; во флаконах по 1,0 и 2,0 сухой пористой массы) – используется для системного воздействия. Получают также из плазмы крови доноров. По влиянием тромбина фибриноген превращается в фибрин, образующий тромбы.
Рекомендуемые файлы
Фибриноген используют как средство скорой помощи.
Особенно эффективен он тогда, когда наблюдается его дефицит при массивных кровотечениях (отслойка плаценты, гипои афибриногенемия, в хирургической, акушерской, гинекологической и онкологической практике).
Назначают обычно в вену, иногда местно в виде пленки, наносимой на кровоточащую поверхность.
Перед применением препарат растворяют в 250 или 500 мл подогретой воды для инъекций. Внутривенно вводят капельно или медленно струйно.
ВИКАСОЛ (Vicasolum; в таб, по 0,015 и в амп. по 1 мл 1% раствора) непрямой коагулянт, синтетический водорастворимый аналог витамина К, который активизирует процесс образования фибринных тромбов. Обозначают как витамин К3.
Фармакологический эффект вызывает не сам викасол, а образующиеся из него витамины К1 и К2, поэтому эффект развивается через 12-24 часа, при внутривенном введении – через 30 минут, при внутримышечном – через 2-3 часа.
Указанные витамины необходимы для синтеза в печени протромбина (II фактор), проконвертина (VII фактор), а также IX и X факторов.
Показания к применению : при чрезмерном снижении протромбинового индекса, при выраженной К-витаминной недостаточности, обусловленной :
1) кровотечением из паренхиматозных органов;
2) процедурой заменного переливания крови, если переливали (ребенку) консервированную кровь; а также при :
3) длительном применении антагонистов витамина К аспирина и НПВС (нарушающих агрегацию тромбоцитов);
4) длительном применении антибиотиков широкого спектра действия (левомицетина, ампициллина, тетрациклина, аминогликозидов, фторхинолонов);
5) применении сульфаниламидов;
6) профилактике геморрагической болезни новорожденных;
7) длительной диарее у детей;
9) у беременных женщин,особенно у страдающих туберкулезом и эпилепсией и получающих соответствующее лечение;
10) передозировке антикоагулянтов непрямого действия;
11) желтухах, гепатитах, а также после ранений, кровотечений (геморрой, язва, лучевая болезнь);
12) подготовке к хирургической операции и в постоперационном периоде.
Эффекты могут быть ослаблены при одновременном назначении антагонистов викасола : аспирин, НПВС, ПАСК, непрямые антикоагулянты группы неодикумарина.
Побочные эффекты : гемолиз эритроцитов при внутривенном введении.
ФИТОМЕНАДИОН (Phytomenadinum;по 1 мл для внутривенного введения, а также капсулы, содержащие 0,1 мл 10% масляного раствора, что соответствует 0,01 препарата). В отличие от природного витамина К1 (транс-соединения) является синтетическим препаратом. Представляет рацемическую форму (смесь транс- и цис- изомеров), а по биологической активности сохраняет все свойства витамина К1. Быстро всасывается и поддерживает пик концентрации до восьми часов.
Показания к применению: геморрагический синдром с гипопротромбинемией, вызванной снижением функций печени (гепатиты, циррозы печени), при язвенных колитах, при передозировке антикоагулянтов, при длительном использовании высоких доз антибиотиков широкого спектра действия и сульфаниламидов; перед тяжелыми операциями для снижения кровоточивости.
Побочные эффекты : явления гиперкоагуляции при несоблюдении режима дозирования.
Из средств, относящихся к коагулянтам прямого действия в клинике также используются препараты :
1) протромбиновый комплекс (VI,VII,IX,X факторы);
2) антигемофильный глобулин (VIII фактор).
ИНГИБИТОРЫ ФИБРИНОЛИЗА (АНТИФИБРИНОЛИТИКИ)
КИСЛОТА АМИНОКАПРОНОВАЯ (АКК) – порошкообразный синтетический препарат, тормозит превращение профибринолизина (плазминогена) в фибринолизин (плазмин) путем воздействия на активатор профибринолизина и этим способствует сохранению фибринных тромбов.
Кроме того, АКК является также ингибитором кининов и некоторых факторов системы комплимента.
Обладает противошоковой активностью (ингибирует протеолитические ферменты, а также стимулирует обезвреживающую функцию печени).
Препарат малотоксичен, быстро выводится из организма с мочой (через 4 часа).
Применяют в клинике скорой помощи, при хирургических вмешательствах и при различных патологических состояниях, когда повышена фибринолитическая активность крови и тканей:
1) при и после операций на легких, простате, поджелудочной и щитовидной железах;
2) при преждевременной отслойке плаценты, длительной задержке в матке мертвого плода;
3) при гепатитах, циррозах печени, при портальной гипертензии, при использовании аппарата искусственного кровообращения;
4) при II и III стадиях ДВС синдрома, при язвенных, носовых, легочных кровотечениях.
АКК вводят при массивных переливаниях консервированной крови, назначают внутривенно или внутрь.
Выпускается: порошок и флаконы по 100 мл стерильного 5% раствора в изотоническом растворе хлорида натрия. В связи с тем, что АКК обладает противошоковой активностью, ингибирует протеолитические ферменты и кинины, угнетает образование антител, препарат используется при шоковых реакциях и как антиаллергическое средство.
Побочные эффекты: возможно головокружение, тошнота, понос, легкий катар верхних дыхательных путей.
АМБЕН (Ambenum, аминометилбензойная кислота) – также синтетический препарат, по химической структуре похож на парааминобензойную кислоту. Белый порошок, плохо растворимый в воде. Это антифибринолитическое средство. Амбен ингибирует фибринолиз, по механизму действия схож с АКК.
Показания к применению те же. Назначают внутривенно, внутримышечно и внутрь. При введении в вену действует быстро, но кратковременно (3 часа). Форма выпуска : ампулы по 5 мл 1% раствора, таблетки по 0,25.
Иногда показаны антиферментные препараты, в частности, контрикал. Он ингибирует плазмин, коллагеназы, трипсин, химотрипсин, играющие важную роль в развитии многих патофизиологических процессов. Препараты этой группы оказывают ингибирующее действие на каталитическое взаимодействие отдельных факторов фибринолиза и процессов свертывания крови.
Показания к применению : локальный гиперфибринолиз постоперационные и постпортальные кровотечения; гиперменорея; генерализованный первичный и вторичный гиперфибринолиз в акушерстве и хирургии; начальная стадия ДВС-синдрома и др.
Побочное действие : редко аллергии; эмбриотоксическое действие; При быстром введении – недомогание, тошнота.
СРЕДСТВА, ПОВЫШАЮЩИЕ АГРЕГАЦИЮ И АДГЕЗИЮ ТРОМБОЦИТОВ
СЕРОТОНИН. Его применение связано со стимуляцией агрегации тромбоцитов, набуханием тканей, изменением микроциркуляции, что способствует возникновению тромбоцитарных тромбов. Серотонин в виде адипината (Serotonini adipinatis в ампулах по 1 мл 1% раствора) применяют внутривенно или внутримышечно при геморрагиях, связанных с патологией кровяных пластинок (тромбоцитопении, тромбоцитопатии). При этом повышается число тромбоцитов, укорачивается время кровотечения, повышается стойкость капилляров.
Используют при болезни Виллебрандта I типа, гипо- и апластических анемиях, при болезни Верльгофа, геморрагических васкулитах.
Нельзя использовать при патологии почек, больным с бронхиальной астмой, при гиперкоагуляции крови.
Побочное действие : при быстром введении – боль по ходу вены; боль в животе, в области сердца, подъем артериального давления, тяжесть в голове, тошнота, диарея, снижение диуреза.
КАЛЬЦИЙ непосредственно участвует в агрегации и адгезии тромбоцитов, а также способствует образованию тромбина и фибрина. Таким образом, он стимулирует образование и тромбоцитарных, и фибринных тромбов.
Показания к применению :
1) как средство, уменьшающее проницаемость сосудов, при геморрагических васкулитах;
2) как кровоостанавливающее средство при легочных, желудочных, носовых, маточных кровотечениях, а также перед операцией;
3) при кровотечениях, связанных со снижением кальция в плазме крови (после переливания больших количеств цитратной крови, плазмозаменителей).
Используют кальция хлорид (внутривенно и внутрь).
Побочные эффекты: при быстром введении возможна остановка сердца, снижение артериального давления; при внутривенном введении отмечается ощущение жара (“горячий укол”); при подкожном введении кальция хлорида – некроз тканей.
СРЕДСТВА, ПОНИЖАЮЩИЕ ПРОНИЦАЕМОСТЬ СОСУДИСТОЙ СТЕНКИ
АДРОКСОН (Adroxonum; в амп.по 1 мл 0,025%) – препарат адренохрома, метаболита адреналина. Он не повышает АД, не влияет на деятельность сердца и на свертывание крови. Основной его эффект – повышение плотности сосудистой стенки и активация агрегации и адгезии тромбоцитов.Поэтому адроксон оказывает гемостатическое действие при капиллярных кровотечениях,когда особенно повышена проницаемость стенок этих сосудов. Однако при массивных кровотечениях препарат не эффективен.
Показания к применению :
1) при паренхиматозных и капиллярных кровотечениях;
2) при травмах и операциях;
3) при кишечных кровотечениях у новорожденных;
5) при тромбоцитарной пурпуре.
Адроксон применяют местно (тампоны,салфетки), внутримышечно или подкожно. ЭТАМЗИЛАТ или дицинон (Ethamsylatum; в таб. по 0,25 и в амп.по 2 мл 12,5% раствора) – синтетик, производное диоксибензола. Препарат снижает проницаемость сосудов, уменьшает транссудацию и экссудацию жидкой части плазмы, нормализует проницаемость сосудистой стенки и улучшает микроциркуляцию, повышает свертываемость крови так как способствует образованию тромбопластина (гемостатический эффект). Последний эффект развивается быстро-при внутривенном введении через 5-15 минут, максимально выражено через 1-2 часа. В таблетках действие проявляется через 3 часа. Препарат вводят в вену, подкожно или внутримышечно.
Показания к применению :
1) тромбоцитарная пурпура;
2) кишечные и легочные кровотечения (хирургия);
3) геморрагический диатез;
4) операции на ЛОР-органах;
5) диабетические ангиопатии (офтальмология).
Люди также интересуются этой лекцией: 14. Рецензия.
Побочное действие – иногда возникает изжога, чувство тяжести в подложечной области, головная боль, головокружение, гиперемия лица, парастезия ног, снижение АД.
Для ликвидации повышенной проницаемости сосудов, особенно при наличии геморрагий, используют препараты витамина С (аскорбиновую кислоту), а также различные флавоноиды (рутин, аскорутин, кверцетин, витамин Р), а также витамеры, то есть полусинтетические производные – венорутон и троксевазин в различных лекарственных формах (капсулы, гель, растворы). Препараты витамина Р используют при интенсивной транссудации жидкой части плазмы, например, при отечности ног (тромбофлебит). Кроме того, эти препараты
назначают при геморрагическом диатезе, кровоизлияниях в сечатку, при лучевой блезни, арахноидитах, гипертонической болезни и при передозировке салицилатов. Рутин и аскорутин используют в педиатрии для ликвидации интенсивной транссудации у детей, больных скарлатиной, корью, дифтерией и токсическим гриппом.
РУТИН выпускается в таблетках по 0,02 (2-3 раза в день). АСКОРУТИН – по 0,05. ВЕНОРУТОН – в капсулах по 0,3; ампулах по 5 мл 10% раствора.
Препараты из растений (настои, экстракты, таблетки) оказывают слабое гемостатическое действие. Поэтому их используют при легких кровотечениях (носовые, геморроидальные),при кровоточивости, кровохарканьи, геморрагических диатезах, в акушерской и гинекологической практике.
Контроль анализов при приеме антикоагулянтов и других препаратов разжижающих кровь в поликлинический практике
Услуги нашего медцентра
ВАРФАРИН –является антагонистом витамина К, в результате чего снижается образование в печени протромбина и других факторов свертывания крови. Препарат назначается для лечения и профилактики тромбоза глубоких вен, эмболии легочной артерии, транзиторных ишемических атак, ишемического инсульта, для профилактики инфаркта миокарда, больным с мерцательной аритмией , пороками сердца и др. Дозировка препарата в начале лечения составляет обычно 5-10 мг в сутки, в последующем при достижении терапевтического эффекта она зависит от МНО.
КОНТРОЛЬ –проводится с помощью МНО (международное нормализированное отношение). При назначении варфарина МНО определяется перед началом лечения, затем через 2-3 дня, далее 1 раз в неделю. Если достигается желаемое значение МНО ( в среднем 2,0-3,0 в зависимости от патологи), то в последующем МНО определяют 1 раз в месяц. При стабильном значении МНО его можно определять 1 раз в 3 месяца. Числовое значение МНО и частоту его контроля определяет лечащий врач с учетом основного заболевания и сопутствующей патологии, а также возраста. У больных старше 75 лет повышен риск кровотечений.
ПЛАВИКС – (клопидогрель). Механизм действия связан с воздействием на мембрану тромбоцитов, вследствие этого происходят изменения агрегации( склеивание) тромбоцитов. Аналогичные препараты – тиклопидин, прасугрел, тикагрелол. В амбулаторной практике препарат назначается для профилактики тромботических осложнений у больных перенесших инфаркт миокарда, острый коронарный синдром, ишемический инсульт, окколюзию переферических артерий и др. Средняя доза плавикса 75 мг в сутки.
КОНТРОЛЬ – периодически проверяют количество тромбоцитов и время кровотечения. Частоту контроля определяет врач. При сочетании с аспирином риск кровотечений увеличивается.
АСПИРИН ( ацетилсалициловая кислота) – влияет на синтез арахидоновой кислоты и простагландинов, угнетает агрегацию (склеивание) тромбоцитов, вследствие чего улучшается микроциркуляция, текучесть крови. В амбулаторной практике аспирин назначается при ишемической болезни сердца (ИБС): после перенесенного инфаркта миокарда, стенокардии, после ишемического (некардиоэмболического) инсульта, преходящего нарушения мозгового кровообращения, периферическом атеросклерозе, при мерцательной аритмии (когда невозможно использовать пероральные антикоагулянты) и др. Препарат используется обычно в дозировке 75-100 мг в сутки. Лучше применять кишечнорастворимые формы аспирина (аспирин-кардио и др.) для уменьшения риска повреждения слизистой желудка.
КОНТРОЛЬ – периодически по назначению врача определяют АЧТВ (активированное частичное тромбиновое время) терапевтический эффект которого поддерживается на уровне в 1,5 – 2 раза выше нормы. В зависимости от лабораторного оборудования нормы АЧТВ могут быть различными. Кроме того, периодически необходимо контролировать количество тромбоцитов крови.
НИЗКОМОЛЕКУЛЯРНЫЕ ГЕПАРИНЫ
К этой группе препаратов относятся дальтепарин натрия (фрагмин) , надропарин кальция (фраксипарин), эноксапарин натрия (клексан). Средства влияют на активность Ха-фактора, вследствие чего подавляется образование тромбина, одного из главных компонентов свертывания крови. Преимуществом этих препаратов является то, что их можно использовать в амбулаторной практике с меньшей частотой контроля показателей свертывающей системы крови, по сравнению со стандартным гепарином. Низкомолекулярные гепарины вводятся внутривенно или подкожно ( в область живота) 1 -2 раза в сутки. Во внебольничных условиях эти препараты чаще всего используются для лечения и профилактики венозных тромбозов. Дозировки зависят от конкретного заболевания, вида препарата, сопутствующей патологии.
КОНТРОЛЬ – периодически по назначению врача определяется АЧТВ (может удлиняться), протромбин, количество тромбоцитов, Ха –фактор (выпускается специальный набор для его определения, анализ выполняется в крупных лабораториях).
ФОНДАПАРИНУКС НАТРИЯ
Препарат взаимодействует с антитромбином, в результате чего из процесса свертывания крови удаляется Ха – фактор. В амбулаторной практике фондапаринукс натрия (арикстра) в основном используется для профилактики и лечения тромбоза глубоких вен нижних конечностей. Назначается подкожно по 2,5 мг 1 раз в сутки.
КОНТРОЛЬ – периодически по назначению врача определяют АЧТВ, протромбин, количество тромбоцитов (но риск возникновения тромбоцитопемий низкий). При лечении фондапаринуксом натрия может повышаться АСТ и АЛТ. Установлено, что риск кровотечений при дозе 2,5 мг в сутки меньше, чем при использовании низкомолекулярных гепаринов (эноксипарина).
КСАРЕЛТО
амбулаторной практике ксарелто (ривароксабан) используется для профилактики тромбоза глубоких вен и профилактики инсульта и артериальных тромбоэмболий у больных с неклапанной мерцательной аритмией, после ортопедических операций. Препарат выпускается в таблетках по 10, 15 и 20 мг. В большинстве случаев дозировка составляет 10 мг в сутки.
КОНТРОЛЬ –периодически по назначению врача определяют протромбиновое время , АЧТВ, выполняют Hep Test ( выполняется с помощью специального лабораторного набора).
БЛОКАТОРЫ ГЛИКОПРОТЕИНОВЫХ РЕЦЕПТОРОВ ТРОМБОЦИТОВ
К препаратам этой группы относятся абциксимаб, руциромаб, тирофибан, эптифибатид. Механизм действия связан с блокированием рецепторов тромбоцитов. Используется в соцетании с ацитилcалициловой кислотой и плавиксом (или аналогами) в виде внутривенной инъекции при нестабильной стенкардии, чрез кожных, коронарных вмешательствах(ангиопластика, стентирование) у больных с повышенным риском тромботических осложнений, а также при инфаркте миокарда без стойких подъемов сегмента ST.
КОНТРОЛЬ – во время введения препарата контролируют содержание тромбоцитов, уровень гемоглобина,гематокрит. Рекомендуется, активно искать признаки кровотечений. Частота тромбоцитопений доходит до 5%. Кроме того, содержание тромбоцитов советуют определять перед введением препарата и через 4-6 и 12-24 часа. Риск кровотечений увеличен у женщин с весом менее 75 кг ,у больных возрасте старше 65 лет, с заболеваниями желудочно-кишечного тракта в анамнезе, при недавнем использовании антикоагу лянтов. Блокаторы рецепторов тромбоцитов в основном применяются в стационарных условиях.
Наш медцентр обеспечивает быстрое выполнение различных анализов (более 1000) с выездом специалиста на дом, медсестры на дом.
«Внутрисосудистое свертывание крови при COVID-19 определяет весь ход болезни»
 Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Сегодня известно, что при COVID-19, в первую очередь, страдает свертывающая система крови. Вот почему у всех умерших от осложнений новой коронавирусной инфекции находят большое количество тромбов. Как это объяснить? Почему это заметили не сразу? Каким образом и почему это происходит? Можно ли предотвратить развитие такого осложнения? Об этом – наш разговор с А.Д. Макацария, академиком РАН, одним из крупнейших в мире специалистов по изучению нарушений свертываемости крови, создателем Школы клинической гемостазиологии, заведующим кафедрой Сеченовского университета. Александр Давидович и его ученики активно сотрудничают с университетом Сорбонны, Венским, Римским, Миланским и Тель-Авивским университетами, Технион в Хайфе. Под его руководителем защищено 150 кандидатских и докторских диссертаций. Автор более 1200 научных трудов, в том числе 40 монографий.
– Александр Давидович, в последнее время во всем мире появляется всё больше сообщений о том, что при COVID-19 страдает свертывающая система крови. Так ли это, и если да, то чем вы объясняете этот феномен?
– Безусловно, это так. Более того, хочу сказать, что практически нет такой инфекции (вирусной или, тем более, бактериальной), которая бы не влияла на свертывание крови. Доказательство тому – учение о сепсисе и септическом шоке как универсальной модели ДВС-синдрома – синдрома диссеминированного внутрисосудистого свертывания крови. Степень тяжести тромботических нарушений зависит от особенностей возбудителя и организма-хозяина (иммунная система, система гемостаза, наличие сопутствующих заболеваний и т.д.).
– Но ведь не у всех пациентов развивается сепсис и септический шок?
– Конечно, не у всех. Поэтому очень актуальным и далеко не изученным в настоящее время является механизм патогенеза осложнений, вызванных коронавирусной инфекцией. Во многом это обусловлено особенностями вируса, а также особенностями организма человека, начиная от количества и качества рецепторов, представленных у человека и их способностью связываться с этим вирусом. Безусловно, на исходы заболевания огромное влияние оказывает коморбидность, то есть наличие сопутствующих хронических заболеваний у пациента.
– Почему, по вашему мнению, эта особенность течения болезни проявилась не сразу?
– Я считаю, что все это проявилось сразу, но не было адекватно оценено врачами изначально: еще не было такого количества вскрытий и широкого тестирования на гемостазиологические маркеры. Надо сказать, мы занимаемся изучением этой проблемы довольно давно, практически с самого начала эпидемии. Еще в самом начале апреля мы опубликовали работу, основанную на первых наблюдениях наших китайских коллег. Работа называлась «COVID-19 и синдром диссеминированного внутрисосудистого свертывания крови». Она имела чрезвычайно широкий резонанс, поскольку уже тогда врачи начали понимать роль свертывающей системы крови в инфекционном процессе.
– Каков механизм тромбообразования при covid-19 и отличается ли он от этого процесса при других патологиях?
– Это очень непростой вопрос. На сегодняшний день однозначно можно утверждать – при этом вирусе с самого начала имеет место активация гемостаза, внутрисосудистое свертывание крови и тромбообразование в сосудах мелкого калибра жизненно важных органов. При этом повреждаются не только легкие, а блокада микроциркуляции и ее необратимый характер определяют исход заболевания. Позднее начало антикоагулянтной терапии является неблагоприятным фактором. Причем этот процесс внутрисосудистого свертывания в капиллярах легкого играет важную роль в развитии острого респираторного дистресс-синдрома (ОРДС), о котором все говорят. Но далеко не все с самого начала уловили связь между внутрисосудистым свертыванием крови и ОРДС.
В западной литературе даже появился термин «легочная интраваскулярная коагуляция». Практически во всех случаях имеет место активация системного воспалительного ответа. Это общебиологическая реакция, которая особенно проявляется в ответ на инфекцию, вирусные возбудители. Международные организации признали, что коронавирусная инфекция – это сепсис.
С другой стороны, международная организация по тромбозу и гемостазу в абсолютном числе случаев признала наличие ДВС-синдрома у тяжелых больных с COVID-19 . Сочетание сепсиса и коагулопатии – это септический шок. Еще китайские коллеги указывали, что в 92% случаев больные умирают от септического шока. Конечно, нельзя отрицать, что наряду с вирусом причиной септического шока может быть присоединение вторичной бактериальной инфекции. У больных COVID-19 и нарушениями в системе гемостаза, как правило, имеет место гиперферритинемия, которая возникает при критических состояниях как реактант острой фазы воспаления и характеризуется цитокиновым штормом вследствие гиперактивации макрофагов и моноцитов. Вследствие этого вырабатывается большое количество ферритина – сложного белкового комплекса, выполняющего роль основного внутриклеточного депо железа у человека и животных. В данном случае это всегда белок острой фазы, маркер тяжелого воспаления, а вовсе не показатель перегрузки железом, как можно подумать на первый взгляд.
Таким образом, цитокиновый и тромботический шторм усугубляют состояние больного и определяют степень тяжести. Но есть и особенности. Возможно, при COVID-19 в первую очередь повреждается фибринолиз – часть системы гемостаза, которая обеспечивает процесс разрушения уже сформированных кровяных сгустков, тем самым, выполняя защитную функцию предотвращения закупорки кровеносных сосудов фибриновыми сгустками. Отсюда синдром фибринирования при меньшей частоте геморрагических осложнений. И отсюда же открывается перспектива применения тромболитиков, о чем сейчас так много говорят и пишут. А впервые предложили такую схему наши американские коллеги.
– А ведь есть немало людей с нарушениями свертываемости крови. Сейчас, во время эпидемии, для них настали трудные времена.
– Это так. В нашей популяции есть люди не только с явными, но и со скрытыми нарушениями гемостаза, предрасполагающими к тромбозам – генетические тромбофилии, антифосфолипидный синдром и ряд других заболеваний, сопровождающихся избыточной активацией системы гемостаза; а также люди с высокой готовностью к супервоспалительному ответу (врожденные факторы и ряд ревматологических и иммунных заболеваний). Им сейчас важно контролировать своё состояние, а врачам не забывать об этом.
И, наконец, COVID-19 – это тромбовоспаление. Это, по сути, вирус-опосредованная модель NET-оза, которая характеризует тесную взаимосвязь таких биологических процессов, как воспаление и тромбообразование. Нейтрофилы и выделяемые ими внеклеточные ловушки нейтрофилов (NET) играют огромную роль в развитии так называемых иммунотромбозов. Это одно из приоритетных научных направлений сегодня , которое мы сейчас вместе с учениками и в том числе зарубежными коллегами также разрабатываем.
Вообще надо сказать, что открытие NET расширило горизонты в понимании биологии нейтрофилов и роли этих клеток в организме. Использование организмом хозяина хроматина в сочетании с внутриклеточными белками в качестве естественного противомикробного агента имеет древнюю историю и меняет наше представление о хроматине как только о носителе генетической информации. Благодаря избыточному и неконтролируемому формированию NET, нейтрофилы могут способствовать развитию патологического венозного и артериального тромбоза, или «иммунотромбоза», а также играют важную роль в процессах атеротромбоза и атеросклероза. Высвобождение NET является, как выяснилось, одной из причин тромбообразования при таких состояниях, как сепсис и рак. Наличие NET при этих заболеваниях и состояниях дает возможность использовать их или отдельные компоненты в качестве потенциальных биомаркеров. NET и их компоненты могут быть привлекательны в качестве терапевтических мишеней. Дальнейшие исследования нейтрофилов и NET необходимы для разработки новых подходов к диагностике и лечению воспалительных и тромботических состояний.
– Размышляя о высокой летальности у пациентов, которым пришлось применить ИВЛ, вы констатируете, что мы, возможно, пошли не тем путем. А какой путь может оказаться более верным?
– Да, я имел в виду, что при оценке вентиляционно-перфузионных нарушений при COVID-19 превалируют перфузионные нарушения, нарушения микроциркуляции, а это значит, что главная терапевтическая мишень – восстановление нормальной перфузии тканей, то есть противотромботическая терапия, а возможно, даже и фибринолитическая. Механическая вентиляция не может решить вопрос перфузионных нарушений.
– Видите ли вы, что в связи с эпидемией стали более частыми проблемы тромбообразования в акушерско-гинекологической практике?
– Случилось так, что во многом и благодаря нашим стараниям (лекциям и публикациям), большинство акушеров сегодня осведомлены о том, что беременность – это состояние так называемой физиологической гиперкоагуляции, и этим пациенткам нередко назначаются антикоагулянты во время беременности. Тем не менее, требуются дальнейшие исследования для вынесения суждения о частоте тромбозов у беременных с COVID-19.
Вообще надо сказать, что большинство осложнений беременности либо обусловлены, либо сочетаются с высоким тромбогенным потенциалом. Генетические факторы свертывания крови, особенно антифосфолипидный синдром, являются факторами риска огромного количества осложнений беременности – это и внутриутробные гибели плода, и неудачи ЭКО, и задержка внутриутробного развития плода, и преждевременная отслойка плаценты, что приводит к тяжелым тромбогеморрагическим осложнениям, это, наконец, тромбозы и тромбоэмболии. Поэтому, конечно, можно ожидать, что в условиях COVID-19 эти осложнения могут представлять собой еще большую опасность. Ведь вирус может быть фактором, активирующим факторы свертываемости крови. Конечно, тут нужны обобщающие исследования, но уже сейчас наши отдельные наблюдения говорят о том, что риск таких осложнений возрастает.
– Являются ли, на ваш взгляд, одним из проявлений этой проблемы случаи тяжелого течения covid-19 в педиатрии (состояния, похожие на синдром Кавасаки)?
– Глава ВОЗ Тедрос Аданом Гебрейесус призвал врачей всех стран обратить особое внимание на сообщения о том, что у некоторых детей, заразившихся коронавирусом, проявляются симптомы, схожие с еще одним заболеванием — синдромом Кавасаки (мультисистемным воспалительным синдромом). Действительно, в сообщениях из Европы и Северной Америки говорилось, что некоторое число детей поступало в отделения интенсивной терапии с мультисистемным воспалительным состоянием, с некоторыми симптомами, похожими на синдром Кавасаки и синдром токсического шока.
Синдром Кавасаки был впервые описан в 1967 году японским педиатром по имени Томисаку Кавасаки. Он обычно поражает детей до пяти лет. При этом синдроме у пациента начинается воспаление кровеносных сосудов (васкулит) и лихорадка. Болезнь Кавасаки имеет четко выраженный набор симптомов, включая постоянно высокую температуру, покраснение глаз и области вокруг рта, сыпь на теле и покраснение и отек ног и рук.
13 мая нынешнего года в авторитетном медицинском издании The Lancet было опубликовано исследование итальянских врачей, которые сообщили, что в провинции Бергамо, одной из наиболее пострадавших от эпидемии коронавируса, была зафиксирована вспышка синдрома Кавасаки или схожего с ним синдрома.
Важно, что в большинстве случаев дети также имели положительный результат теста на антитела к КОВИД-19, предполагая, что синдром последовал за вирусной инфекцией.
Болезнь Кавасаки имеет тенденцию проявляться в группах генетически похожих детей и может выглядеть немного по-разному в зависимости от генетики, лежащей в основе группы. Это говорит о том, что различные триггеры могут вызывать воспалительную реакцию у детей с определенной генетической предрасположенностью.
Вполне возможно, что атипичная пневмония SARS-COV-2, вызванная вирусом COVID-19, является одним из таких триггеров. Это важный вопрос, требующий пристального изучения.
– Александр Давидович, как вы думаете, почему у всех COVID-19 проявляется по-разному?
– Тут очень важна проблема факторов риска. Всё дело в том, что, помимо видимых болезней типа сахарного диабета или гипертонии, существуют болезни невидимые, о которых мы зачастую даже не подозреваем. В последние годы большое распространение получило учение о генетической тромбофилии. Во всем мире это примерно до 20 процентов людей, которые являются носителями той или иной формы генетической тромбофилии. С этим можно жить сто лет, но если возникает инфекция, травма, делается операция – больной может погибнуть от тромбоэмболии, даже если операция выполнена на высочайшем техническом уровне. Причиной тому – скрытая генетическая тромбофилия – мутация, которая делает её носителя подверженным высокому риску тромбообразования.
Одна из форм тромбофилии – так называемая гипергомоцистеинемия, которая может быть как приобретенной так и генетически обусловленной, также может быть важным фактором тромбозов, инфарктов, инсультов. А сейчас есть данные о том, что гипергомоцистеинемия усугубляется и при SARS-CoV2 инфекции. Соответственно, в группу риска входят все те, у кого повышен уровень гомоцистеина в крови , но человек может не знать об этом. Поэтому мы сейчас начали масштабное исследование по выявлению этих групп риска, выделению различных форм тромбофилии у больных с COVID-19. Наша цель – узнать, входят ли эти люди в группы риска по развитию тяжелых осложнений новой коронавирусной инфекции.
Высокая контагиозность вируса и большое количество заболевших поневоле «позволяет» вирусу выявить людей с изначальной явной или скрытой предрасположенностью к тромбозам. Это пациенты не только с генетической тромбофилией или антифосфолипидным синдромом, но и с сахарным диабетом, ожирением, ревматическими болезнями и другими патологическими состояниями, ассоциированными с повышенным свертыванием и/или воспалением.
– Какие методы профилактики и лечения covid-19 вы считаете перспективными?
– Помимо уже названных, это противовирусная терапия, терапия специфическими иммуноглобулинами, противотромботическая терапия и лечение, направленное на снижение воспаления (так называемые антицитокиновые препараты). Многое нам предстоит ещё понять об этом новом для нас заболевании, но постепенно мы движемся в сторону лучшего объяснения многих его механизмов. Вы знаете, я всегда много работал, но, пожалуй, никогда ещё я не был так занят исследовательской и практической работой, как сейчас. Уверен, что она даст свои важные результаты.
Беседу вела Наталия Лескова.
КОВИД. Тромбы. Антикоагулянты
Кому нужны антикоагулянты, когда и в каких дозах?
 Коронавирус повышает тромбообразование. Тромбоз глубоких вен и тромбоэмболия легочных артерий очень часто встречается среди тяжелобольных людей с КОВИД. В связи с этим, антикоагулянты стали частью лечение пациентов с коронавирусной инфекцией.
Коронавирус повышает тромбообразование. Тромбоз глубоких вен и тромбоэмболия легочных артерий очень часто встречается среди тяжелобольных людей с КОВИД. В связи с этим, антикоагулянты стали частью лечение пациентов с коронавирусной инфекцией.
Какой риск тромбоза у пациента с КОВИД?
Риски у реанимационных пациентов
Среди реанимационных пациентов частота тромбозов доходит до 30%, даже при использовании профилактических доз антикоагулянтов 1 .
В исследованиях, где всем пациентам делали УЗИ глубоких вен, тромбоз был обнаружен у 65-69% пациентов 2,3 !
Во многих исследованиях, у пациентов с тромбозом был выше Индекс Массы Тела, что указывает на то, что лишний вес и ожирение может повышать риск тромбообразования при КОВИД.
Риски у госпитализированных пациентов
Среди госпитализированных пациентов, которые не нуждались в реанимации, тромбоэмболия обнаруживается примерно у 3-6% 4,5 . У некоторых пациентов, тромбы были диагностированы в первые 24 часа госпитализации.
В исследованиях, где всем пациентам делали УЗИ глубоких вен, тромбоз обнаруживается чаще, в 12-21% случаев 6,7 .
Анализ 3000 госпитализированных пациентов, принимающих профилактические дозы антикоагулянтов, выявил дополнительные факторы риска тромбоза 8 :
- Возраст и мужской пол
- Сердечно-сосудистые заболевания
- Перенесенный инфаркт миокарда
- Д-димер > 500 нг/мл
Тромбоз повышает риск смерти на 37%. 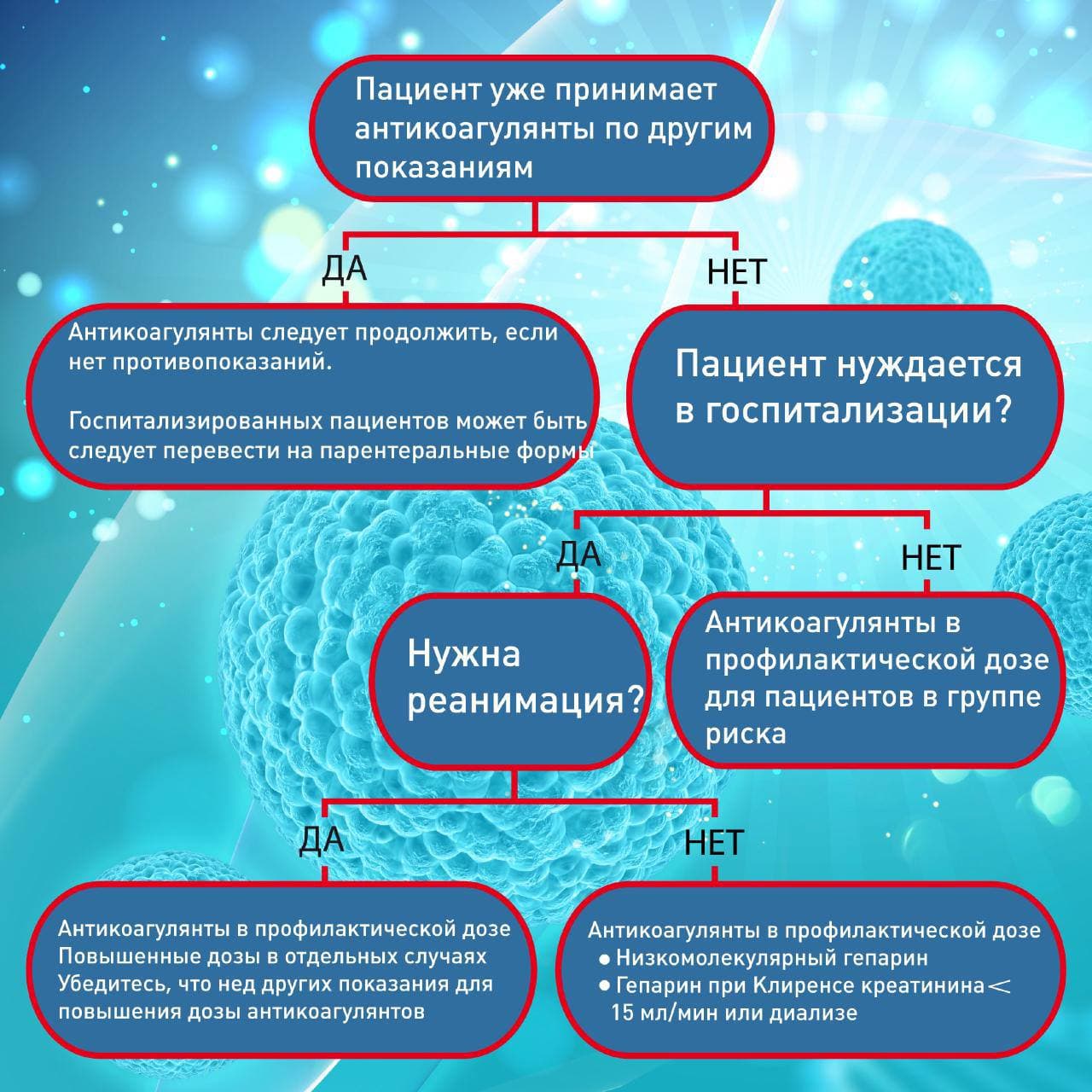
Какие анализы и обследования нужны госпитализированным пациентам?
Это нужно проверить у всех госпитализированных пациентов 9
- Общий анализ крови
- Коагуляция: МНО, Протромбиновое время
- Фибриноген
- Д-димер
- УЗИ глубоких вен при подозрение на тромбоз глубоких вен
- КТ ангиография легочных артерий при подозрение на тромбоэмболию легочной артерии
Только результаты анализов не должны быть причиной начала или прекращения антикоагулянтов, при отсутствии клинических показаний. Например, повышенный Д-димер не специфичен для тромбоэмболии, поэтому не может диагностировать ее.
Кому нужны антикоагулянты, в каких дозах и как долго?
Все госпитализированные пациенты должны получать профилактическую дозу антикоагулянтов. Как правило, применяются подкожные инъекции.
Профилактические дозы
- Эноксапарин 40 мг один раз в день (при клиренсе креатинина > 30 мл/мин)
- Эноксапарин 30 мг один раз в день (при клиренсе креатинина > 15-30 мл/мин)
- Гепарин 5000 Ед каждый 8-12 часов (при клиренсе креатинина 10 и пациентов с очень высоким Д-димером, в 6 раз выше верхней границы нормы 11 .
Как уже было сказано выше, у многих реанимационных пациентов развиваются тромбы, несмотря на профилактическую дозу антикоагулянтов. В связи с этим, многие эксперты рекомендуют повышенные дозы антикоагулянтов в реанимации.
Кому нужна терапевтическая доза антикоагулянтов?
- Если пациент уже принимает антикоагулянты по другим показаниям (мерцательная аритмия, тромбоз и т.д.), то их нужно продолжить. На время госпитализации, может быть следует перейти на инъекции
- Новый диагноз тромбоза глубоких вен или тромбоэмболия легочных артерий
- Тромбоз катетеров несмотря на профилактические дозы антикоагулянтов
Решение начать полную дозу антикоагулянтов должно быть взвешенным. Отдельные изменения в анализах, как например повышение Д-димера, не может быть единственной причиной повышение дозы антикоагулянта.
Терапевтические дозы
- Эноксапарин 1 мг/кг два раза в день
- Гепарин в/в под контролем протромбинового времени
- Апиксабан 5 мг два раза в день
- Ривароксабан 20 мг один раз в день
Нужно ли назначать терапевтические дозы антикоагулянтов тяжелым пациентам или пациентам в реанимации, у которых нет признаков тромбоэмболии?
На данный момент точного ответа нет. Результаты исследований противоречивы: в одном исследование терапевтические дозы антикоагулянтов повышают 12 смертность, в другом – понижают 13 , в третьем – никак не влияют 14 . Чтобы понять нужны ли терапевтические дозы антикоагулянтов тяжелым больным с КОВИД, необходимы рандомизированные исследования.
Поэтому, эмпирическое назначение терапевтических доз антикоагулянтов остается противоречивым. Если у пациента подозревается тромбоз, рекомендуется провести соответствующие обследования или искать другие причины для повышение дозы антикоагулянтов.
Кому нужно продолжать антикоагулянты после выписки из больницы?
Пациентам с диагностированным тромбозом необходимо минимум три месяца антикоагулянта в терапевтической дозе.
Риск тромбоза у выписанных пациентов незначительно повышен 15 . Но антикоагулянты в профилактической дозе после выписки из больницы рекомендуются людям в группе риска, если нет опасности кровотечения 16 :
- Предыдущий тромбоз
- Недавняя операция или травма
- Иммобилизация
- Ожирение
В таком случае антикоагулянты в профилактической дозе назначаются на 31-39 дней.
Нужны ли антикоагулянты не госпитализированным пациентам?
Большинство не госпитализированных пациентов не нуждается в антикоагулянтах. Но антикоагулянты могут быть назначены пациентам в группе риска (предыдущий тромбоз, недавняя операция или травма, иммобилизация, ожирение). В таком случае, антикоагулянты в профилактической дозе назначаются на 31-39 дней.
Антиагреганты и КОВИД
В данный момент идут исследования роли антиагрегантов при КОВИД. На данный момент нет данных для их назначения пациентам исключительно из-за КОВИД. Однако, если пациент принимает препараты из этой группы, то их можно продолжить принимать по стандартным показанием
- Incidence of thrombotic complications in critically ill ICU patients with COVID-19, Klok et al., Thromb Res. 2020;191:145. Epub 2020 Apr 10
- Venous Thrombosis Among Critically Ill Patients With Coronavirus Disease 2019 (COVID-19)., Nahum et al., JAMA Netw Open. 2020;3(5):e2010478. Epub 2020 May 1.
- High incidence of venous thromboembolic events in anticoagulated severe COVID-19 patients., Llitjos et al., J Thromb Haemost. 2020;18(7):1743. Epub 2020 May 27.
- Incidence of venous thromboembolism in hospitalized patients with COVID-19., Middeldorp et al., J Thromb Haemost. 2020;18(8):1995. Epub 2020 Jul 27.
- Venous and arterial thromboembolic complications in COVID-19 patients admitted to an academic hospital in Milan, Italy.. Lodigianin et al., Thromb Res. 2020;191:9. Epub 2020 Apr 23.
- Systematic assessment of venous thromboembolism in COVID-19 patients receiving thromboprophylaxis: incidence and role of D-dimer as predictive factors., Artifoni et al., J Thromb Thrombolysis. 2020;50(1):211.
- Incidence of deep vein thrombosis among non-ICU patients hospitalized for COVID-19 despite pharmacological thromboprophylaxis., Santoliquido et al., J Thromb Haemost. 2020;18(9):2358. Epub 2020 Aug 27.
- Thrombosis in Hospitalized Patients With COVID-19 in a New York City Health System. Bilalogly et al., JAMA. 2020;324(8):799
- ISTH interim guidance to recognition and management of coagulopathy in COVID-19., Akima et al., J Thromb Haemost. 2020;18(8):2057. Epub 2020 Jul 15.
- Association of Treatment Dose Anticoagulation With In-Hospital Survival Among Hospitalized Patients With COVID-19., Paranhpe et al., J Am Coll Cardiol. 2020;76(1):122. Epub 2020 May 6.
- Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy., Tang et al., J Thromb Haemost. 2020;18(5):1094. Epub 2020 Apr 27.
- Clinical Outcomes With the Use of Prophylactic Versus Therapeutic Anticoagulation in Coronavirus Disease 2019., Motta et al., Crit Care Explor. 2020;2(12):e0309. Epub 2020 Dec 16.
- Therapeutic Anticoagulation Is Associated with Decreased Mortality in Mechanically Ventilated COVID-19 Patients., Muoi et al
- Thrombosis, Bleeding, and the Observational Effect of Early Therapeutic Anticoagulation on Survival in Critically Ill Patients With COVID-19., Al-Samkari H et al., Ann Intern Med. 2021
- Postdischarge venous thromboembolism following hospital admission with COVID-19., Roberts et al., Blood. 2020;136(11):1347.
- COVID-19 and Thrombotic or Thromboembolic Disease: Implications for Prevention, Antithrombotic Therapy, and Follow-Up: JACC State-of-the-Art Review., Bikdeli et al., J Am Coll Cardiol. 2020;75(23):2950. Epub 2020 Apr 17.

 Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
