По каким параметрам классифицируются?
Сердечные пороки подразделяются по следующим параметрам:
- По времени возникновения (врожденные, приобретенные);
- По этиологии (вследствие хромосомных аномалий, вследствие заболеваний, неясной этиологии);
- По расположению аномалии (перегородочные, клапанные, сосудистые);
- По количеству пораженных структур;
- По особенностям гемодинамики (с цианозом, без цианоза);
- По отношению к кругам кровообращения;
- По фазе (фаза адаптации, фаза компенсации, терминальная фаза);
- По типу шунта (простые с лево-правым шунтом, простые с право-левым шунтом, сложные, обструктивные);
- По типу (стеноз, коарктация, обструкция, атрезия, дефект (отверстие), гипоплазия);
- По влиянию на скорость кровотока (незначительное, умеренное, выраженное влияние).
Клиническое разделение пороков на белые и синие основано на преобладающих внешних проявлениях болезни. Данная классификация является в некоторой степени условной, поскольку большинство пороков одновременно относятся к обеим группам.
Успех лечения и профилактика
Ранняя диагностика и тщательное следование рекомендаций детских кардиохирургов значительно улучшают прогноз при ВПС, однако далеко не во всех случаях. Основным показателем, позволяющим делать какие-либо предположения, выступает вид порока и его тяжесть. Если ребенок доживает до 2–3 лет, шансы на выздоровление или улучшение состояния существенно возрастают. Смертность в таком случае составляет около 5% от общего количества больных. Уходом за детьми занимаются родители в домашних условиях или же медперсонал кардиологических отделений.
Учитывая, что распространенными провоцирующими факторами ВПС выступают генетические нарушения, женщинам рекомендуется внимательно относится к беременности и по возможности готовиться к ней заранее. Особенно это касается семейных пар из групп риска.
До планируемого зачатия обоим партнерам нужно:
- сдать необходимые анализы;
- вылечить сопутствующие заболевания;
- отказаться от вредных привычек;
- пропить витаминные комплексы.
После наступления беременности нужно как можно раньше встать на учет в женской консультации, регулярно посещать гинеколога и проходить обследование. Особое внимание стоит уделить генетическим скринингам, которые делаются в каждом триместре.
Ранее всем детям с ВПС рекомендовали полный отказ от физических нагрузок. Сейчас вести обычную двигательную активность разрешено малышам, которые:
- прошли хирургическую коррекцию нарушения;
- не имеют одышки, тахикардии, повышенного АД и других негативных симптомов.
Таким детям не повредит спортивная ходьба и плаванье, а вот профессиональный спорт при ВПС – табу, независимо от самочувствия.
Нужен ли будет специальный уход за детьми с ВПС, будет зависеть от типа дефекта и результата лечения.

Интенсивные потуги или продолжительный безводный период также вредны для малыша, поэтому способ родоразрешения выбирают с учетом типа ВПС у плода, течения беременности, состояния матери и прочих обстоятельств.
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Классификация врожденных пороков сердца



СЕСТРИНСКИЙ ПРОЦЕСС ПРИ
ЗАБОЛЕВАНИЯХ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ У ДЕТЕЙ
ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА (ВПС)
Частота врожденных пороков сердца среди новорожденных, по данным ВОЗ, составляет 0,8-1%.
В России ежегодно рождается с врожденными пороками сердца около 20.000-25.000 детей.
Сердечно-сосудистая система начинает функционировать первой, уже приблизительно через 21 день после зачатия, благодаря сокращению сердца, у эмбриона начинает циркулировать кровь. В результате воздействия тех или иных факторов риска, происходит нарушение процесса нормального эмбриогенеза со 2-й по 8-ю недели беременности, что может привести к формированию изолированного или комбинированного порока сердца.
Факторы риска развития врожденных пороков сердца:
Ø наследственная предрасположенность, хромосомные аберрации;
Ø вирусные инфекции в первые три месяца беременности (краснуха, корь, грипп, ветряная оспа, паротитная инфекция);
Ø профессиональные вредности матери;
Ø воздействие тератогенных факторов (лекарственных средств, радиации, химических веществ и др.).
Существует большое разнообразие анатомических вариантов врожденных пороков сердца.
Нарушение процессов эмбриогенеза, приводящих к формированию врожденных пороков сердца
| Возраст плода | Закладка сердечнососудистой системы | Врожденные пороки развития |
| 3 недели | Легочные вены | Аномалии легочных вен |
| 4-6 недель | Межпредсердная перегородка | Дефект межпредсердной перегородки (ДМПП) |
| 4-8 недель | Межжелудочковая перегородка | Дефект межжелудочковой перегородки (ДМЖП) |
| 5-7 недель | Легочная артерия, аорта | Тетрада Фалло, изолированный стеноз легочной артерии, транспозиция аорты |
Врожденные пороки сердца у детей могут проявляться сразу после рождения или через некоторое время.
Выделяют IV группы ВПС, учитывая состояние гемодинамики в малом и большом кругах кровообращения, отсутствие или наличие цианоза и дефекты развития сердечнососудистой системы.
Классификация врожденных пороков сердца
| Нарушение гемодинамики | Без цианоза | С цианозом |
| С обогащением малого круга кровообращения | Открытый артериальный (Боталлов) проток (ОАП), дефекты межпредсердной и межжелудочковой перегородок (ДМПП, ДМЖП) | Транспозиция магистральных сосудов, общий артериальный ствол |
| С обеднением малого круга кровообращения | Изолированный стеноз легочной артерии | Тетрада Фалло, атрезия трехстворчатого клапана |
| С обеднением большого круга кровообраще-ния | Изолированный аортальный стеноз, коарктация аорты | |
| Без нарушения гемодинамики | Аномалии положения дуги аорты и ее ветвей, небольшой дефект межжелудочковой перегородки |
Клиническая картина врожденных пороков сердца разнообразна и определяется величиной анатомических дефектов, степенью нарушения гемодинамики, адаптационно-компенсаторными механизмами и характером осложнений.
Некоторые ВПС у новорожденных и детей раннего возраста могут иметь скудные клинические проявления и для их распознавания требуются дополнительные методы исследования.
В клинической картине ВПС необходимо учитывать фазовость течения заболевания:
1 фаза– первичной адаптации, в эту фазу происходит приспособление организма к нарушениям гемодинамики.
Адаптационно-компенсаторные механизмы у новорожденных и детей раннего возраста неустойчивы. При небольших изменениях гемодинамики клинические проявления, как правило, скудные, а при значительных, может быстро развиться декомпенсация, так называемый «аварийный вариант» (по В.В. Парину и Ф.З. Меерсону).
2 фаза – относительной компенсации, если дети с ВПС
не гибнут в первой фазе болезни, то постепенно наступает улучшение гемодинамики, состояния и развития ребенка.
3 фаза – необратимой декомпенсации (терминальная). Наступление этой фазы связано с усугублением нарушений гемодинамики, приводящих к дистрофическим изменениям сердечной мышцы и истощению компенсаторных возможностей организма. Присоединение интеркуррентных заболеваний и различных осложнений ускоряет развитие этой фазы. Достижения современ-ной кардиохирургии позволяют уменьшить количество детей, достигаю-щих 3 фазы заболевания.
Основные клинические проявления ВПС:
Ø повышенная утомляемость, снижение выносливости к физическим нагрузкам;
Ø бледность кожных покровов при пороках без цианоза (бледные пороки) или выраженный цианоз кожных покровов при пороках с цианозом (синие пороки);
Ø одышка, усиливающаяся при физической нагрузке (при напряжении, сосании, плаче), а затем возникающая и в покое, возможны приступы удушья;
Ø тахикардия до 200 ударов в минуту; видимая систолическая пульсация во II—IIIмежреберье у левого края грудины, сердечные шумы (чаще грубый систолический шум, проводящийся на крупные сосуды), симптом «кошачье мурлыканье», определяющийся пальпаторно у левого края грудины, позже появляется выпячивание грудной клетки в области сердца («сердечный горб»);
Ø отставание весоростовых показателей и психомоторного развития;
Ø частые ОРВИ и воспалительные заболевания органов дыхания;
Ø во второй фазе выявляется симптом «барабанных палочек» – утолщение концевых фаланг пальцев рук и ног, ногти приобретают форму часовых стекол.
Адаптационно-компенсаторные механизмы у новорожденных и детей раннего возраста неустойчивы. При небольших изменениях гемодинамики клинические проявления, как правило, скудные, а при значительных, может быстро развиться декомпенсация, так называемый «аварийный вариант» (по В.В. Парину и Ф.З. Меерсону).
Виды врожденных пороков сердца: тип смешения крови
Классификация врожденных сердечных аномалий на виды затруднительна, поскольку каждый исследователь предлагает свой признак, на основе которого стоит делить ВПС на виды. Самая распространенная классификация создана на основе факторов перемешивания разных типов крови – венозной и артериальной, степени проявления признаков патологии и выраженности изменений в гемодинамике.
«Бледные» врожденные пороки сердца характеризуются отсутствием смешивания разных типов крови и ее сбросом из большого в малый круг кровообращения. Эта группа ВПС получила такое название из-за того, что у больных очень бледная кожа. Делится она на 4 подвида – некоторые из них встречаются чаще, остальные – очень редкие:
- Врожденные пороки с насыщением легочного круга (дефекты перегородок между сердечными желудочками и предсердиями, незарастающий артериальный проток).
- С “обкрадыванием” кровоснабжения легких (стеноз легочных артерий изолированного типа).
- С “обкрадыванием” в большом круге кровообращения (стеноз аорты и коарктация).
- Без характерных изменений в циркуляции крови (аномалии в расположении сердца).
«Синюшные» врожденные пороки сердца характеризуются перемешиванием разных видов крови и выбросом крови по направлению справа налево. Внешне это проявляется в цианозе, или синюшной окраске кожных покровов. Данная разновидность патологии является наиболее опасной, поскольку сопровождаются ухудшением кислородного насыщения крови. В этой группе выделяют 2 подвида:
- Врожденные пороки с насыщением круга кровообращения в легких (смещение магистральных сосудов, порок Эйзенменгера).
- С “обкрадыванием” кровоснабжения легких (заболевание тетрада Фалло, аномалия Эбштейна, атрезия трикуспидального типа).
- Врожденные пороки с насыщением легочного круга (дефекты перегородок между сердечными желудочками и предсердиями, незарастающий артериальный проток).
- С “обкрадыванием” кровоснабжения легких (стеноз легочных артерий изолированного типа).
- С “обкрадыванием” в большом круге кровообращения (стеноз аорты и коарктация).
- Без характерных изменений в циркуляции крови (аномалии в расположении сердца).
Недостаточность правого атриовентрикулярного (трехстворчатого) клапана
Недостаточность трехстворчатого клапана часто носит функциональный характер и связана лишь с первичным расширением правого желудочка и обусловленным этим растяжением кольца правого атриовентрикулярного клапана.
Однако при выраженной перегрузке правого предсердия развивается застой в большом круге кровообращения, сопровождающийся общими отеками и другими явлениями, характерными для правожелудочковой сердечной недостаточности.
Наиболее частой причиной стеноза клапанного отверстия при данном виде порока сердца служит выраженный атеросклероз. При этом резко увеличивается постнагрузка, обусловленная повышенным сопротивлением сердечному выбросу. В результате возникает выраженная гемодинамическая перегрузка левого желудочка, приводящая к развитию сначала его гипертрофии, а затем левожелудочковой сердечной недостаточности.
Основные проявления
Патофизиология врожденных пороков сердца в большей степени заключается в нарушении нормального кровообращения. Чаще всего этому способствует:
- Повышение сопротивления току крови, приводящее к гипертрофии соответствующего сердечного отдела.
- Создание порочного сообщения между обоими кругами кровообращения.
Очень часто оба этих патогенетических механизма могут комбинироваться. В связи с этим можно выделить следующие признаки пороков сердца:
- Одышка.
- Патологические шумы.
- Обморочные состояния.
- Цианоз.
- Сердцебиение.
- Нарушение ритма.
- Периферические отеки на ногах.
- Асцит (скопление жидкости в брюшной полости).
- Гидроторакс (скопление жидкости в плевральной полости).
Стоит заметить, что компенсированные пороки чаще всего протекают бессимптомно и выявляются при проведении профилактического осмотра. Основные симптомы пороков сердца проявляются тогда, когда организм уже не может своими силами справляться с нарушениями гемодинамики.
- Электрокардиография. Электрокардиограмма поможет выявить изменения в работе сердца. ЭКГ при пороках сердца не играет большой роли и чаще всего помогает выявить последствия заболевания.
- Эхокардиография. Это ультразвуковая диагностика, предназначенная для тщательного изучения функциональных и морфологических особенностей сердца.
- Фонокардиография – методика, позволяющая отобразить тоны сердца в графическом виде.
- Рентген. Позволяет выявить конфигурацию сердца, а также обнаружить транспозицию сосудов.
Врожденные пороки сердца
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
НЦССХ имени А.Н. Бакулева РАМН, Москва
В рожденные пороки сердца (ВПС) — достаточно распространенная патология среди заболеваний сердечно-сосудистой системы, которая является основной причиной смерти детей первого года жизни. Частота ВПС составляет 30% от всех пороков развития. Лечение врожденных сердечных аномалий возможно только хирургическим путем. Благодаря успехам кардиохирургии стали возможны сложные реконструктивные операции при ранее неоперабельных ВПС. В этих уcловиях основной задачей в организации помощи детям с ВПС является своевременная диагностика и оказание квалифицированной помощи в хирургической клинике.
Основными причинами рождения детей с ВПС являются: хромосомные нарушения – 5%; мутация 1-го гена – 2–3%; влияние внешних факторов (алкоголизм родителей, прием лекарственных препаратов, перенесенные вирусные инфекции во время беременности и т.д.) – 1–2% ;полигенно-мультифокальное наследование – 90%.
Помимо этиологических выделяют факторы риска рождения ребенка с ВПС. К ним относятся: возраст матери, эндокринные заболевания супругов, токсикоз и угроза прерывания I триместра беременности, мертворожденные в анамнезе, наличие детей с врожденными пороками развития у ближайших родственников. Количественно оценить риск рождения ребенка с ВПС в семье может только генетик, но дать предварительный прогноз и направить родителей на медико-биологическую консультацию может каждый врач.
Классификация
Встречается более 90 вариантов ВПС и множество их сочетаний. В Институте сердечно-сосудистой хирургии им. А.Н. Бакулева АМН СССР была разработана классификация, основанная на распределении ВПС с учетом анатомических особенностей порока и гемодинамических нарушений.
Для практикующих врачей-кардиологов удобнее пользоваться более упрощенным делением ВПС на 3 группы:
1. ВПС бледного типа с артериовенозным шунтом: дефект межжелудочковой перегородки (ДМЖП), дефект межпредсердной перегородки (ДМПП), открытый артериальный проток (ОАП); открытый атриовентрикулярный канал (АВК).
2. ВПС синего типа с веноартериальным шунтом: транспозиция магистральных сосудов (ТМС), тетрада Фалло (ТФ), триада Фалло, атрезия трикуспидального клапана (АТК) и т.д.
3. ВПС без сброса, но с препятствием на пути кровотока из желудочков (стенозы легочной артерии и аорты). Такое деление охватывает 9 наиболее распространенных ВПС.
Нарушение гемодинамики при врожденных пороках сердца
Не случайно во всех предложенных классификациях большое внимание уделено оценке нарушений гемодинамики при ВПС, так как степень этих нарушений тесно связана с анатомической тяжестью порока, от них зависит тактика медикаментозного лечения и сроки выполнения операции.
ВПС вызывает ряд изменений компенсаторного характера, которые заставляют перестраиваться весь организм ребенка, но при длительном существовании порока процессы компенсации ведут к выраженным деструктивным изменениям органов и систем, что приводит к гибели больного.
В зависимости от состояния малого круга кровообращения в организме больного с ВПС наблюдаются следующие патологические изменения:
• при наличии увеличенного кровотока в легких (пороки бледного типа с артериовенозным шунтом) развивается гиперволемия и гипертензия малого круга кровообращения;
• при наличии обедненного кровотока в легких (пороки синего типа с веноартериальным шунтом) у больного развивается гипоксемия;
• при увеличении кровотока в малом круге кровообращения развивается гиперволемия и легочная гипертензия.
Примерно 50% детей первого года жизни с большим сбросом крови в малый круг кровообращения без хирургической помощи погибают при явлениях сердечной недостаточности. Если ребенок переживает этот критический период, то к году в результате спазма легочных артериол уменьшается сброс крови в малый круг и состояние ребенка стабилизируется, однако это улучшение касается только самочувствия больного, так как одновременно начинают развиваться склеротические процессы в сосудах легких. Существует много классификаций легочной гипертензии. Для практики наиболее удобной является классификация, разработанная в ИССХ им. А. Н. Бакулева АМН СССР (В.И. Бураковский и соавт., 1975). Она основана на величине давления в легочной артерии, степени сброса крови и соотношении общелегочного сопротивления к показателям большого круга кровообращения (табл. 1).
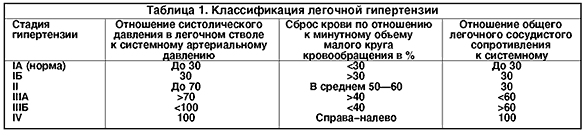
Согласно этой классификации, больные делятся на 4 группы, где I и III стадия разделены на подгруппы А и Б. Больные IА группы имеют небольшие нарушения гемодинамики и нуждаются в наблюдении кардиолога. У больных IБ и II группы ставится вопрос об операции. Легочная гипертензия в этих группах носит функциональный характер.
У больных III группы при большом сбросе крови в малый круг изменения в легочных сосудах значительно более выражены. При IIIА гемодинамической группе возможна радикальная коррекция порока, и давление после операции снижается. В IIIБ и IV группе хирургическое лечение не показано. Дифференциальный диагноз между IIIА и Б группами сложен, и нередко для решения вопроса об операбельности порока необходимо выполнить внутрисосудистое ультразвуковое исследование и/или биопсию легкого для изучения морфологических изменений в легочных сосудах. Для оценки этих изменений наиболее часто используется классификация, предложенная Д. Хитом и Дж. Эдвардсом в 1958 г. (табл. 2).

При цианотических формах ВПС наличие сброса венозной крови в артериальную или смешение крови ведут к увеличению объема крови в большом круге кровообращения и уменьшению в малом, что приводит к снижению насыщения крови кислородом (гипоксемии) и к появлению цианоза кожи и слизистых. Для улучшения доставки кислорода к органам и повышения эффективности вентиляции происходит развитие коллатерального кровообращения между сосудами большого и малого круга кровообращения. Перестройка коллатеральной сети кровообращения происходит в сосудах всех органов. Особенно это выражено в сосудах сердца, легких и головного мозга.
Благодаря компенсаторным механизмам состояние больного с цианотическими формами ВПС, несмотря на тяжелые нарушения гемодинамики, может быть длительно удовлетворительным, но постепенно компенсаторные механизмы истощаются, длительная гиперфункция миокарда приводит к развитию тяжелых необратимых дистрофических изменений в сердечной мышце. Поэтому оперативное вмешательство при цианотических пороках (радикальное или паллиативное) показано в самом раннем детском возрасте.
Диагностика
Первичная диагностика ВПС основывается на данных неинвазивных методов исследования. Большое значение для диагностики имеет целенаправленный сбор анамнеза у родителей ребенка. При бледных пороках сердца необходимо выяснить, часто ли болеет ребенок респираторными инфекциями, были ли у него пневмонии, так как это говорит о большом сбросе крови слева-направо. С другой стороны, прекращение респираторных инфекций у больного с большим сбросом крови в малый круг говорит о начале развития легочной гипертензии. Это должно быть поводом для направления больного к кардиохирургу. Естественное течение ВПС может осложниться развитием инфекционного эндокардита, поэтому необходимо выяснить, бывают ли у ребенка подъемы температуры тела без признаков респираторной инфекции. Следует также выяснить, не было ли у больного синкопальных состояний, судорожного синдрома, которые могут быть следствием аритмий сердца.
При осмотре ребенка с подозрением на ВПС необходимо отметить цвет кожных покровов и слизистых. Цианоз может быть периферическим и генерализованным. Важно отметить наличие или отсутствие цианоза на всех 4 конечностях, так как при некоторых ВПС наблюдается дифференцированный цианоз (предуктальная коарктация аорты, транспозиции магистральных сосудов в сочетании с перерывом дуги аорты). При осмотре грудной клетки необходимо отметить деформацию грудной клетки в области сердца — появление так называемого сердечного горба (по величине и локализации которого можно косвенно судить о сложности ВПС и/или развитии легочной гипертензии).
При пальпации грудной клетки у больного с ВПС можно отметить смещение верхушечного толчка, изменение его площади, наличие “дрожания” над областью сердца. Пальпация позволяет оценить размеры печени и селезенки. Методом перкуссии определяют размеры сердца, печени и селезенки.
Аускультация является наиболее информативным методом физикального обследования больных с ВПС. При аускультации можно отметить изменение тонов сердца (усиление, ослабление или расщепление), появление шумов, а также их локализацию, иррадиацию и место максимального выслушивания. Интенсивность шума не всегда коррелирует с тяжестью порока, например, при ВПС с легочной гипертензией и синих пороках со стенозом легочной артерии эта зависимость носит обратный характер. При аускультации легких можно выявмть признаки застоя в малом круге.
Физикальное исследование дополняется проведением неинвазивного инструментального обследования, которое включает электрокардиографию (ЭКГ), фонокардиографию (ФКГ) и рентгенографию органов грудной клетки.
ЭКГ позволяет судить о гипертрофии различных отделов сердца, патологических отклонениях электрической оси, наличии нарушений ритма и проводимости. Изменения на ЭКГ не являются специфичными для какого-либо порока, но в сочетании с данными, полученными при клиническом обследовании и с помощью других неинвазивных методов, позволяют судить о тяжести порока. Разновидностью метода ЭКГ является холтеровское суточное ЭКГ-мониторирование, которое помогает выявить скрытые нарушения ритма и проводимости.
Следующим неинвазивным методом обследования кардиологических больных является ФКГ, которая воспроизводит данные аускультации сердца и позволяет более детально и количественно оценить характер, продолжительность и локализацию сердечных тонов и шумов.
Рентгенография органов грудной клетки дополняет предыдущие методы и позволяет оценить: состояние малого круга кровообращения (наличие артериального или венозного застоя, снижение наполнения сосудов легких); расположение, форму, размеры сердца и его отдельных камер; изменения со стороны других органов и систем (легкие, плевра, позвоночник, а также расположение внутренних органов).
Сочетание ЭКГ, ФКГ и рентгенография органов грудной клетки позволяет диагностировать большинство изолированных пороков и предположить наличие сложных ВПС.
Наиболее высокоинформативным неинвазивным методом исследования является эхокардиография (ЭХОКГ). С появлением данной методики, особенно двухмерной ЭХОКГ, значительно расширились возможности диагностики ВПС. Этот метод позволяет провести анатомически точную диагностику дефектов перегородок сердца, поражения атриовентрикулярных и полулунных клапанов, размеры и расположение камер сердца и магистральных сосудов, а также оценить сократительную способность миокарда. При определенных пороках (неосложненные ДМПП, ДМЖП, ОАП, частично открытый АВК, коарктация аорты) можно выполнить операцию без проведения катетеризации сердца. Однако в ряде случаев при сложных ВПС и сопутствующей легочной гипертензии необходимо провести катетеризацию сердца и ангиокардиографию, так как эти методы позволяют провести точную анатомическую и гемодинамическую диагностику ВПС. Проведение катетеризации сердца возможно только в условиях специализированной кардиохирургической клиники. В настоящее время при проведении катетеризации сердца в случае необходимости выполняется электрофизиологическое исследование для уточнения механизма аритмий сердца, оценки функции синусового и атриовентрикулярного узлов, а также проводятся различные эндоваскулярные операции: баллонная ангиопластика при стенозах легочной артерии и аорты; эмболизация небольших ОАП, коронаросердечных фистул, аортолегочных коллатералей; баллонная атриосептостомия при простой ТМС и стентирование легочных сосудов при периферических стенозах.
Тактика хирургического лечения
Тактика оказания помощи больным с ВПС строится с учетом течения порока, эффективности консервативного лечения, возможности и риска проведения хирургического лечения. После установления диагноза необходимо решить:
1. Как лечить больного (медикаментозно или хирургически)?
2. Определить сроки выполнения операции.
Ответить на эти вопросы помогает классификация, предложенная J. Kirklin и соавт. (1984).
0-я группа – больные с ВПС, с незначительными нарушениями гемодинамики, которые не нуждаются в операции.
1-я группа – больные, состояние которых позволяет провести операцию в плановом порядке ( через год и более).
2-я группа – больные, которым операция показана в ближайшие 3–6 мес.
3-я группа – больные с тяжелыми проявлениями ВПС, которых необходимо оперировать в течение нескольких недель.
4-я группа – больные, нуждающиеся в экстренной операции (в течение 48 ч после госпитализации).
Наиболее сложная проблема в кардиохирургии – операция у детей первого года жизни с ВПС. Хирургическая летальность в последние годы значительно снижена и отличается от высокой естественной смертности при ВПС. Операция у детей первого года жизни выполняется в том случае, если консервативными методами не удается достичь стабилизации состояния. Большинство неотложных операций выполняются у детей с цианотическими ВПС.
Если у новорожденного с ВПС отсутствуют признаки сердечной недостаточности, цианоз выражен умеренно, то консультация кардиохирурга может быть проведена позднее. Наблюдение за такими детьми осуществляет кардиолог по месту жительства. Такая тактика позволяет провести обследование больного в более благоприятных условиях, снизить риск проведения инвазивных методов исследования и оперативного вмешательства.
В более поздней возрастной группе хирургическая тактика при ВПС зависит от тяжести патологии, предполагаемого прогноза, возраста и массы тела больного. K.Turley и соавт. в 1980 г. предложили разделить ВПС на 3 группы, в зависимости от вида возможной операции.
К 1-й группе относятся такие наиболее часто встречающиеся пороки, как ОАП, ДМЖП, ДМПП, частично открытый АВК, коарктация аорты, стеноз и недостаточность митрального и аортального клапанов. При установлении данных пороков единственным выбором может быть операция. Она может быть отложена, если нарушения гемодинамики нерезко выражены, а возраст ребенка и масса тела слишком малы (более поздний возраст и достаточная масса тела снижают риск выполнения кардиохирургических вмешательств).
Во 2-ю группу входят сложные цианотические пороки, такие, как тетрада Фалло, стеноз легочной артерии, атрезия легочной артерии 1-го типа, транспозиция магистральных сосудов и др. Выбор между радикальной и паллиативной операцией зависит от анатомической тяжести порока, степени гипоксемии и массы тела ребенка.
К 3-й группе относятся ВПС, при которых возможна только паллиативная или гемодинамическая коррекция порока. К ней относятся различные варианты сложных пороков: атрезия трикуспидального и митрального клапанов, двухкамерное сердце, синдром гипоплазии правого и левого сердца, единственный желудочек сердца и др.
Радикальная коррекция простых неосложненных пороков не представляет технических трудностей для специализированной кардиохирургической клиники. При ДМЖП и ДМПП выполняется ушивание или пластика дефектов заплатой, при ОАП – перевязка или пересечение протока. При выраженной гипоксемии первым этапом у больного с ВПС проводится паллиативная операция – наложение различных межсистемных анастомозов. После проведения операции улучшается насыщение крови кислородом, что позволяет ребенку развиваться в более благоприятных условиях. Выполнение двухэтапных операций, по данным различных авторов, не только не увеличивает риск вмешательства, но уменьшает летальность при радикальной коррекции.
При некоторых анатомически сложных ВПС, когда отсутствуют или недоразвиты различные отделы сердца (атрезия трикуспидального и митрального клапанов, единственный желудочек сердца, двухкамерное сердце и т.д.) выполнение радикальной операции не представляется возможным и единственной операцией может быть гемодинамическая коррекция внутрисердечной гемодинамики, которая позволяет разделить артериальные и венозные потоки крови, не устраняя полностью анатомические пороки. К ним относятся различные модификации гемодинамической коррекции по методу Фонтена, Мастарда и Сенинга.
Список литературы Вы можете найти на сайте http://www.rmj.ru
1. Бураковский В.И., Бухарин В.А. Константинов С.А. и др. Врожденные пороки сердца. В кн. Частная хирургия болезней сердца и сосудов / Под ред. В.И. Бураковского и С.А.Колесникова. М.: Медицина, 1967; 315—23.
2. Бураковский В.И., Бухарин В.А., Плотникова Л.Р. Легочная гипертензия при врожденных пороках сердца. М. Медицина, 1975; 247.
3. Амосов Н.М., Бендет Я.А. Терапевтические аспекты кардиохирургии. Киев: Здоровье, 1983; 33—96.
4. Белоконь Н.А., Кубергер М.Б. Болезни сердца и сосудов у детей. Руководство для врачей. В 2 томах. — М. Медицина, 1987; 918.
5. Бураковский В.А., Бухарин В.А., Подзолков В.П. и др. Врожденные пороки сердца. В кн. Сердечно-сосудистая хирургия / Под ред. В.И. Бураковского, Л.А. Бокерия. М. Медицина, 1989; 345—82.
6. Иваницкий А.В., Роль рентгенологического исследования в диагностике пороков сердца у детей. Педиатрия. 1985; 8 (7) 55—7.
7. Н.А.Белоконь, В.П. Подзолков. Врожденные пороки сердца. М. Медицина, 1991; 352.
При некоторых анатомически сложных ВПС, когда отсутствуют или недоразвиты различные отделы сердца (атрезия трикуспидального и митрального клапанов, единственный желудочек сердца, двухкамерное сердце и т.д.) выполнение радикальной операции не представляется возможным и единственной операцией может быть гемодинамическая коррекция внутрисердечной гемодинамики, которая позволяет разделить артериальные и венозные потоки крови, не устраняя полностью анатомические пороки. К ним относятся различные модификации гемодинамической коррекции по методу Фонтена, Мастарда и Сенинга.
Врожденные пороки сердца у детей. Этиология, классификация, пренатальная диагностика.
Врожденные пороки сердца – одна из наиболее частых аномалий развития, занимающая третье место после аномалий центральной нервной системы и опорно-двигательного аппарата. Рождаемость детей с врожденными пороками сердца во всех странах мира, включая Россию, составляет от 2,4 до 14,2 на 1000 новорожденных.
Проблемы диагностики и лечения врожденных пороков сердца чрезвычайно важны в детской кардиологии. Терапевны и кардиологи, как правило, недостаточно знакомы с этой патологией в силу того, что подавляющее большинство детей к половозрелому возрасту уже получили хирургическое лечение или погибли.
Причины возникновения врожденных пороков сердца неясны. Пороки сердца возникают на 3-7 неделе беременности, во время закладки и формирования структур сердца. В первом триместре беременности (в срок 4-8-12 недель) под влиянием различных тератогенных воздействий нарушается процесс формирования анатомических структур сердечно-сосудистой системы, в связи с чем образуются дефекты в перегородках сердца, сужение сердечных устьев, изменение формы клапанов и т.д.
К врожденным порокам сердца традиционно относят так же не закрывшиеся в результате нарушения постнатальной перестройки гемодинамики фетальные коммуникации (в частности, открытый артериальный проток).
Актуальность
Значительной распространенностью ВПС в детской популяции. В России ежегодно рождается до 35000 детей с ВПС, что составляет 8-10 на 1000 родившихся живыми детей. В Ярославле и области статистика распространенности ВПС совпадает с общероссийской. Заболеваемость ВПС среди детей в возрасте от 0 до 14 лет составляет 8,11‰, среди подростков – 5,4‰ (по итогам 2009 года). На долю ВПС приходится 22% от всех врожденных пороков развития.
Тенденцией к росту распространенности врожденных пороков сердца.
– рост наследственной и инфекционной патологии.
– ухудшение экологической обстановки,
– «старение» беременных, ухудшение состояния их здоровья, «вредные привычки» и др.
Наряду с этим увеличивается количество более сложных и тяжелых пороков сердца.
Высокой летальностью при ВПС:
- По данным Т.В.Парийской и В.И. Гикавого (1989) в Санкт-Петербурге летальность пациентов с ВПС в течение первого года жизни составляет 40%, из них среди новорожденных – 48,3%, среди детей 1-3 месяца – 32,4%, 4-8 месяцев – 19,3%.
- После первого года жизни летальность от ВПС снижается и среди детей в возрасте от 1 до 15 лет она составляет 5% от общего числа больных, родившихся с ВПС (Н.А.Белоконь, В.И.Подзолков, 1991).
Поэтому ВПС занимают одно из ведущих мест в структуре причин младенческой смертности (2-3 место) и детской инвалидности. Среди врожденных пороков развития, приводящих к инвалидности, ВПС составляют около 50% (Е.Ф.Лукушкина, 2000; Л.И.Меньшикова, Т.Т.Кузьмина, 2003).
Этиология врожденных пороков сердца
– экзогенные и эндогенные факторы среды
ВПС, обусловленные генетическими нарушениями, могут встречаться как изолированно, так и в составе синдромов со множественными врожденными пороками развития – МВПР:
– синдром Дауна (трисомия 21),
– синдром Патау (трисомия 13),
– синдром Эдвардса (трисомия 18),
– синдром Шерешевского-Тернера (Х0).
Полигенно-мультифакториальное наследование является причиной ВПС в 90% случаев.
Влияние внешних факторов:
- Инфекционные агенты (вирус краснухи, цитомегаловирус, вирус простого герпеса, вирус гриппа, энтеровирус, вирус Коксаки В и др).
- Соматические заболевания матери, в первую очередь, сахарный диабет, приводят к развитию гипертрофической кардиомиопатии и ВПС.
- Профессиональные вредности и вредные привычки матери (хронический алкоголизм, компьютерное излучение, интоксикации ртутью, свинцом, воздействие ионизирующей радиации и т.д.).
- Экологические неблагополучия.
- Социально-экономические факторы.
- Психо-эмоциональные стрессовые ситуации.
Факторы риска рождения детей с ВПС:
– эндокринные заболевания супругов;
– токсикоз и угроза прерывания первого триместра беременности;
– мертворожденные в анамнезе;
– наличие детей с ВПС у ближайших родственников.
Количественно оценить риск рождения в семье ребенка с ВПС может только генетик, но дать предварительный прогноз и направить родителей на медико-биологическую консультацию может и должен каждый врач.
Классификация врожденных пороков сердца (Мардер, 1953)
Гемодинамическая группа ВПС
Без цианоза
С цианозом
С гиперволемией малого круга кровообращения
ТМА без легочного стеноза, ОАС, тотальный АДЛВ, двойное отхождение сосудов от правого желудочка. Компл. Эйзенменгера, леводеленность (гипоплазия левых отделов сердца)
С гиповолемией малого круга кровообращения
Пороки Фалло, ТМА со стенозом легочной артерии, атрезия трехстворчатого клапана, аномалия Эбштейна,
праводеленность (гипоплазия правых отделов сердца)
С гиповолемией большого круга кровообращения
Стеноз устья аорты, коарктация аорты, перерыв дуги аорты
Без нарушений гемодинамики в большого и малого кругов кровообращения
Аномалии положения сердца, МАРС, двойная дуга аорты, аномалии отхождения сосудов от дуги аорты
Рабочая группировка 9 наиболее распространенных ВПС (Н.А.Белоконь, В.П. Подзолков, 1991)
1. Врожденные пороки сердца бледного типа с артериовенозным шунтированием крови:
– дефект межжелудочковой перегородки (ДМЖП),
– дефект межпредсердной перегородки (ДМПП),
– открытый артераиальный проток (ОАП).
2. Врожденные пороки сердца синего типа с венозно-артериальным шунтированием крови:
– транспозиция магистральный сосудов,
– атрезия трехстворчатого клапана.
3. Врожденные пороки сердца бледного типа без сбросов крови, но с препятствием току крови из желудочков:
– стеноз устья легочной артерии,
– стеноз устья авторы,
Фазы естественного течения врожденного порока сердца
I. Фаза адаптации.
Продолжительность фазы адаптации от нескольких недель до 2-х лет.
В связи с особенностями внутриутробной гемодинамики (наличие плацентарного круга кровообращения и фетальных коммуникаций) у плода при большинстве ВПС не развивается декомпенсация.
С рождением ребенка сердечно-сосудистая система новорожденного адаптируется к внеутробным условиям гемодинамики: происходит разобщение кругов кровообращения, становление как общей, так и внутрисердечной гемодинамики, начинает функционировать малый круг кровообращения с последующим постепенным закрытием фетальных коммуникаций: артериального протока и овального окна.
В этих условиях при неразвитых еще механизмах компенсации гемодинамика часто оказывается неадекватной, развиваются различные осложнения. Состояние ребенка прогрессивно и резко ухудшается, что заставляет проводить консервативную терапию и экстренные хирургические вмешательства.
Осложнения фазы адаптации врожденного порока сердца
У больных с ВПС первой и третьей гемодинамических групп:
– Недостаточность кровообращения (ранняя, аварийная»)
– Ранняя легочная гипертензия
– Нарушения ритма и проводимости
У больных с цианотическими ВПС:
– Одышечно-цианотические (гипоксемические ) кризы.
– Нарушение мозгового кровообращения.
При любых ВПС высок риск развития бактериального эндокардита.
2. Фаза относительной компенсации (фаза мнимого благополучия). Продолжается от нескольких месяцев до десятков лет.
Для этого периода характерно подключение большого количества компенсаторных механизмов с целью обеспечения существования организма в условиях нарушенной гемодинамики.
Выделяют кардиальные и экстракардиальные компенсаторные механизмы.
К кардиальным относятся:
– увеличение активности ферментов цикла аэробного окисления (сукцинатдегидрогеназы);
– вступление в действие анаэробного обмена;
К экстракардиальным механизмам компенсации относятся:
– активация симпатического звена ВНС, что приводит к увеличению числа сердечных сокращений и централизации кровообращения;
– повышение активности ренин-ангиотензин-альдостероновой системы, вследствие чего повышается артериальное давление и сохраняется адекватное кровоснабжение жизненно важных органов, а задержка жидкости приводит к увеличению объёма циркулирующей крови.
При этом задержке излишней жидкости в организме и формированию отеков противостоит предсердный натрийуретический фактор;
– стимуляция эритропоэтина приводит к увеличению количества эритроцитов и гемоглобина и, таким образом, повышению кислородной ёмкости крови.
Осложнения фазы относительной компенсации
- Бактериальный эндокардит.
- Нарушения ритма и проводимости.
- Относительная анемия.
3. Фаза декомпенсации (терминальная фаза).
Для этого периода характерно истощение компенсаторных механизмов и развитие рефрактерной к лечению сердечной недостаточности; формирование необратимых изменений во внутренних органах.
Осложнения фазы декомпенсации ВПС (терминальной фазы)
У больных с ВПС первой и третьей
- Хроническая недостаточность кровообращения.
- Легочная гипертензия.
- Дистрофия.
- Нарушения ритма и проводимости.
У больных с цианотическими ВПС:
- Одышечно-цианотические (гипоксемические)
- Нарушение мозгового кровообращения.
- Относительная анемия.
- Гипоксический геморрагический васкулит.
- Гепато-ренальный синдром.
- Гипоксические артриты.
У больных с аортальными пороками:
- Артериальная гипертензия.
- Стенокардитический синдром.
При всех ВПС сохраняется риск развития бактериального эндокардита
Пренатальная диагностика и пренатальная оценка тяжести врожденного порока сердца
Некоторым детям с ВПС для сохранения жизни неотложные хирургические вмешательства необходимо провести в первые часы после рождения. Поэтому пренатальная диагностика и пренатальная оценка тяжести ВПС иногда имеет решающее значение для обеспечения ребенка своевременной специализированной (в том числе, кардио-хирургической) помощью.
Пренатальная диагностика плода методом ультразвукового исследования (УЗИ) проводится в настоящее время планово всем беременным женщинам в 10-12, 20-22 и в 32-34 недели беременности. Среди большого перечня задач этого исследования – диагностика пороков развития, в том числе пороков развития сердечно-сосудистой системы.
Выявленные пренатально врожденного порока сердца по степени тяжести и риска неблагоприятного прогноза делятся на 5 категорий
Пороки сердца первой и второй категорий, в частности, транспозиция магистральных артерий (ТМА), двойное отхождение сосудов от правого желудочка, общий артериальный ствол, крайняя степень тетрады Фалло, атрезия легочной артерии с агенезией клапанов, перерыв дуги аорты и др. часто создают критические жизнеугрожающие ситуации в периоде новорожденности и в грудном возрасте. Дети с этими пороками сердца должны попасть в поле зрения кардиолога и кардиохирурга сразу после рождения.
В Москве на базе Городской клинической больницы № 67 создано специализированное отделение, куда госпитализируются для родоразрешения женщины, беременные плодом с «критическим» вариантом ВПС. При необходимости, новорожденный ребенок сразу транспортируется для хиргического лечения в Научный Центр сердечно-сосудистой хирургии им. Бакулева.
При некоторых пороках сердца первой группы и на современном уровне развития кардиохирургии невозможно выполнить полноценную хирургическую коррекцию. Они сопровождаются высокой естественной и послеоперационной летальностью. Если пренатально выявлены именно такие пороки, то встает вопрос о прерывании беременности (!?).
Третья категория – относительно простые ВПС, не угрожающие жизни больного непосредственно после рождения: (ДМЖП небольшого диаметра, мышечные ДМЖП, умеренный аортальный или легочный стеноз, изолированная декстрокардия, двухстстворчатый аортальный клапан). В большинстве случаев эти ВПС подлежат диспансерному наблюдению и плановой хирургической коррекции. Прогноз благоприятный.
Четвертая категория: кардиомиопатии; изолированные аритмии, опухоли сердца. Эта патология подлежит терапевтическому лечению. К операции прибегают только в случае злокачественного течения заболевания.
К пятой категории отнесены фетальные коммуникации. После рождения они рассматриваются как патология при персистировании (т.е. если остаются открытыми), начиная с определенного возраста ребенка.
Ранняя постнатальная диагностика врожденного порока сердца
Клинические симптомы, настораживающие в отношении ВПС у новорожденных детей:
(врач-неонатолог родильного дома и отделений патологии новорожденных)
1. Центральный цианоз с рождения или через некоторое время, который не устраняется назначением кислорода.
2. Шум над областью сердца может быть признаком порока, однако у ребенка возможны и физиологические шумы и шумы, связанные с персистенцией фетальных коммуникаций. Кроме того, наиболее тяжелые пороки сердца часто не сопровождаются шумом.
3. Постоянная тахикардия или брадикардия, не связанная с неврологической патологией или соматическим состоянием.
4. Тахипноэ более 60 в минуту, в том числе во сне, с втяжением уступчивых мест грудной клетки или без него.
5. Симптомы недостаточности кровообращения (включая гепатомегалию, отеки, олигурию).
6. Нерегулярный ритм сердца.
7. Уменьшение или отсутствие пульсации на нижних конечностях (КА);
8. Генерализованное ослабление пульса – подозрение на гипоплазию левых отделов сердца или циркуляторный шок.
9. «Высокий» пульс – подозрение на сброс крови из аорты с низким диастолическим АД (ОАП, ОАС).
Дополнительные обследования при подозрении на ВПС в периоде новорожденности:
- Гипероксический тест – положителен при цианозе центрального генеза. При ВПС с право-левым шунтированием крови общий ранний цианоз имеет центральное происхождение и обусловлен сбросом венозной крови в большой круг кровообращения и снижением парциального содержания кислорода в артериальной крови. Новорожденному ребенку с выраженным общим цианозом проводится ингаляция 100% кислорода через маску в течение 10 – 15 минут под контролем анализа газов крови. При ВПС цианоз не уменьшается или снижается незначительно. Результаты теста должны рассматриваться в комплексе с другими диагностическими признаками.
- ЭКГ, ЭХОКгр, рентгенография органов грудной клетки в 3-х проекциях (фронтальной, правой и левой переднекосых).
- Измерение АД на плечевых и бедренных артериях.
Критерии диагностикиВПС в грудном и раннем возрасте (участковый педиатр, врач общей практики, детский кардиолог)
- Клинические данные: цианоз, одышка, отставание в физическом развитии, симптомы СН, сердечный горб, кардиомегалия, изменение тонов и ритма сердца, шумы органического характера, изменение АД.
- Электрокардиография: положение эл. оси сердца, гипертрофия миокарда, дисметаболические изменения в миокарде.
- ЭХОКгр.
- Изменения на рентгенограмме органов грудной полости.
- Артериальная гипоксемия (по показателям газов крови)
- Гемолитико-уремический синдром у детей: клиническая картина
- Гемолитико-уремический синдром у детей: диагностика, лечение профилактика
– атрезия трехстворчатого клапана.
Врачебная классификация: врождённые болезни
 В медицинской литературе, возможностей проявления ВПС перечислено огромное множество. Одни варианты заболевания распространены более чем другие.
В медицинской литературе, возможностей проявления ВПС перечислено огромное множество. Одни варианты заболевания распространены более чем другие.
Отчасти диагностику патологий и выявления, какие бывают врожденные пороки сердца, облегчило возникновение новых технологий, и возможность напрямую видеть и оценивать работу сердечной мышцы.
Точных данных о том, почему на этапах формирования плода может появиться данное нарушение развития сердечной мышцы, не выявлено.
 Однако исследователи предполагают связь между инфекционным заболеванием беременной матери, радиационным излучением, недостатком питательной пищи и будущим заболеванием родившегося ребёнка. Обычно порок выражается в том, что не заращиваются сердечные перегородки или боталлов проток.
Однако исследователи предполагают связь между инфекционным заболеванием беременной матери, радиационным излучением, недостатком питательной пищи и будущим заболеванием родившегося ребёнка. Обычно порок выражается в том, что не заращиваются сердечные перегородки или боталлов проток.
Медицина выявляет множество классификаций врождённых пороков сердца. Условно, их делят на две группы:
- белые, при которых не происходит смешение артериальной и венозной крови, а сама кровь сбрасывается слева направо;
- синие, с право-левым сбросом крови, при которых происходит смешение артериальной и венозной крови, а сама кровь сбрасывается справа налево.
Также существуют следующие виды пороков сердца: с перекрестным сбросом, с препятствиями нормальному кровотоку, пороки сердечного клапана, венечных артерий и врожденные нарушения сердечного ритма.
На этот момент существует Международная Номенклатура врождённых пороков, для организации общей диагностической системы.
Подобная классификация врожденных пороков сердца является наиболее распространённой — зачастую её знают не только медики, но и родители ребёнка с заболеванием.
 К болезням, характеризующимся сбросом крови справа-налево, относят имеющие повреждения межжелудочковой и межпредсердной перегородок, открытый артериальный проток, дренаж легочных вен, открытый общий атриовентрикулярный канал, дефекты аортолегочной перегородки.
К болезням, характеризующимся сбросом крови справа-налево, относят имеющие повреждения межжелудочковой и межпредсердной перегородок, открытый артериальный проток, дренаж легочных вен, открытый общий атриовентрикулярный канал, дефекты аортолегочной перегородки.
К заболеваниям, при которых кровь сбрасывается справа-налево, относят те, в которых происходит изменение магистральных сосудов, аномалию Эбштейна, отсутствие трехстворчатого сердечного клапана, общий артериальный ствол, развитие одного желудочка, гипоплазию левого сердца и правого желудочка.
 Заболевания, влияющие на нарушение кровотока, включают в себя сужение аортального сердечного клапана, его стеноз, или стеноз клапана артерии лёгкого, стеноз митрального клапана сердечной мышцы и ветвей лёгочных артерий.Пороки клапанного сердечного аппарата являются отдельной группой. В неё включены только те нарушения, которые связаны с патологиями развития атриовентрикулярных или полулунных клапанов без каких-либо других дисфункций.
Заболевания, влияющие на нарушение кровотока, включают в себя сужение аортального сердечного клапана, его стеноз, или стеноз клапана артерии лёгкого, стеноз митрального клапана сердечной мышцы и ветвей лёгочных артерий.Пороки клапанного сердечного аппарата являются отдельной группой. В неё включены только те нарушения, которые связаны с патологиями развития атриовентрикулярных или полулунных клапанов без каких-либо других дисфункций.
В группу включаются недостаточность и стеноз митрального клапана, а также недостаточность клапанов лёгочной артерии и аорты.
Пороки венечных артерий включают все отклонения от их типичного состояния: патологическое отхождение их устьев, коронаро-сердечные свищи.
Синие пороки именуются таковыми из-за цианоза, к которому приводят. В этом случае кожа больного приобретает голубоватый цвет из-за нехватки кислорода.
В случае повреждений межпредсердной или межжелудочковой перегородки кровь циркулирует из левой части сердца в правую, сокращая эффективность работы сердца. Это один из самых часто встречающихся пороков.
Поражающая сердце гипоплазия обычно приводит к недоразвитости правого или левого желудочка. В результате лишь одна сторона сердца способна с эффективностью перенаправлять кровоток к телу и лёгким.
Этот тип заболевания является наиболее серьёзным. Обычно является синим пороком сердца.
- по состоянию общего движения крови по сосудам;
- по причинам возникновения;
- по местонахождению проявления заболевания;
- по функциональной форме;
- по степени проявления.
Условное разделение
 Еще одна категория врожденных пороков подразделяется на 2 типа. Самый обширный из них — это, так называемые, белые, когда происходит лево-правый сброс крови, когда не происходит смешивания венозной и артериальной крови. Относят сюда 4 группы: с обеднением малого (пульмональный стеноз изолированного типа) или большого круга кровообращений (коарктация аорты, стеноз аортальный изолированный); с обогащением малого круга (AB-коммуникация, дефект перегородок между предсердиями или желудочками); без чрезмерного нарушения гемодинамики (например, при разных видах дистопии сердца).
Еще одна категория врожденных пороков подразделяется на 2 типа. Самый обширный из них — это, так называемые, белые, когда происходит лево-правый сброс крови, когда не происходит смешивания венозной и артериальной крови. Относят сюда 4 группы: с обеднением малого (пульмональный стеноз изолированного типа) или большого круга кровообращений (коарктация аорты, стеноз аортальный изолированный); с обогащением малого круга (AB-коммуникация, дефект перегородок между предсердиями или желудочками); без чрезмерного нарушения гемодинамики (например, при разных видах дистопии сердца).
Другая категория, входящая в такое условное разделение врожденных пороков — синие. В данном случае кровь венозная и артериальная смешиваются, однако сброс крови право-левый. Здесь тоже присутствует обеднение и обогащение малого круга кровообращения. К первому типу относят такие нарушения, как комплекс Эйзенменгера, транспозицию магистральных сосудов. Обеднение круга происходит при аномалии Эбштейна, если развита тетрада Фалло.
Помимо этого выделяют еще целый ряд аномалий (среди них и тетрада Фалло), которые присутствуют в медицинской практике, но не включены в перечень, представленный Международной номенклатурой. Сюда относят:
Врожденный порок сердца, с точки зрения анатомии и физиологии
Сердце – мышечный орган, обеспечивающий поступление крови по сложной системе кровоснабжения к каждой клеточке тела. Строение сердца обеспечивает создание большого и малого (легочного) кругов кровообращения путём наличия перегородки, делящей сердце на правую и левую половины. Они не сообщаются между собой.
Кроме того, каждая из этих половин разделяется на предсердие и желудочек с помощью клапана, препятствующего обратному току крови. Подобная система клапанов присутствует и в крупных сосудах, отходящих от сердца.
Любое нарушение в строении сердца и последовательности сообщающихся с ним сосудов, чревато серьёзными осложнениями, угрожающими жизни. Об этом говорит статистика, указывающая на смертность детей с наличием ВПС в 80% случаев, при отсутствии хирургической коррекции в течении года после рождения.
Изменение клапанной системы носят следующий характер:
- Недостаточность (относится так же и к перегородке, разделяющей сердце на правую и левую половины) – дефекты, допускающие постоянное сообщение между полостями.
- Стеноз – сужение диаметра просвета естественного сообщения между полостями.
- Комбинированный порок – сочетание стеноза и недостаточности на одном клапане.
- Сочетанный порок — изменения на разных клапанах.
Суть нарушений при сформированных пороках сводятся:
Изменения нормальных потоков и показателей кровообращения.
- Возникает повышенная нагрузка на миокард:
- за счёт увеличения объёма крови, которую надо протолкнуть через сердце (при недостаточности);
- за счёт сопротивления (уменьшение диаметра отверстия, через которое должна пройти кровь при сокращении).
- Увеличивается частота и сила сердечных сокращений.
- Возрастает необходимость миокарда в энергии и питательных веществах.
- Через некоторое время (для каждого порока этот показатель индивидуален) происходит истощение ресурсов.
- Сердце не справляется с нагрузкой:
- сокращение сердца происходит не в полном объёме;
- увеличивается объём остаточной крови в полостях после сокращения;
- происходит увеличение сердца в размерах с истончением стенок, оно растягивается как воздушный шарик.
- Возникает повышение давления в одном из кругов кровообращения, а затем и в обоих.
- Снабжение внутренних органов кислородом и питательными веществами происходит не в полном объёме. Наступает их кислородное голодание (гипоксия) и дисметаболические изменения.
- При явлениях прогрессирования сердечной недостаточности, наступает смерть.
Изменение качества крови (при смешивании артериальной и венозной крови).
Надо отметить, что в чистом виде, существование последнего нарушения возможно
только во внутриутробном периоде. При рождении к нему присоединяются и начинают прогрессировать гемодинамические нарушения.
Имеется группа и менее тяжких изменений в клапанном аппарате, без нарушения кровообращения, наличие которых позволяет выявлять врождённые пороки сердца у взрослых в достаточно зрелом возрасте. Они связаны со слабостью или незрелостью клапанного аппарата.
К примеру, пролапс митрального клапана, когда во время сокращения, одна из створок прогибается в полость предсердия. Если в это время обратно кровь не поступает, или её количество минимально, больной, не испытывая по жизни больших нагрузок, может прожить достаточно долго, не подозревая о наличии врождённого дефекта в сердце.
Некоторое возрастание количества ВПС у взрослых в последнее время связано с улучшением качества диагностических методов. Обращение больного к врачам в таких случаях происходит по поводу появляющихся со временем атеросклеротических изменений в сосудах и в структуре клапанного аппарата, вызывающих определённую симптоматику.
Констатируя этот факт при проведении УЗИ сердца или при других исследованиях, врач-диагност одновременно выявляет у таких больных и пороки сердца, характерные только для врождённой патологии. Подход к лечению врожденных пороков сердца тут индивидуален и зависит от степени выраженности сердечной недостаточности.
- Возникает повышенная нагрузка на миокард:
- за счёт увеличения объёма крови, которую надо протолкнуть через сердце (при недостаточности);
- за счёт сопротивления (уменьшение диаметра отверстия, через которое должна пройти кровь при сокращении).
- Увеличивается частота и сила сердечных сокращений.
- Возрастает необходимость миокарда в энергии и питательных веществах.
- Через некоторое время (для каждого порока этот показатель индивидуален) происходит истощение ресурсов.
- Сердце не справляется с нагрузкой:
- сокращение сердца происходит не в полном объёме;
- увеличивается объём остаточной крови в полостях после сокращения;
- происходит увеличение сердца в размерах с истончением стенок, оно растягивается как воздушный шарик.
- Возникает повышение давления в одном из кругов кровообращения, а затем и в обоих.
- Снабжение внутренних органов кислородом и питательными веществами происходит не в полном объёме. Наступает их кислородное голодание (гипоксия) и дисметаболические изменения.
- При явлениях прогрессирования сердечной недостаточности, наступает смерть.
Что такое врождённый порок сердца и можно ли его вылечить?
Врождённый порок сердца иногда требует врачебной помощи уже в момент появления младенца на свет. Но есть много других дефектов, не проявляющих себя длительное время. У взрослого человека они обнаруживаются в любом возрасте.
Заболевание сердца у ребёнка выявляется по характерным признакам, которые надо знать родителям. Ведь своевременная операция не только спасает жизнь ребёнка. После хирургического лечения дети ничем не отличаются от здоровых сверстников.
Врождённый порок сердца иногда требует врачебной помощи уже в момент появления младенца на свет. Но есть много других дефектов, не проявляющих себя длительное время. У взрослого человека они обнаруживаются в любом возрасте.
Пороки сердца – классификация, диагностика, лечение и прогноз
 Пороками сердца называют врождённые или приобретённые патологии клапанов сердца, стенок или перегородок миокарда, а также отходящих от сердечной мышцы крупных сосудов, в результате чего нарушается нормальный ток крови в миокарде и развивается недостаточность кровообращения.
Пороками сердца называют врождённые или приобретённые патологии клапанов сердца, стенок или перегородок миокарда, а также отходящих от сердечной мышцы крупных сосудов, в результате чего нарушается нормальный ток крови в миокарде и развивается недостаточность кровообращения.
Транспозиция магистральных артерий (сосудов) – критический врождённый порок сердца, который характеризуется желудочково-артериальным дискордантным и предсердно-желудочковым конкордантным соединениям.
Декстрокардия – неправильное расположение сердца, то есть большая его часть находится в правой части грудной клетки полностью симметрично нормальному. При этом происходит “обратное” расположение исходящих и входящих сосудов.
Классификация
Все многообразие сердечных дефектов делят на две большие группы: врожденные и приобретенные пороки сердца. К первой группе относятся те аномалии, что формируются в ходе эмбриогенеза, а ко второй — возникающие у детей и взрослых людей в течение жизни. Каждая из этих групп в свою очередь делится на несколько более мелких категорий.
Врожденные пороки сердца подразделяются на следующие типы.
Пороки с незначительными расстройствами гемодинамики по малому кругу:
- стеноз аорты (сужение главного сосуда, отходящего от сердца);
- коарктация аорты ;
- атрезия (недоразвитие) аортального клапана.

Пороки с повышенным кровотоком в легких:
- дефекты перегородок между отделами сердца (между желудочками — ДМЖП, между предсердиями — ДМПП);
- открытый артериальный проток;
- синдром Лютамбаше.
Пороки с обеднением легочного кровотока:
- болезнь Фалло;
- стеноз легочной артерии.
- аномалия Тауссиг-Бинга;
- транспозиция артерий.
Приобретенные пороки — это преимущественно пороки клапанов сердца. Классифицируются они по нескольким принципам.
По локализация порока (какой клапан поражен):
- аортальный;
- митральный;
- трикуспидальный;
- клапан легочной артерии.

По характеру нарушения:
- стеноз — сужение отверстия клапана;
- недостаточность — неполное сметане створок клапанов;
- комбинированный — стеноз+недостаточность.
К возникновению этих пороков приводят различные заболевания, в ходе которых поражаются сердечные клапаны: ревматизм, атеросклероз, сепсис, травмы.
Пороки с обеднением легочного кровотока:





